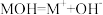用食用白醋(醋酸浓度约1mol/L)常温下进行下列实验,能证明醋酸为弱电解质的是
| A.白醋中滴入石蕊试液呈红色 |
| B.实验测得该白醋的pH为2.3 |
| C.蛋壳浸泡在白醋中有气体放出 |
| D.白醋加入豆浆中有沉淀产生 |
更新时间:2016/12/09 09:52:44
|
【知识点】 弱电解质的电离
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,0.1mol·L-1某一元酸(HA)溶液中 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是| A.溶液中水电离出的c(H+)=10-10mol·L-1 |
| B.溶液中c(H+)+c(A-)=0.1mol·L-1 |
| C.上述溶液加NaA晶体,溶液的c(OH-)增大 |
| D.常温下将HA稀释十倍,氢离子浓度变为原来的十分之一 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,向 饱和的
饱和的 溶液中通入
溶液中通入 气体(气体体积换算成标准状况),发生反应:
气体(气体体积换算成标准状况),发生反应: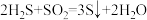 ,测得溶液
,测得溶液 与通入
与通入 的关系如图所示(忽略溶液体积的变化),已知
的关系如图所示(忽略溶液体积的变化),已知 的酸性比
的酸性比 的强。下列有关说法错误的是
的强。下列有关说法错误的是

 饱和的
饱和的 溶液中通入
溶液中通入 气体(气体体积换算成标准状况),发生反应:
气体(气体体积换算成标准状况),发生反应: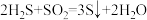 ,测得溶液
,测得溶液 与通入
与通入 的关系如图所示(忽略溶液体积的变化),已知
的关系如图所示(忽略溶液体积的变化),已知 的酸性比
的酸性比 的强。下列有关说法错误的是
的强。下列有关说法错误的是
A.该温度下 的 的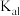 约为 约为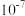 |
B.曲线y代表继续通入 气体后溶液 气体后溶液 的变化 的变化 |
| C.整个过程中,水的电离程度逐渐增大 |
D.a点之后,随 气体的通入 气体的通入 的值保持不变 的值保持不变 |
您最近半年使用:0次

 水溶液的
水溶液的