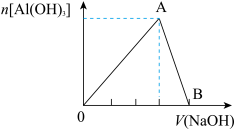
按照要求填空
(1)书写下列反应的化学方程式
①用FeCl3溶液作为腐蚀液刻制铜印刷电路板_______ ;
②工业上粗硅的制取:_______
(2)与量有关的离子方程式书写
①Ba(OH)2溶液与NaHSO4溶液反应后溶液呈中性的离子方程式_______ ;
② Ca(HCO3)2溶液与少量NaOH溶液反应的离子方程式_______ ;
③Al2(SO4)3溶液与过量NaOH溶液反应的离子方程式_______ ;
(1)书写下列反应的化学方程式
①用FeCl3溶液作为腐蚀液刻制铜印刷电路板
②工业上粗硅的制取:
(2)与量有关的离子方程式书写
①Ba(OH)2溶液与NaHSO4溶液反应后溶液呈中性的离子方程式
② Ca(HCO3)2溶液与少量NaOH溶液反应的离子方程式
③Al2(SO4)3溶液与过量NaOH溶液反应的离子方程式
更新时间:2016-12-09 10:16:44
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(K2FeO4)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的 KOH,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为_________ 。
②该反应中的还原剂是_________ ,每生成1mol Na2FeO4 转移_________ mol 电子。
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO +Cl- +H2O(未配平)
+Cl- +H2O(未配平)
① 配平离子反应方程式:_________ 。
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为_________ mol。
③用双线桥标出电子转移的方向和数目_________ 。
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式_________ 。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为
②该反应中的还原剂是
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO
 +Cl- +H2O(未配平)
+Cl- +H2O(未配平)① 配平离子反应方程式:
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为
③用双线桥标出电子转移的方向和数目
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】以黄铜矿(CuFeS2)、FeCl3和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下:
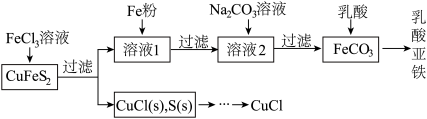
FeCl3溶液与黄铜矿发生反应的离子方程式为___________

FeCl3溶液与黄铜矿发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】Si是现代社会半导体工业发展的基石。
(1)硅元素在自然界中的存在形式有_______
A、游离态B、化合态C、游离态和化合态都有
硅的氧化物属于_______ 氧化物(填“酸性”、“两性”或“碱性" )。
(2)SiO2是玻璃的主要成分之一,SiO2还可以用作_______ ,SiO2与氢氧化钠溶液反应的化学方程式为_______ ,工艺师常用_______ (填物质名称)来雕刻玻璃。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作_______ 。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是_______ 。
A.普通玻璃坩埚B.石英玻璃坩埚C.氧化铝坩埚D.铁坩埚
(4)制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
石英砂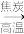 粗硅
粗硅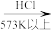 SiHCl3(粗)
SiHCl3(粗) SiHCl3(纯)
SiHCl3(纯) 高纯硅
高纯硅
①写出由纯SiHCl3制备高纯硅的化学反应方程式_______ ;
②整个制备过程必须严格控制无水无氧,SiHCl3遇水剧烈反应生成H2SiO3,HCl和另一种物质,写出配平的化学反应方程式_______
(1)硅元素在自然界中的存在形式有
A、游离态B、化合态C、游离态和化合态都有
硅的氧化物属于
(2)SiO2是玻璃的主要成分之一,SiO2还可以用作
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作
A.普通玻璃坩埚B.石英玻璃坩埚C.氧化铝坩埚D.铁坩埚
(4)制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
石英砂
 粗硅
粗硅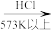 SiHCl3(粗)
SiHCl3(粗) SiHCl3(纯)
SiHCl3(纯) 高纯硅
高纯硅①写出由纯SiHCl3制备高纯硅的化学反应方程式
②整个制备过程必须严格控制无水无氧,SiHCl3遇水剧烈反应生成H2SiO3,HCl和另一种物质,写出配平的化学反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)写出纯碱的化学式:____ 。
(2)写出一氯甲烷的结构式:_____ 。
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象___ 。
(4)写出工业制粗硅的化学方程式:___ 。
(2)写出一氯甲烷的结构式:
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象
(4)写出工业制粗硅的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是______ 。
A.陶瓷 B.玻璃 C.水泥 D.生石灰
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为_____ ,工艺师常用_____ (填物质名称)来雕刻玻璃。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作______ 。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是_____ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(1)下列物质不属于硅酸盐的是
A.陶瓷 B.玻璃 C.水泥 D.生石灰
(2)SiO2是玻璃的主要成分之一,SiO2与氢氧化钠溶液反应的化学方程式为
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)工业上常利用反应2C+SiO2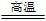 Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
Si+2CO↑制备硅单质,该反应中所含元素化合价升高的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)向AlCl3溶液中持续 滴加NaOH溶液至过量 ,现象为____ 。写出产生上述现象所发生反应的化学方程式:____ ,____ 。
(2)白色絮状沉淀Fe(OH)2在空气中会迅速的变成灰绿色,最后变成红褐色,原因是发生了化学反应,请写出该反应的化学方程式:____ 。
(3)检验溶液中是否含有Fe3+的方法很多。
方法一:向某溶液中加入KSCN溶液,其现象是____ ,说明溶液中含有Fe3+。
方法二:向某溶液中加入NaOH溶液,其现象是____ ,说明溶液中含有Fe3+。
(1)向AlCl3溶液中
(2)白色絮状沉淀Fe(OH)2在空气中会迅速的变成灰绿色,最后变成红褐色,原因是发生了化学反应,请写出该反应的化学方程式:
(3)检验溶液中是否含有Fe3+的方法很多。
方法一:向某溶液中加入KSCN溶液,其现象是
方法二:向某溶液中加入NaOH溶液,其现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】根据要求完成下列化学方程式或离子 方程式。
(1)工业用电解饱和食盐水制氯气的化学方程式为____________________ 。
(2)向新制的Na2S 溶液中滴加新制的氯水的离子 方程式为_______________ 。
(3)氯化铝与过量NaOH 溶液反应的离子 方程式为____________________ 。
(4)乙醇催化氧化制乙醛的化学方程式为____________________ 。
(1)工业用电解饱和食盐水制氯气的化学方程式为
(2)向新制的Na2S 溶液中滴加新制的氯水的
(3)氯化铝与过量NaOH 溶液反应的
(4)乙醇催化氧化制乙醛的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题
(1)在一定量的稀 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
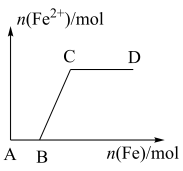
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以_________ 形式存在。
ii.BC段铁元素以_________ 形式存在
iii.CD段铁元素以__________ 形式存在。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________ 。
(1)在一定量的稀
 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以
ii.BC段铁元素以
iii.CD段铁元素以
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】金属及其化合物在人类的历史上有着重要的作用。回答下列有关问题:
(1)向20 mL沸水中逐滴滴加2 mL饱和FeCl3溶液,继续加热至液体呈红褐色,形成的分散系中分散质微粒的直径大小范围是___________ 。
(2)最近两年,随着神舟号系列飞船和蛟龙号潜艇性能的进一步优化,我国已成功实现“上天入地”。在上天入地时,为了给工作仓内工作人员提供氧气,一般要携带一种淡黄色粉末,其化学式为___________ ,将其撒入脱脂棉,滴加几滴水,脱脂棉能被点燃,说明反应___________ 。
(3)电子工业上可用FeCl3溶液腐蚀电路板上的铜,写出该反应的离子方程式:___________ 。
(4)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(5)将硫酸亚铁与稀硫酸混合,二者不反应,滴入H2O2后,溶液很快变成黄色,该反应的离子方程式为___________ 。
(6)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式___________ 。
(1)向20 mL沸水中逐滴滴加2 mL饱和FeCl3溶液,继续加热至液体呈红褐色,形成的分散系中分散质微粒的直径大小范围是
(2)最近两年,随着神舟号系列飞船和蛟龙号潜艇性能的进一步优化,我国已成功实现“上天入地”。在上天入地时,为了给工作仓内工作人员提供氧气,一般要携带一种淡黄色粉末,其化学式为
(3)电子工业上可用FeCl3溶液腐蚀电路板上的铜,写出该反应的离子方程式:
(4)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(5)将硫酸亚铁与稀硫酸混合,二者不反应,滴入H2O2后,溶液很快变成黄色,该反应的离子方程式为
(6)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】请根据物质在生产、生活中的应用填空:
(1)自来水厂对水消毒,常使用的物质是_______ (填“液氯”或“明矾”)。
(2)制造光导纤维的基本原料是_______ 。
(3)常温下盛装浓硝酸可使用的容器是_______ (填“铁罐”或“铜罐”)。
(4)电子工业常用30%的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式_______ 。
(5)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是_______ 。
(6)大型中央空调的制冷剂可用液氨,原因是_______ 。
(1)自来水厂对水消毒,常使用的物质是
(2)制造光导纤维的基本原料是
(3)常温下盛装浓硝酸可使用的容器是
(4)电子工业常用30%的
 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(5)NO是治疗心血管疾病的信使分子,NO与空气接触的反应现象是
(6)大型中央空调的制冷剂可用液氨,原因是
您最近一年使用:0次