高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(K2FeO4)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的 KOH,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为_________ 。
②该反应中的还原剂是_________ ,每生成1mol Na2FeO4 转移_________ mol 电子。
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO +Cl- +H2O(未配平)
+Cl- +H2O(未配平)
① 配平离子反应方程式:_________ 。
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为_________ mol。
③用双线桥标出电子转移的方向和数目_________ 。
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式_________ 。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物 Na2FeO4 中铁元素的化合价为
②该反应中的还原剂是
(2)方法二:
反应:Fe(OH)3+ClO-+OH-—FeO
 +Cl- +H2O(未配平)
+Cl- +H2O(未配平)① 配平离子反应方程式:
②若反应过程中转移了 3mol 电子,则还原产物的物质的量为
③用双线桥标出电子转移的方向和数目
(3)向 Na2FeO4 溶液中加入适量饱和的 KOH 溶液,有 K2FeO4 析出,请写出该反应的化学方程式
更新时间:2022-12-02 14:46:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式___________ 。
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式___________
③过量的二氧化碳通入澄清石灰水中的离子方程式___________ 。
(2)写出下列反应方程式。
①铁在氯气中燃烧___________ ;
②钠和水的反应___________ ;
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:___________ 。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式
③过量的二氧化碳通入澄清石灰水中的离子方程式
(2)写出下列反应方程式。
①铁在氯气中燃烧
②钠和水的反应
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,按要求完成各小题。
(1)元素①的原子结构示意图为_______ ,元素④的原子的电子式为_______ 。
(2)元素②的最简单氢化物的化学式为_______ , 该物质与O2完全燃烧时的化学反应方程式为_______ 。
(3)上述6种元素对应的化合物中,最高价氧化物对应水化物碱性最强的是_______ (填化学式),最高价氧化物对应水化物具有两性的是_______ (填化学式),两者发生反应的离子方程式为_______ 。
| ① | He | ||||||
| ② | ③ | Ne | |||||
| ④ | ⑤ | ⑥ | Ar |
(2)元素②的最简单氢化物的化学式为
(3)上述6种元素对应的化合物中,最高价氧化物对应水化物碱性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】现有下列几种物质:①盐酸;②Na2O;③Na2O2;④Al(OH)3;⑤Na2CO3;⑥H2O;⑦CO2;⑧乙醇;⑨Cu ;⑩NaOH溶液。
(1)其中属于电解质的有___________ (填写序号,下同),属于碱性氧化物的有___________ 。
(2)④与⑩反应的离子方程式为___________ 。
(3)Na2O2,可与CO2发生反应: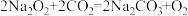 ,该反应中,氧化剂与还原剂的物质的量之比为
,该反应中,氧化剂与还原剂的物质的量之比为___________ 。
(4)若用超氧化钾(KO2)作供氧剂,写出它和CO2反应的化学方程式:___________ 。
(1)其中属于电解质的有
(2)④与⑩反应的离子方程式为
(3)Na2O2,可与CO2发生反应:
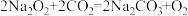 ,该反应中,氧化剂与还原剂的物质的量之比为
,该反应中,氧化剂与还原剂的物质的量之比为(4)若用超氧化钾(KO2)作供氧剂,写出它和CO2反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知反应:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)改写成离子方程式:_______ ;
(2)上述反应中,被还原的物质是_______ ;氧化剂和还原剂个数比_______
(3)用双线桥法标出该反应的电子转移情况_______
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)改写成离子方程式:
(2)上述反应中,被还原的物质是
(3)用双线桥法标出该反应的电子转移情况
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑该反应中氧化产物是_______ 。
(2)配平碱性条件下湿法制备高铁酸钾反应的离子方程式:_______ 。
_______Fe(OH)3+_______ClO-+_______=_______FeO +_______Cl-+_______
+_______Cl-+_______
(3)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。实验室制取Fe(OH)3胶体的化学方程式是:_______ 。
(4)证明有Fe(OH)3胶体生成的最简单实验操作是_______ 。
(5)取少量制得的Fe(OH)3胶体加入试管中,逐滴加入足量稀硫酸溶液,现象是_______ 。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑该反应中氧化产物是
(2)配平碱性条件下湿法制备高铁酸钾反应的离子方程式:
_______Fe(OH)3+_______ClO-+_______=_______FeO
 +_______Cl-+_______
+_______Cl-+_______(3)Fe(OH)3胶体可使水中悬浮物沉降下来,用作净水剂。实验室制取Fe(OH)3胶体的化学方程式是:
(4)证明有Fe(OH)3胶体生成的最简单实验操作是
(5)取少量制得的Fe(OH)3胶体加入试管中,逐滴加入足量稀硫酸溶液,现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】完成以下填空:
(1)写出下列反应的离子方程式
① Na溶于水_____________
② 过量CO2与NaOH溶液________________
③ 工业制漂白液____________
④ 浓盐酸与二氧化锰反应制取氯气__________
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,即“一硫二硝三炭”,其爆炸时的反应为: S+ 2KNO3 +3C = K2S + N2↑ + 3CO2↑,根据方程式,该反应中被还原的物质是___________ (填化学式)
(3)NaH可在野外作生氢剂,反应原理为NaH + H2O = NaOH + H2↑,H2O中氢元素____________ (填“被氧化”或“被还原”)。
(1)写出下列反应的离子方程式
① Na溶于水
② 过量CO2与NaOH溶液
③ 工业制漂白液
④ 浓盐酸与二氧化锰反应制取氯气
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,即“一硫二硝三炭”,其爆炸时的反应为: S+ 2KNO3 +3C = K2S + N2↑ + 3CO2↑,根据方程式,该反应中被还原的物质是
(3)NaH可在野外作生氢剂,反应原理为NaH + H2O = NaOH + H2↑,H2O中氢元素
您最近一年使用:0次
【推荐1】已知下列5个反应,试从氧化还原反应的角度,用序号回答下列问题。
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2 ③Cl2+H2O=HCl+HClO ④C+H2O CO+H2 ⑤2H2O
CO+H2 ⑤2H2O 2H2↑+O2↑
2H2↑+O2↑
(1)水只作氧化剂的是________ (填序号,(2),(3)同)。
(2)水只作还原剂的是________ 。
(3)水既作氧化剂,又作还原剂的是________ 。
(4)用双线桥法标出反应①电子转移的方向和数目________ 。
(5)反应③的离子方程式为________ 。
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2 ③Cl2+H2O=HCl+HClO ④C+H2O
 CO+H2 ⑤2H2O
CO+H2 ⑤2H2O 2H2↑+O2↑
2H2↑+O2↑(1)水只作氧化剂的是
(2)水只作还原剂的是
(3)水既作氧化剂,又作还原剂的是
(4)用双线桥法标出反应①电子转移的方向和数目
(5)反应③的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是2NaCl+2H2O 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)电解食盐水的过程中,氧化产物是____________________ ,用双线桥表示出电子转移的方向和数目________________ ,题干中反应改写成离子方程式是_____________ 。
(2)实验室用______________ 溶液(填化学式)处理多余的氯气,避免污染环境,写出化学方程式___________________________________________________ 。
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO42-、Ca2+、Mg2+等杂质离子。精制时依次加入BaCl2溶液、Na2CO3、NaOH,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式__________ 。
 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。(1)电解食盐水的过程中,氧化产物是
(2)实验室用
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO42-、Ca2+、Mg2+等杂质离子。精制时依次加入BaCl2溶液、Na2CO3、NaOH,充分反应后过滤,在滤液中加入盐酸中和至中性。盐酸与滤液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】电镀产生的废液中含有Cr2O72-,其中的Cr(VI)对环境和生物都有很大危害,将该废液进行如下处理,就可循环利用。

(1)在上述步骤中,需用还原剂的是_______ ,需用氧化剂的是_______ (填编号)。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是_____ (填化学式)。
(3)步骤⑤中的反应体系中共有五种物质Na2CrO4、NaCrO2、H2O2、H2O和X。X是____ (填化学式),写出反应的化学方程式__________________________________ ;
(4)若废液中Cr2O72-的浓度为540.0mg/L,处理上述废液20L,将Cr2O72-转化为Cr3+,至少需加入KI______ g。

(1)在上述步骤中,需用还原剂的是
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是
(3)步骤⑤中的反应体系中共有五种物质Na2CrO4、NaCrO2、H2O2、H2O和X。X是
(4)若废液中Cr2O72-的浓度为540.0mg/L,处理上述废液20L,将Cr2O72-转化为Cr3+,至少需加入KI
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】《天工开物》记载的炼锡方法基本上就是现代碳还原法,该反应的化学方程式为:SnO2 + 2C=Sn + 2CO ↑。反应中,作为氧化剂的物质是______ (填化学式),作为还原剂的物质是______ (填化学式)。在该反应中,若消耗了1mol SnO2,则生成______ mol Sn,转移电子的物质的量是______ mol。
您最近一年使用:0次
【推荐3】氧化剂过氧化氢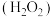 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。根据所学知识,回答下列问题:
在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。根据所学知识,回答下列问题:
(1)保存过氧化氢的试剂瓶上最适合贴上的一个标签是_______(填标号)。
(2)向滴加了淀粉溶液的 溶液中加入
溶液中加入 ,观察到的现象是
,观察到的现象是_______ 。
(3)油画中铅白(碱式碳酸铅)与空气中的硫化氢反应生成硫化氢,可 洗涤,发生反应为:
洗涤,发生反应为: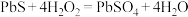 ,则处理
,则处理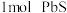 转移电子的物质的量是
转移电子的物质的量是_______ 。
(4)向橙红色 溶液中加入硫酸酸化,再加入足量
溶液中加入硫酸酸化,再加入足量 ,溶液变为蓝色
,溶液变为蓝色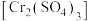 ,则上述反应中
,则上述反应中 作
作_______ 剂(填“氧化”或“还原”),铬元素化合价_______ (填“升高”“降低”或“不变”)。
(5)常温下,往 溶液中滴加少量
溶液中滴加少量 溶液,可发生如下两个反应:
溶液,可发生如下两个反应: ;
;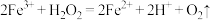 。下列说法正确的是_______(填标号)。
。下列说法正确的是_______(填标号)。
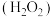 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。根据所学知识,回答下列问题:
在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。根据所学知识,回答下列问题:(1)保存过氧化氢的试剂瓶上最适合贴上的一个标签是_______(填标号)。
A. | B. | C. | D. |
 溶液中加入
溶液中加入 ,观察到的现象是
,观察到的现象是(3)油画中铅白(碱式碳酸铅)与空气中的硫化氢反应生成硫化氢,可
 洗涤,发生反应为:
洗涤,发生反应为: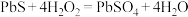 ,则处理
,则处理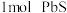 转移电子的物质的量是
转移电子的物质的量是(4)向橙红色
 溶液中加入硫酸酸化,再加入足量
溶液中加入硫酸酸化,再加入足量 ,溶液变为蓝色
,溶液变为蓝色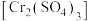 ,则上述反应中
,则上述反应中 作
作(5)常温下,往
 溶液中滴加少量
溶液中滴加少量 溶液,可发生如下两个反应:
溶液,可发生如下两个反应: ;
;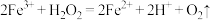 。下列说法正确的是_______(填标号)。
。下列说法正确的是_______(填标号)。A. 的氧化性一定比 的氧化性一定比 强 强 |
B.在 分解过程中,溶液的 分解过程中,溶液的 逐渐下降 逐渐下降 |
C.在 分解过程中,Fe2+和 分解过程中,Fe2+和 的总量保持不变 的总量保持不变 |
D. 生产过程要严格避免混入 生产过程要严格避免混入 |
您最近一年使用:0次

 溶液;③NaOH固体;④液态氯化氢;⑤冰醋酸;⑥石墨。上述状态下的物质中,能导电的有
溶液;③NaOH固体;④液态氯化氢;⑤冰醋酸;⑥石墨。上述状态下的物质中,能导电的有





