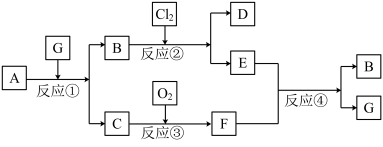
三氯化铁是合成草酸铁的重要原料。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:
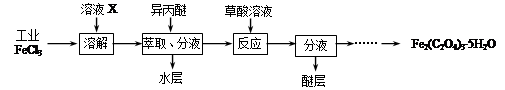
①为抑制FeCl3水解,溶液X为____________ 。
②上述流程中FeCl3能被异丙醚萃取,其原因是_________ ;检验萃取、分液后所得水层中是否含有Fe3+的方法是______________ 。
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是__________________ 。
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器________________ (填“甲”或“乙”)中。下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是________________ 。

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;__________ ;___________ ;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O;________________ ,得到无水FeCl3。
(1)利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:

①为抑制FeCl3水解,溶液X为
②上述流程中FeCl3能被异丙醚萃取,其原因是
③所得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是
④为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于如图所示仪器

a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
(2)某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)出发,制备单质铜和无水FeCl3,再由FeCl3合成Fe2(C2O4)3·5H2O。请补充完整由蚀刻废液制备单质铜和无水FeCl3的实验步骤(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液):向废液中加入足量铁粉,充分反应后过滤;
2014·江苏南通·二模 查看更多[4]
(已下线)2014届江苏省南通市高三第二次调研化学试卷2016届江苏省泰州中学高三上学期第二次质检化学试卷2017届江苏省南通市高三高考全真模拟(二)化学试卷福建省福州一中2019-2020学年高二下学期第一次月考化学试题
更新时间:2016-12-09 10:21:00
|
相似题推荐
解答题-无机推断题
|
困难
(0.15)
名校
解题方法
【推荐1】框图中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。
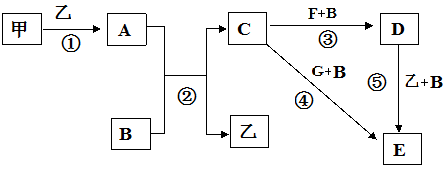
请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是______________ (填序号)。
(2)反应⑤的化学方程式为____________________________ 。
(3)甲与B反应的离子方程式_______________________________ 。
(4)在实验室将C溶液滴入F溶液中,观察到的现象是______________________ 。
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:__________________ 。
(6)已知:酚酞在c(OH-)为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和50g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去(假设过程中液体体积不变)。
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的,上述观点是否正确___________ 。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的,设计实验证明烧瓶内溶液中含H2O2,简述实验方法_____________________ 。

请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是
(2)反应⑤的化学方程式为
(3)甲与B反应的离子方程式
(4)在实验室将C溶液滴入F溶液中,观察到的现象是
(5)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:
(6)已知:酚酞在c(OH-)为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和50g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去(假设过程中液体体积不变)。
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的,上述观点是否正确
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的,设计实验证明烧瓶内溶液中含H2O2,简述实验方法
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐1】硫脲 [CS(NH2)2]在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。
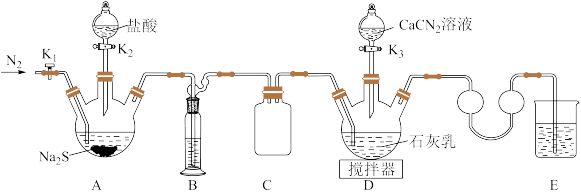
已知: 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。
回答下列问题:
(1)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整_______ 。
(2)检查气密性后加入药品,打开K₂。装置B中盛装的试剂为_______ 。反应结束后关闭K₂,打开K₁通 一段时间,目的是
一段时间,目的是_______ 。
(3)撤走搅拌器,打开K₃,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500 mL溶液。在锥形瓶中加入足量氢氧化钠溶液和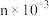 mol单质碘,发生反应:
mol单质碘,发生反应: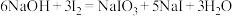 ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: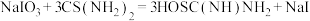 ;
;
②充分反应后加稀硫酸至酸性,发生反应: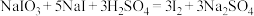
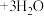 ,滴加两滴淀粉溶液,用c mol·L⁻¹
,滴加两滴淀粉溶液,用c mol·L⁻¹  标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。
粗产品中硫脲的质量分数为_______ (用含“m、n、c、V”的式子表示);若滴定时加入的稀硫酸量不足,会导致所测硫脲的质量分数_______ (填“偏高”、“偏低”或“不变”)已知:
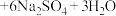 。
。
 ,再与
,再与 合成
合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。
已知:
 易溶于水,易被氧化,受热时部分发生异构化生成
易溶于水,易被氧化,受热时部分发生异构化生成 。
。回答下列问题:
(1)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整
(2)检查气密性后加入药品,打开K₂。装置B中盛装的试剂为
 一段时间,目的是
一段时间,目的是(3)撤走搅拌器,打开K₃,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。
①称取m g产品,加水溶解配成500 mL溶液。在锥形瓶中加入足量氢氧化钠溶液和
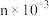 mol单质碘,发生反应:
mol单质碘,发生反应: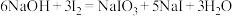 ,量取25mL硫脲溶液加入锥形瓶,发生反应:
,量取25mL硫脲溶液加入锥形瓶,发生反应: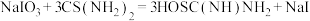 ;
;②充分反应后加稀硫酸至酸性,发生反应:
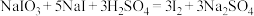
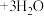 ,滴加两滴淀粉溶液,用c mol·L⁻¹
,滴加两滴淀粉溶液,用c mol·L⁻¹  标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。至终点时消耗标准溶液V mL。
。至终点时消耗标准溶液V mL。粗产品中硫脲的质量分数为

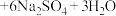 。
。
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
解题方法
【推荐2】铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、A12O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如图所示。
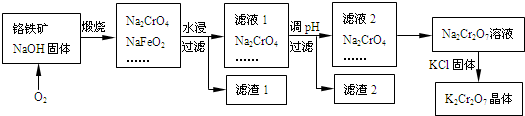
已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O 2CrO42-+2H+。
2CrO42-+2H+。
请回答:
(1)K2Cr2O7中K元素的原子结构示意图为____________ ,化合价是_______________ 。
(2)往铬铁矿里通入氧气的主要目的是__________________ 。滤液1的成分除Na2CrO4外,还含有_____ (填化学式)。
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式
是________________________ 。
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是____________________ 。
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、__________ 、过滤、洗涤、干燥。
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是_______________________ 。

已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O
 2CrO42-+2H+。
2CrO42-+2H+。请回答:
(1)K2Cr2O7中K元素的原子结构示意图为
(2)往铬铁矿里通入氧气的主要目的是
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式
是
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
【推荐3】高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程:
(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列_____ 物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是________ ;操作Ⅱ是根据KMnO4和K2CO3两物质在__________ (填性质)上差异,采用 __________ (填操作步骤)、趁热过滤得到KMnO4粗晶体的。
(3)上述流程中可以循环使用的物质有石灰、CO2、____ 和____ (写化学式)。
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是_______ 。
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:__________________ 。
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:________________ 。
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得_____ mol KMnO4。

(1) KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列
A.75%酒精 B.双氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名称是
(3)上述流程中可以循环使用的物质有石灰、CO2、
(4) 向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是
(5) 铋酸钠(NaBiO3,不溶于水)用于定性检验酸性溶液中Mn2+的存在(铋元素的还原产物为Bi3+,Mn的氧化产物为+7价),写出反应的离子方程式:
(6) 写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(7)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
您最近一年使用:0次