向2.0L恒容密闭容器中充入1.0mol PCl5,在温度为T时发生如下反应PCl5(g)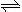 PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:

回答下列问题:
(1)反应在前50s的平均速率v(PCl5)=__________ ,该反应的△S___ 0(填“<”、“>”或“=”).
(2)温度为T时,该反应的化学平衡常数=_____________ 。
(3)上述反应到达平衡状态时,PCl3的体积分数为________ 。
要提高平衡时PCl3的体积分数,可采取的措施有_____________ 。
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=___________ 。
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是____________________ 。
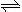 PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+ Cl2(g)△H=" +124" kJ•mol-1。反应过程中测定的部分数据见下表:
回答下列问题:
(1)反应在前50s的平均速率v(PCl5)=
(2)温度为T时,该反应的化学平衡常数=
(3)上述反应到达平衡状态时,PCl3的体积分数为
要提高平衡时PCl3的体积分数,可采取的措施有
| A.温度不变,压缩容器体积增大压强 | B.使用高效催化剂 |
| C.温度和体积不变,减小PCl5的起始量 | D.体积不变,提高反应温度 |
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是
更新时间:2016/12/09 02:23:11
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g) 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
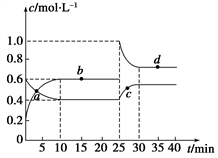
(1)该温度下,该反应的平衡常数为______________ 。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是________ 点。从起点开始首次达到平衡时,以NO2表示的反应速率为____________ 。
(3)25 min时,加入了__________ (填加入物质的化学式及加入的物质的量),使平衡发生了移动。
(4)d点对应NO2的物质的量浓度________ (填“大于”、“小于”或“等于”)0.8 mol·L-1,理由是____________________________________________________ 。
 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
(1)该温度下,该反应的平衡常数为
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是
(3)25 min时,加入了
(4)d点对应NO2的物质的量浓度
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】以生物质为原料制备氢气可以有效减少环境污染,同时能降低对化石燃料的依赖。乙酸是生物油的主要成分之一,常被用作模型化合物。已知:乙酸水蒸气重整制氢过程中可能发生的反应如下:
i.CH3COOH(g)+2H2O(g) 2CO2(g)+4H2(g) △H;
2CO2(g)+4H2(g) △H;
ii.CH3COOH(g) 2CO(g)+2H2(g) △H1=+213.7kJ•mol-l;
2CO(g)+2H2(g) △H1=+213.7kJ•mol-l;
iii.CH3COOH(g) CH4(g)+CO2(g) △H2=-33.5kJ•mol-1;
CH4(g)+CO2(g) △H2=-33.5kJ•mol-1;
iv.CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.1kJ•mol-1。
CO2(g)+H2(g) △H3=-41.1kJ•mol-1。
一定温度和催化剂条件下,向5L密闭容器中充入2molCH3COOH(g)和4molH2O(g),只发生反应i,10min后反应达到化学平衡状态,此时容器内的压强变为初始时的1.5倍。从反应开始到平衡状态,用H2的浓度变化表示的平均反应速率v(H2)=____ 。
i.CH3COOH(g)+2H2O(g)
 2CO2(g)+4H2(g) △H;
2CO2(g)+4H2(g) △H;ii.CH3COOH(g)
 2CO(g)+2H2(g) △H1=+213.7kJ•mol-l;
2CO(g)+2H2(g) △H1=+213.7kJ•mol-l;iii.CH3COOH(g)
 CH4(g)+CO2(g) △H2=-33.5kJ•mol-1;
CH4(g)+CO2(g) △H2=-33.5kJ•mol-1;iv.CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.1kJ•mol-1。
CO2(g)+H2(g) △H3=-41.1kJ•mol-1。一定温度和催化剂条件下,向5L密闭容器中充入2molCH3COOH(g)和4molH2O(g),只发生反应i,10min后反应达到化学平衡状态,此时容器内的压强变为初始时的1.5倍。从反应开始到平衡状态,用H2的浓度变化表示的平均反应速率v(H2)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)某温度时,在2 L容器中,X、Y、Z三种物质的物质的量随时间变化曲线如图所示。由图中数据分析,该反应的化学方程式为:_______________ .
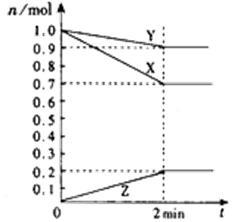
(2)反应开始至2 min,Z的平均反应速率为____________ 。
(3)不同时间测得以下反应速率:
①v(X)=0.075 mol· L-1·min-1
②v(Y)=0.001 mol· L-1·s-1
③v(Z)=0.06 mol·L-1·min-1
速率由大到小关系正确为______ 。
A.①>③>② B.③>①>② C.②>③>①

(2)反应开始至2 min,Z的平均反应速率为
(3)不同时间测得以下反应速率:
①v(X)=0.075 mol· L-1·min-1
②v(Y)=0.001 mol· L-1·s-1
③v(Z)=0.06 mol·L-1·min-1
速率由大到小关系正确为
A.①>③>② B.③>①>② C.②>③>①
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是:B(g) A(g)+H2(g) ΔH=+125kJ·mol—1
A(g)+H2(g) ΔH=+125kJ·mol—1
(1)该反应的平衡常数表达式为K=______________ 。随着温度的升高,K 值____________ (填“增大”、“减小”或“不变”)。
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应)。物质B的平衡转化率与水蒸气的用量、体系总压强关系如下图。
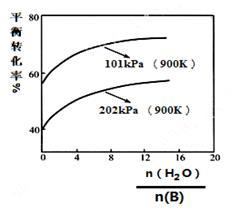
①由上图可得出:
结论一:
其他条件不变,水蒸气的用量越大,平衡转化率越___ ;
结论二:______________________________________
②加入稀释剂能影响反应物B的平衡转化率的原因是:__________________ 。
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高B的平衡转化率。试解释其原因:________________________ 。
 A(g)+H2(g) ΔH=+125kJ·mol—1
A(g)+H2(g) ΔH=+125kJ·mol—1(1)该反应的平衡常数表达式为K=
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应)。物质B的平衡转化率与水蒸气的用量、体系总压强关系如下图。

①由上图可得出:
结论一:
其他条件不变,水蒸气的用量越大,平衡转化率越
结论二:
②加入稀释剂能影响反应物B的平衡转化率的原因是:
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高B的平衡转化率。试解释其原因:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z和W,它们的物质的量随时间的变化如下表所示。
(1)体系中发生反应的化学方程式是____________ ;
(2)列式计算该反应在0~3 min时间内产物W的平均反应速率:________________ ;
(3)该反应达到平衡时反应物Y的转化率α等于_________________________ ;
(4)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应改变的实验条件分别是:
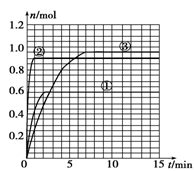
①________ ;②________ ;③________ 。
| t/min | X/mol | Y/mol | Z/mol | W/mol |
| 0 | 2.00 | 1.00 | 0.00 | 0.00 |
| 1 | 1.80 | 0.80 | 0.20 | 0.10 |
| 3 | 1.50 | 0.50 | 0.50 | 0.25 |
| 5 | 1.30 | 0.30 | 0.70 | 0.35 |
| 9 | 1.10 | 0.10 | 0.90 | 0.45 |
| 10 | 1.10 | 0.10 | 0.90 | 0.45 |
| 14 | 1.10 | 0.10 | 0.90 | 0.45 |
(2)列式计算该反应在0~3 min时间内产物W的平均反应速率:
(3)该反应达到平衡时反应物Y的转化率α等于
(4)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应改变的实验条件分别是:

①
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】综合治理空气污染是环境化学当前主要研究的内容。
(1)汽车尾气中的 NO(g)和CO(g)在一定温度和催化剂条件下可转化为 N2(g)和 CO2(g)得到净化。
①已知2NO(g)+2CO(g) N2(g)+2CO2(g) 反应能自发进行,则该为
N2(g)+2CO2(g) 反应能自发进行,则该为__________ 反应(填“吸热”或“放热”)。
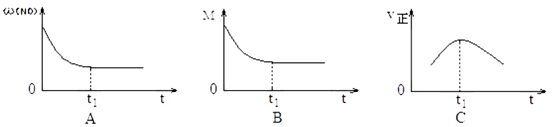
②上述反应在绝热、恒容密闭容器中进行,并在 t1时可达到平衡(图中 ω、M、v正分别表示质量分数混合气体平均相对分子质量和正反应速率),则下列示意图中符合题意的是__________ (填选项序号)。
(2)在25℃、101kPa下,将2molNO、2.4molCO通入固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示。
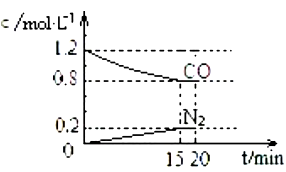
③NO的转化率为__________ ,0~15min 内,v(NO) =__________ 。
④20min 时若改变反应条件,导致CO浓度下降,则改变的条件可能是__________ (填选项序号)。
a.升高温度 b.增加CO的量 c.降低温度 d.扩大容气体积
⑤如图所示,无摩擦、无质量的活塞 1、2 将反应器隔成甲、乙两部分,在 25℃、101kPa 下实现平衡时,各部分体积分别为 V甲、V乙。此时若去掉活塞1,不引起活塞2的移动,则X =__________ , V甲:V乙=__________ 。
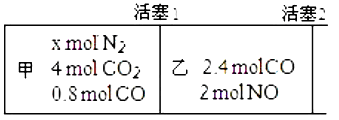
(1)汽车尾气中的 NO(g)和CO(g)在一定温度和催化剂条件下可转化为 N2(g)和 CO2(g)得到净化。
①已知2NO(g)+2CO(g)
 N2(g)+2CO2(g) 反应能自发进行,则该为
N2(g)+2CO2(g) 反应能自发进行,则该为②上述反应在绝热、恒容密闭容器中进行,并在 t1时可达到平衡(图中 ω、M、v正分别表示质量分数混合气体平均相对分子质量和正反应速率),则下列示意图中符合题意的是

(2)在25℃、101kPa下,将2molNO、2.4molCO通入固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示。

③NO的转化率为
④20min 时若改变反应条件,导致CO浓度下降,则改变的条件可能是
a.升高温度 b.增加CO的量 c.降低温度 d.扩大容气体积
⑤如图所示,无摩擦、无质量的活塞 1、2 将反应器隔成甲、乙两部分,在 25℃、101kPa 下实现平衡时,各部分体积分别为 V甲、V乙。此时若去掉活塞1,不引起活塞2的移动,则X =
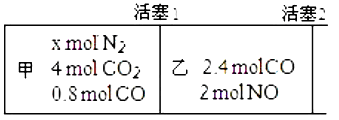
您最近一年使用:0次



