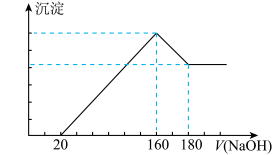
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为____________________ ;沉淀中Al(OH)3的质量为____________ g。
(2)合金中Mg的质量为___________ ;所用HCl的物质的量浓度为___________ mol/L。

求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为
(2)合金中Mg的质量为
更新时间:2016-12-09 10:43:29
|
相似题推荐
填空题
|
困难
(0.15)
【推荐1】111
Ⅰ.已知向含有淀粉的10mL 0.2mol/L KIO3酸性溶液滴加0.3mol/LNaHSO3溶液的过程中,溶液的颜色先变蓝色,然后褪色,发生的离子反应如下:
①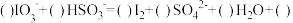 ;
;
②I2+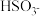 +H2O=2I-+SO
+H2O=2I-+SO +3H+
+3H+
回答下列问题:
(1)写出①反应的离子反应方程式____________________ .
(2)根据①②反应写出还原性粒子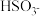 ,I2,I-由强到弱的顺序
,I2,I-由强到弱的顺序____________ .
(3)溶液刚好褪色时,则消耗的NaHSO3溶液的体积为__________________ .
(4)预测已知向含有淀粉的NaHSO3溶液滴加KIO3溶液的现象_________________ .
Ⅱ.在密闭容器中,将碳酸氢钠和过氧化钠的混合粉未加热至250℃,使其充分反应最后测得残余固体中两种化合物的组成分别为amol和bmol,且a>b,试回答下列问题
(5)反应后中固体的成分及其物质的量是:_______________
(6)原混合物中碳酸氢钠和过氧化钠的物质的量分别为:_______________
(7)反应后容器气态物质成分及其物质的量是:_______________
Ⅰ.已知向含有淀粉的10mL 0.2mol/L KIO3酸性溶液滴加0.3mol/LNaHSO3溶液的过程中,溶液的颜色先变蓝色,然后褪色,发生的离子反应如下:
①
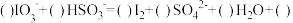 ;
;②I2+
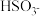 +H2O=2I-+SO
+H2O=2I-+SO +3H+
+3H+回答下列问题:
(1)写出①反应的离子反应方程式
(2)根据①②反应写出还原性粒子
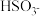 ,I2,I-由强到弱的顺序
,I2,I-由强到弱的顺序(3)溶液刚好褪色时,则消耗的NaHSO3溶液的体积为
(4)预测已知向含有淀粉的NaHSO3溶液滴加KIO3溶液的现象
Ⅱ.在密闭容器中,将碳酸氢钠和过氧化钠的混合粉未加热至250℃,使其充分反应最后测得残余固体中两种化合物的组成分别为amol和bmol,且a>b,试回答下列问题
(5)反应后中固体的成分及其物质的量是:
(6)原混合物中碳酸氢钠和过氧化钠的物质的量分别为:
(7)反应后容器气态物质成分及其物质的量是:
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】化学计量在化学中占有重要地位,请回答下列问题:
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g。
①两种气体总的物质的量为 。② C与O原子个数比为 。
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
①下列的相关说法正确的是 (填序号)。
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
② 盐酸的物质的量浓度 ,合金中镁的质量分数 。
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g。
①两种气体总的物质的量为 。② C与O原子个数比为 。
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 8.8 | 17.6 | 22.0 |
| 气体体积/L | 2.24 | 4.48 | 4.48 |
①下列的相关说法正确的是 (填序号)。
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
② 盐酸的物质的量浓度 ,合金中镁的质量分数 。
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
【推荐1】某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程_____________ 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因___________ 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是_________ 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是____________ 。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是___________ 。
③乙同学这样配制混合溶液的理由是___________ 。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4 mL 2 mol·L-1HCl 溶液 | 沉淀溶解 |
| Ⅱ | 4 mL 2 mol·L-1NH4Cl 溶液 | 沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是
③乙同学这样配制混合溶液的理由是
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐1】计算
(1)将200mL3mol/L的Al2(SO4)3溶液稀释至500mL,求稀释后硫酸根的浓度为多少______ ?
(2)将K2SO4和Al2(SO4)3和KAl(SO4)2三种混合溶液加H2SO4酸化。测得c(SO )=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO
)=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO ),则c(K+)为多少
),则c(K+)为多少 ______ ?
(3)Fe、Al混合物共0.2mol,用盐酸将其完全溶解,放出标准状况下5.6L气体,然后再滴入4mol/L的NaOH溶液,请计算:
①求该混合物中Fe、Al的物质的量______ ?
②若该Fe、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Fe2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为多少______ mL?
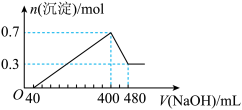
(4)将一定质量的Mg和Al混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示计算:
①酸的物质的量浓度为多少______ ?
②若将上述混合物中等物质的量的Mg和Al分别与稀硫酸充分反应,产生的气体通入相同条件下恒容的甲乙两密闭容器中,求甲乙两容器内的压强比为多少______ ?
(1)将200mL3mol/L的Al2(SO4)3溶液稀释至500mL,求稀释后硫酸根的浓度为多少
(2)将K2SO4和Al2(SO4)3和KAl(SO4)2三种混合溶液加H2SO4酸化。测得c(SO
 )=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO
)=1.05 mol/L, c(Al3+)=0.55 mol/L,c(H+)=0.10mol/L(假设H2SO4完全电离为H+和SO ),则c(K+)为多少
),则c(K+)为多少 (3)Fe、Al混合物共0.2mol,用盐酸将其完全溶解,放出标准状况下5.6L气体,然后再滴入4mol/L的NaOH溶液,请计算:
①求该混合物中Fe、Al的物质的量
②若该Fe、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Fe2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积为多少
(4)将一定质量的Mg和Al混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示计算:

①酸的物质的量浓度为多少
②若将上述混合物中等物质的量的Mg和Al分别与稀硫酸充分反应,产生的气体通入相同条件下恒容的甲乙两密闭容器中,求甲乙两容器内的压强比为多少
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到-3价。某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

(1)请写出该合金中铁与硝酸反应的离子方程式_______________ 。
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_______________ 。
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为___________ 。
(4)B与A的差值为__________ mol。
(5)B点对应的沉淀的物质的量为_______ mol,C点对应的氢氧化钠溶液的体积为______ mL。

(1)请写出该合金中铁与硝酸反应的离子方程式
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为
(4)B与A的差值为
(5)B点对应的沉淀的物质的量为
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐3】准确称取6.00克铝土矿样品(含Al2O3、Fe2O3、SiO2),将其放入盛有100毫升H2SO4溶液的烧杯中,充分反应后滤出沉淀物。在滤液X中加入10摩/升的NaOH溶液,产生的沉淀的质量w与所加NaOH溶液的体积V之间有如图所示的关系。求:
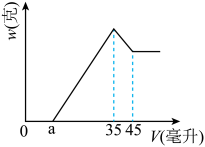
(1)分析图象可知滤液X中所含有的溶质成分为_____ (填化学式)。
(2)H2SO4溶液的物质的量浓度是__________ ?
(3)图中a值为2.3毫升时,铝土矿样品中Fe2O3的质量分数_________________ 。
(4)a值的变化范围是____________________ ?

(1)分析图象可知滤液X中所含有的溶质成分为
(2)H2SO4溶液的物质的量浓度是
(3)图中a值为2.3毫升时,铝土矿样品中Fe2O3的质量分数
(4)a值的变化范围是
您最近一年使用:0次

 、
、 均转化为沉淀,将反应器内水分蒸干,最后得到白色固体物质共29g,则原混和物中Na2CO3的质量是
均转化为沉淀,将反应器内水分蒸干,最后得到白色固体物质共29g,则原混和物中Na2CO3的质量是

