某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程_____________ 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因___________ 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是_________ 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是____________ 。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是___________ 。
③乙同学这样配制混合溶液的理由是___________ 。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4 mL 2 mol·L-1HCl 溶液 | 沉淀溶解 |
| Ⅱ | 4 mL 2 mol·L-1NH4Cl 溶液 | 沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是
③乙同学这样配制混合溶液的理由是
更新时间:2016-12-08 21:10:51
|
相似题推荐
填空题
|
困难
(0.15)
解题方法
【推荐1】将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)
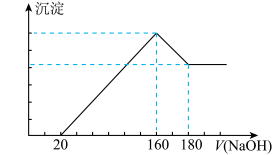
求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为____________________ ;沉淀中Al(OH)3的质量为____________ g。
(2)合金中Mg的质量为___________ ;所用HCl的物质的量浓度为___________ mol/L。

求:
(1)加入NaOH溶液0~20mL过程中反应的离子方程式为
(2)合金中Mg的质量为
您最近半年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐1】完成下列问题
(1)一定温度下,Ksp[Mg3(PO4)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。向浓度均为0.20mol/L的MgCl2和CaCl2混合溶液中逐滴加入Na3P04,先生成___________ 沉淀(填化学式);当测得溶液其中一种金属阳离子沉淀完全(浓度小于10-5mol/L)时,溶液中的另一种金属阳离子的物质的量浓度c=____________ mol/L。
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
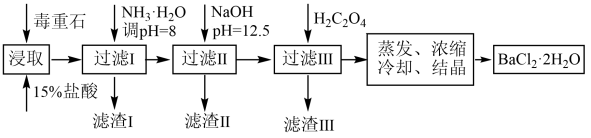
①毒重石用盐酸浸取前需充分研磨,目的是_____________________ 。
②加入NH3·H2O调节PH=8可除去_____________ (填离子符号),滤渣II中含____________ (填化学式)。加入H2C2O4时应避免过量,原因是_________________ 。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中加入400mL0.01mol/LNa2SO4溶液,下列叙述正确的是

(1)一定温度下,Ksp[Mg3(PO4)2]=6.0×10-29,Ksp[Ca3(PO4)2]=6.0×10-26。向浓度均为0.20mol/L的MgCl2和CaCl2混合溶液中逐滴加入Na3P04,先生成
(2)毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:

①毒重石用盐酸浸取前需充分研磨,目的是
②加入NH3·H2O调节PH=8可除去
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.7 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)已知25℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100mL该条件下的CaSO4饱和溶液中加入400mL0.01mol/LNa2SO4溶液,下列叙述正确的是

| A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大 |
| B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小 |
| C.溶液中析出CaSO4固体沉淀.溶液中c(Ca2+)、c(SO42-)都变小 |
| D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大 |
您最近半年使用:0次
填空题
|
困难
(0.15)
名校
【推荐2】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:______________ ;农业上用石膏降低其碱性的反应原理:__________ 。
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________ (填“>”“<”或“=”)n。
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=__________ 。
(4)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),则溶液显
)=c(Cl-),则溶液显________ (填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=________ 。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:盐碱地产生碱性的原因:
(2)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
(3)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(4)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显
您最近半年使用:0次
填空题
|
困难
(0.15)
【推荐3】现有0.175 mol·L-1醋酸钠溶液500 mL,(已知室温下,醋酸的电离平衡常数Ka=1.75×10-5)。
(1)写出醋酸钠水解反应的化学方程式 ______________________________ ;
(2)下列图象能说明醋酸钠的水解反应达到平衡的是____________ ;

A. 溶液中c(Na+)与反应时间t的关系
B.CH3COO-的水解速率与反应时间t的关系
C.溶液的pH与反应时间t的关系
D.KW与反应时间t的关系
(3)向醋酸钠溶液中加入少量下列物质,水解平衡向正向移动的有______;
(4)在醋酸钠溶液中加入冰醋酸,溶液中微粒浓度的关系式能成立的有__________;
(5)欲配制0.175 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案:
方案一:用托盘天平称取___________ g无水醋酸钠,溶于适量水中,配成500 mL溶液。[已知:M(CH3COONa) = 82g/mol ]
方案二:用体积均为250 mL且浓度均为___________ mol·L-1的醋酸与氢氧化钠两溶液混合而成(设混合后的体积等于混合前两者体积之和)。
(6)在室温下,0.175 mol·L-1醋酸钠(CH3COONa)溶液的pH约为________ 。
(1)写出醋酸钠水解反应的
(2)下列图象能说明醋酸钠的水解反应达到平衡的是

A. 溶液中c(Na+)与反应时间t的关系
B.CH3COO-的水解速率与反应时间t的关系
C.溶液的pH与反应时间t的关系
D.KW与反应时间t的关系
(3)向醋酸钠溶液中加入少量下列物质,水解平衡向正向移动的有______;
| A.冰醋酸 | B.纯碱固体 | C.醋酸钠固体 | D.氯化铵固体 |
| A.c(CH3COO-) + c(CH3COOH)>c(Na+) |
| B.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.c(CH3COO-)>c(H+)>c(OH-)>c(Na+) |
方案一:用托盘天平称取
方案二:用体积均为250 mL且浓度均为
(6)在室温下,0.175 mol·L-1醋酸钠(CH3COONa)溶液的pH约为
您最近半年使用:0次



