下列四个装置图均与电化学有关,请根据图示回答相关问题:

(1)这四个装置中,利用电解原理的是__________ (填装置序号);
(2)装置①若用来精炼铜,则a极的电极材料是_______ (填“粗铜”或“精铜”),电解质溶液为_______ ;
(3)装置②的总反应方程式是_________________________ ;
(4)装置③中钢闸门应与外接电源的_________ 极相连(填“正”或“负”)
(5)装置④中的铁钉几乎没被腐蚀,其原因是_________ 。

(1)这四个装置中,利用电解原理的是
(2)装置①若用来精炼铜,则a极的电极材料是
(3)装置②的总反应方程式是
(4)装置③中钢闸门应与外接电源的
(5)装置④中的铁钉几乎没被腐蚀,其原因是
更新时间:2016-12-09 10:54:51
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】利用实验室常用的物品,根据电化学原理,可以设计原电池。请填写下列空白:
(1)实验原理:Fe+2H+=_____________ 。
(2)实验用品:电极( ) (填所用电极的名称)、稀硫酸、烧杯、导线、耳机(或电流计)。
(3)实验装置如图所示。

(4)原电池工作原理分析:
该原电池工作时,负极为_________ (填化学式),发生_________ (填“氧化”或“还原”),其电极反应式为______________ ,另一电极为正极,发生_________ 反应,其电极反应式为_______________ ,外电路中电子流动方向为_______________ 。
(1)实验原理:Fe+2H+=
(2)实验用品:电极
(3)实验装置如图所示。

(4)原电池工作原理分析:
该原电池工作时,负极为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电化学技术是有效解决CO、SO2、NOx等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下:

(1)电解质溶液中H+向___________ (填“A极”或“B极”)移动。
(2)请写出负极电极反应式___________ 。
(3)用该原电池做电源,石墨做电极电解2 L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L气体(标况)。
①上述过程中转移的电子数为___________ mol。
②假设电解前后溶液体积不变,则电解后溶液中H+的浓度为___________ mol·L-1,析出Ag的质量为___________ g。

(1)电解质溶液中H+向
(2)请写出负极电极反应式
(3)用该原电池做电源,石墨做电极电解2 L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24L气体(标况)。
①上述过程中转移的电子数为
②假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:

(1)打开K2,闭合K1,若所盛溶液为 溶液,则A为
溶液,则A为___________ 极,B极的电极反应式为___________ ;
(2)打开K1,闭合K2,若所盛溶液为滴有酚酞的 溶液,
溶液,
①A电极附近可观察到的现象是___________ ,电极反应式为___________ 。
②反应一段时间后打开K2,B极产生气体的体积(标准状况)为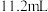 ,将溶液充分振荡混匀,如果忽略溶液的体积变化和气体的溶解等,则该溶液中
,将溶液充分振荡混匀,如果忽略溶液的体积变化和气体的溶解等,则该溶液中 的浓度为
的浓度为___________  。
。
(3)如要用电解方法精炼粗铜,打开K1,闭合K2,电解液选用 溶液,则A电极的材料应换成是
溶液,则A电极的材料应换成是___________ ,B极的电极反应式为___________ ;反应一段时间后电解质溶液中 浓度
浓度___________ (填“增大”、“减小”、“不变”)。

(1)打开K2,闭合K1,若所盛溶液为
 溶液,则A为
溶液,则A为(2)打开K1,闭合K2,若所盛溶液为滴有酚酞的
 溶液,
溶液,①A电极附近可观察到的现象是
②反应一段时间后打开K2,B极产生气体的体积(标准状况)为
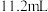 ,将溶液充分振荡混匀,如果忽略溶液的体积变化和气体的溶解等,则该溶液中
,将溶液充分振荡混匀,如果忽略溶液的体积变化和气体的溶解等,则该溶液中 的浓度为
的浓度为 。
。(3)如要用电解方法精炼粗铜,打开K1,闭合K2,电解液选用
 溶液,则A电极的材料应换成是
溶液,则A电极的材料应换成是 浓度
浓度
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】如图所示装置为在直流电的作用下电解CuSO4 溶液图,其中A、B为石墨电极,
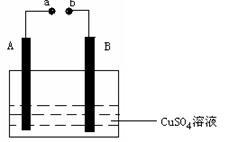
a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则:
(1)a为电源的_______ 极。b为电源的_______ 极
(2)写出电极反应方程式:A_______ ,B_______ 。
(3)A电极析出气体体积为_______ L(在标准状况下)。

a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则:
(1)a为电源的
(2)写出电极反应方程式:A
(3)A电极析出气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“霾”是当今世界环境热点话题。目前宁夏境内空气质量恶化原因之一是机动车尾气和燃煤产生的烟气。NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
2NO(g)+ 2CO(g) 2CO2(g)+ N2(g) △H=﹣a kJ•mol-1(a > 0)
2CO2(g)+ N2(g) △H=﹣a kJ•mol-1(a > 0)
(1)在一定温度下,将2.0mol NO、2.4mol CO气体通入到固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:

①0~15min N2的平均速率v(N2)=______ ;NO的转化率为_______ 。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是______ (选填序号)。
a.缩小容器体积 b.增加CO的量 c.降低温度 d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将______ 移动(选填“向左”、“向右”或“不”),重新达到平衡后,该反应的化学平衡常数为_______ 。
(2)已知:2NO(g)+ O2(g)= 2NO2(g) △H=﹣b kJ•mol-1(b > 0)
CO的燃烧热△H=﹣c kJ•mol-1 (c > 0)
则在消除汽车尾气中NO2的污染时,NO2与CO发生反应的热化学反应方程式为:____________________________________________ 。
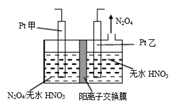
(3)工业废气中含有的NO2还可用电解法消除。制备方法之一是先将NO2转化为N2O4, 然后采用电解法制备 N2O5,装置如图所示。 Pt乙为________ 极,电解池中生成N2O5的电极反应式是____________ 。
2NO(g)+ 2CO(g)
 2CO2(g)+ N2(g) △H=﹣a kJ•mol-1(a > 0)
2CO2(g)+ N2(g) △H=﹣a kJ•mol-1(a > 0)(1)在一定温度下,将2.0mol NO、2.4mol CO气体通入到固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:

①0~15min N2的平均速率v(N2)=
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是
a.缩小容器体积 b.增加CO的量 c.降低温度 d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将

(2)已知:2NO(g)+ O2(g)= 2NO2(g) △H=﹣b kJ•mol-1(b > 0)
CO的燃烧热△H=﹣c kJ•mol-1 (c > 0)
则在消除汽车尾气中NO2的污染时,NO2与CO发生反应的热化学反应方程式为:
(3)工业废气中含有的NO2还可用电解法消除。制备方法之一是先将NO2转化为N2O4, 然后采用电解法制备 N2O5,装置如图所示。 Pt乙为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氯碱工业是以电解饱和食盐水为基础的基本化学工业。如图是某氯碱工业生产原理示意图:
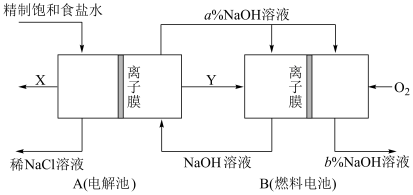
(1)装置A所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2和Ca2,要加入的试剂分别为_____ 、_____ (写化学式)。
(2)氯碱工业是高耗能产业,按图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是_____ (填化学式);X与稀NaOH溶液反应的离子方程式为______ 。
②比较图示中氢氧化钠的质量分数a%与b%的大小:a_____ b(填“>”“<”或“=”)。
③若用装置B作为装置A的辅助电源,每当消耗标准状况下氧气的体积为11.2L时,则装置B可向装置A提供的电量约为______ (一个e-的电量为1.6010-19C;计算结果精确到0.01)。

(1)装置A所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2和Ca2,要加入的试剂分别为
(2)氯碱工业是高耗能产业,按图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是
②比较图示中氢氧化钠的质量分数a%与b%的大小:a
③若用装置B作为装置A的辅助电源,每当消耗标准状况下氧气的体积为11.2L时,则装置B可向装置A提供的电量约为
您最近一年使用:0次
【推荐1】铁及其化合物用途非常广泛。
(1)已知赤铁矿还原冶炼时是逐级进行的,已知:
(a) 3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g)
2Fe3O4(s)+CO2(g)  H = a kJ·mol-1
H = a kJ·mol-1
(b) Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)  H =b kJ·mol-1
H =b kJ·mol-1
(c) Fe3O4(s)+CO(g) 3FeO(s)+CO2 (g)
3FeO(s)+CO2 (g)  H = c kJ·mol-1
H = c kJ·mol-1
①上述反应(a)平衡常数表达式为K=___________________ 。
②反应FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)  H =
H =__________ kJ·mol-1(用含a、b、c的代数式表示)。
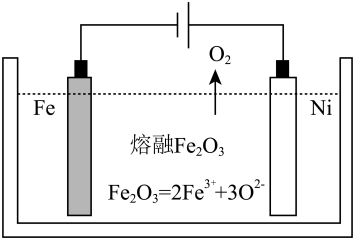
(2)用类似冶炼铝的方法, 在600~1000℃时电解熔融的Fe2O3冶炼铁(装置示意图如图),该法除消耗能量较少外,另一最突出的优点是__________________________________ ;电解时阳极发生的电极反应为____________ 。
(3)生铁在自然界中可发生析氢腐蚀和吸氧腐蚀,析氢腐蚀的负极的电极反应式为_________ ;如图所示,纯铁处于a、b、c三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填字母)_____________ 。

(1)已知赤铁矿还原冶炼时是逐级进行的,已知:
(a) 3Fe2O3(s)+CO(g)
 2Fe3O4(s)+CO2(g)
2Fe3O4(s)+CO2(g)  H = a kJ·mol-1
H = a kJ·mol-1(b) Fe2O3(s)+3CO(g)
 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)  H =b kJ·mol-1
H =b kJ·mol-1(c) Fe3O4(s)+CO(g)
 3FeO(s)+CO2 (g)
3FeO(s)+CO2 (g)  H = c kJ·mol-1
H = c kJ·mol-1①上述反应(a)平衡常数表达式为K=
②反应FeO(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)  H =
H =(2)用类似冶炼铝的方法, 在600~1000℃时电解熔融的Fe2O3冶炼铁(装置示意图如图),该法除消耗能量较少外,另一最突出的优点是

(3)生铁在自然界中可发生析氢腐蚀和吸氧腐蚀,析氢腐蚀的负极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题
(1)下图为探究金属 是否腐蚀的示意图
是否腐蚀的示意图
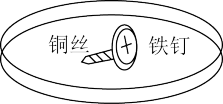
在培养皿中加入一定量的琼脂和饱和 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ (填“左”或“右”)端,结合化学用语解释变红的原因:___________ 。
(2)碳钢在空气中容易被腐蚀,加入钼酸盐有利于缓蚀,其缓蚀原理是在钢铁表面形成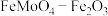 保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入
保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入 ,则
,则 的作用是
的作用是___________ 。
(3)支撑海港码头基础的钢管桩,常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。

①该保护方法叫作___________ (填“牺牲阳极法”或“外加电流法”)。
②下列有关表述正确的是___________ (填字母)。
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(4)利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:

铁电极的电极反应为___________ 。
下列叙述正确的是___________ (填字母)。
A.铁电极为正极,碳电极为负极
B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利于除污
C.碳电极上的反应环境为无溶解氧环境
D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面
(1)下图为探究金属
 是否腐蚀的示意图
是否腐蚀的示意图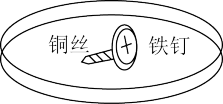
在培养皿中加入一定量的琼脂和饱和
 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为(2)碳钢在空气中容易被腐蚀,加入钼酸盐有利于缓蚀,其缓蚀原理是在钢铁表面形成
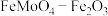 保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入
保护膜。要对密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入铝酸盐外还需加入 ,则
,则 的作用是
的作用是(3)支撑海港码头基础的钢管桩,常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。

①该保护方法叫作
②下列有关表述正确的是
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(4)利用烧结的铁碳混合材料可除去废水中的污染物,在有、无溶解氧的情况下均可在溶液中生成絮凝剂,实现高效工作,其作用原理图示如下:

铁电极的电极反应为
下列叙述正确的是
A.铁电极为正极,碳电极为负极
B.经过加热烧结的铁碳混合物表面空隙发达,吸附能力大幅提高,有利于除污
C.碳电极上的反应环境为无溶解氧环境
D.铁碳混合材料工作过程中电子从铁电极流出,被絮凝剂运输至碳电极表面
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某小组学生研究常见的金属腐蚀现象,分析其原理。按要求回答下列问题。
(1)甲同学设计如图所示对比实验。当a中滴入 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的__ (填“快”或“慢”)。其原因是_____________________________________________________ 。
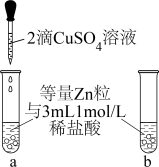
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
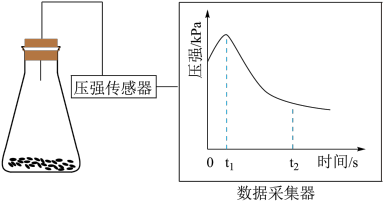
①0~ 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为____________ 。
② ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为_____________________________________________________ 。
③0~ 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________________________________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________________________ (填“氧化反应”或“还原反应”)。
②当暖贴放热结束时,铁粉转化成的物质中可能含有________________________ 。
(1)甲同学设计如图所示对比实验。当a中滴入
 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①0~
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③0~
 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度55,最高温度63,发热时间12小时以上 |
②当暖贴放热结束时,铁粉转化成的物质中可能含有
您最近一年使用:0次



