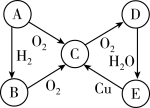
A是用途最广的金属,B、C是常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显血红色,它们相互转化关系如图所示。
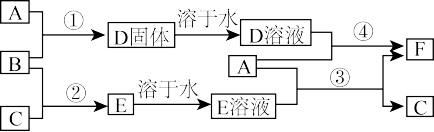
请回答:
(1)写出B物质的化学式:____________ ;F的化学式:__________ 。
(2)A在一定的条件下可与水蒸气发生反应,反应的化学反应方程式为:___________________ 。写出第④步反应的离子方程式______________________ 。
(3)F溶液中滴入NaOH溶液可能产生的实验现象是___________________ ;
(4)将D的饱和溶液滴加到沸水中可以制得一种胶体,写出该反应的化学反应方程式____________ 。
(5)在100mL的F溶液中通入标准状况224mLCl2,F溶液恰好转化成D溶液,则原F溶液的物质的量浓度为__________ 。

请回答:
(1)写出B物质的化学式:
(2)A在一定的条件下可与水蒸气发生反应,反应的化学反应方程式为:
(3)F溶液中滴入NaOH溶液可能产生的实验现象是
(4)将D的饱和溶液滴加到沸水中可以制得一种胶体,写出该反应的化学反应方程式
(5)在100mL的F溶液中通入标准状况224mLCl2,F溶液恰好转化成D溶液,则原F溶液的物质的量浓度为
更新时间:2016-12-09 10:59:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O Fe(OH)3(胶体)+3HCl。
Fe(OH)3(胶体)+3HCl。
(1)判断胶体制备是否成功,可利用胶体的________ 。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到_________________________________ ,其原因是_________________________________________ 。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会________ ,原因是____________________________________________________________________ 。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会________ ,原因是_____________________________________________________________________ 。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是_________________________________________ 。
②随后沉淀溶解,此反应的离子方程式是_________________________________ 。
 Fe(OH)3(胶体)+3HCl。
Fe(OH)3(胶体)+3HCl。(1)判断胶体制备是否成功,可利用胶体的
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是
②随后沉淀溶解,此反应的离子方程式是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I.甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。 试回答下列问题:
(1)其中操作正确的同学是_______ ,写出此过程中的化学方程式:_______ ;
(2)证明有Fe(OH)3胶体生成的最简单实验操作是_______ ;
(3)Fe(OH)3胶体能不能透过滤纸:_______ (填“能”或“不能”)。
(4)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带_______ 电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是_______ ;
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为______ ;继续滴加,沉淀最终消失且得棕黄色溶液,写出化学方程式_______ ;
④欲除去Fe(OH)3胶体中混有的NaCl,所用仪器物品是______ ;操作名称是______ 。
I.甲同学向稀氯化铁溶液中加入少量的NaOH溶液;
II.乙同学直接加热饱和FeCl3溶液;
III.丙同学向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。 试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的最简单实验操作是
(3)Fe(OH)3胶体能不能透过滤纸:
(4)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
②向其中加入饱和Na2SO4溶液,产生的现象是
③向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为
④欲除去Fe(OH)3胶体中混有的NaCl,所用仪器物品是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验兴趣小组同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。根据所学知识回答下列问题:
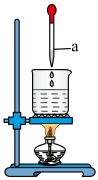
(1)仪器a的名称为___________ 。
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为___________ 。
②证明有 胶体生成的方法是
胶体生成的方法是___________ 。
③下列关于氢氧化铁胶体的说法正确的是___________ (填序号)。
A.具有吸附性 B.单个氢氧化铁分子的直径大于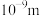
④向 胶体中逐滴加入过量稀硫酸,现象是
胶体中逐滴加入过量稀硫酸,现象是___________ 。

(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为
②证明有
 胶体生成的方法是
胶体生成的方法是③下列关于氢氧化铁胶体的说法正确的是
A.具有吸附性 B.单个氢氧化铁分子的直径大于
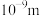
④向
 胶体中逐滴加入过量稀硫酸,现象是
胶体中逐滴加入过量稀硫酸,现象是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学按下列步骤配制500 mL 0.2 mol·L-1 Na2SO4溶液,请填写下表并回答有关问题。
(1)上述实验中使用容量瓶前应_______ 。
(2)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是_______ 。
(3)上述配制溶液的过程缺少步骤⑤,⑤是_______ 。
(4)若进行⑥步操作时加蒸馏水超过刻度线,则需_______ 。
(5)在实验中,以下操作造成实验结果偏低的是_______ (填字母)。
A.在转移溶液时有液体溅到容量瓶外
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头液管加蒸馏水至刻度线
实验步骤 | 有关问题 |
| ①计算所需Na2SO4的质量 | 需要称量Na2SO4的质量为 |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是 |
| ③将Na2SO4加入200 mL烧杯中,并加入适量水 | 为了加快溶解速率,用玻璃棒搅拌 |
| ④将烧杯中溶液转移至 | 为了防止溶液溅出,应用玻璃棒引流 |
| ⑥向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线以下1~2厘米处应 改用胶头滴管加蒸馏水到凹液面与刻度线水平相切 |
(2)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是
(3)上述配制溶液的过程缺少步骤⑤,⑤是
(4)若进行⑥步操作时加蒸馏水超过刻度线,则需
(5)在实验中,以下操作造成实验结果偏低的是
A.在转移溶液时有液体溅到容量瓶外
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头液管加蒸馏水至刻度线
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】欲配制480mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液的体积是_______ ,已有下列仪器:烧杯、量筒、胶头滴管、玻璃棒,还需用到的仪器是_______ 。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。请回答下列问题:
(1)用w来表示该温度下氢氧化钠的溶解度(S)为_______ 。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为_______ 。
(3)用w、d表示溶液中溶质的物质的量浓度(c)为_______ 。
(4)用c、d表示溶液中溶质的质量分数(w)为_______ 。
(5)用S、d表示溶液中溶质的物质的量浓度(c)为_______ 。
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(6)该“84消毒液”的物质的量浓度约为_______ mol·L-1。(保留小数点后一位)
(7)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=_______ mol·L-1。
(8)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。
(9)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为_______ mol·L-1。
②需用浓硫酸的体积为_______ mL。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为
(2)用m、V表示溶液中溶质的物质的量浓度(c)为
(3)用w、d表示溶液中溶质的物质的量浓度(c)为
(4)用c、d表示溶液中溶质的质量分数(w)为
(5)用S、d表示溶液中溶质的物质的量浓度(c)为
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(6)该“84消毒液”的物质的量浓度约为
(7)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(8)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。
| A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| C.需要称量NaClO固体的质量为143.0 g |
①所配制的稀硫酸中,H+的物质的量浓度为
②需用浓硫酸的体积为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C是红色金属单质,H为气体.它们的相互转化关系如下图所示。

请回答下列问题:
(1)写出下列物质的化学式:B_______ D_______ I_______ J_______
(2)反应①②③④中属于置换反应的是_______ (填序号)
(3)写出反应④的化学方程式_______
(4)写出反应②的离子方程式_______ (澄清石灰水过量)
(5)写出反应⑤的离子方程式_______

请回答下列问题:
(1)写出下列物质的化学式:B
(2)反应①②③④中属于置换反应的是
(3)写出反应④的化学方程式
(4)写出反应②的离子方程式
(5)写出反应⑤的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示。
(1)如果A是淡黄色固体,回答下列问题。
①写出A、E的化学式:A________ 、E________ 。
②C→D的化学方程式为____________ 。
③将足量的物质C通入BaCl2溶液中,下列说法正确的是________ (填字母序号)。
a.溶液中出现白色沉淀
b.溶液没有明显变化
c.若继续通入Cl2或NH3,则溶液中均出现白色沉淀
(2)如果A是无色气体,回答下列问题。
①D→E的化学方程式为_______ 。
②E→C的离子方程式为_______ 。

(1)如果A是淡黄色固体,回答下列问题。
①写出A、E的化学式:A
②C→D的化学方程式为
③将足量的物质C通入BaCl2溶液中,下列说法正确的是
a.溶液中出现白色沉淀
b.溶液没有明显变化
c.若继续通入Cl2或NH3,则溶液中均出现白色沉淀
(2)如果A是无色气体,回答下列问题。
①D→E的化学方程式为
②E→C的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。
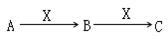
(1)若A由第三周期2种元素组成。常温下,0.1mol/L X溶液的pH=13,则R在周期中的位置是___________ 。X中阴离子的电子式是_________ ,B转化为C的离子方程式是__________ 。
(2)若常温下A、B、C、X均为气态物质,1mol A中含有共价键的数目约为1.806×1024,X为单质,A与X反应生成B的化学方程式是___________ ;在一定条件下,A可与C反应消除C对大气的污染,该反应的化学方程式是____________ 。
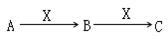
(1)若A由第三周期2种元素组成。常温下,0.1mol/L X溶液的pH=13,则R在周期中的位置是
(2)若常温下A、B、C、X均为气态物质,1mol A中含有共价键的数目约为1.806×1024,X为单质,A与X反应生成B的化学方程式是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下列框图进行反应。又知E溶液是无色的。
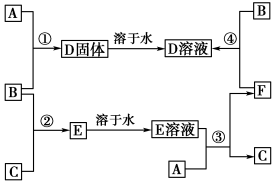
请回答:
(1)画出B原子结构示意图:___________ 。
(2)写出反应①的化学方程式:___________ 。
(3)写出反应②的离子方程式:___________ 。
(4)写出反应③的离子方程式:___________ 。

请回答:
(1)画出B原子结构示意图:
(2)写出反应①的化学方程式:
(3)写出反应②的离子方程式:
(4)写出反应③的离子方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列转化中,A和C均为单质,其中A为常见金属,C为气体,常温下B为液体(部分产物省略)。
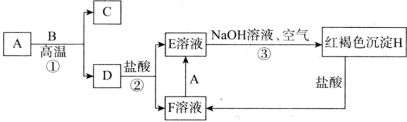
回答下列问题:
(1)A的化学式为___________ ,D的俗名为___________ 。
(2)上述反应①、②、③中属于氧化还原反应的是___________ (填序号)。
(3)反应①的化学方程式为___________ 。
(4)③的反应过程中的实验现象为___________ 。
(5)除去F溶液中混有的少量E的离子方程式为___________ 。

回答下列问题:
(1)A的化学式为
(2)上述反应①、②、③中属于氧化还原反应的是
(3)反应①的化学方程式为
(4)③的反应过程中的实验现象为
(5)除去F溶液中混有的少量E的离子方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A为金属单质,它们之间能发生如下反应(部分产物未标出)
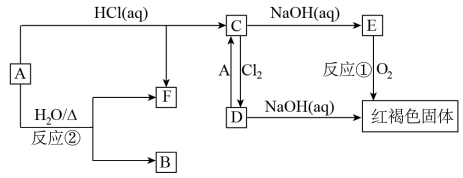
请根据以上信息回答下列问题:
(1)写出物质B的化学式:___________
(2)写出下列反应的化学方程式:
反应①______________________________________________________________________
反应②______________________________________________________________________
(3)写出下列反应的离子方程式:
反应C→D______________________________________________________________________
反应D→C_____________________________________________________________________
(4)检验D中阳离子的方法:_________________________________________________________

请根据以上信息回答下列问题:
(1)写出物质B的化学式:
(2)写出下列反应的化学方程式:
反应①
反应②
(3)写出下列反应的离子方程式:
反应C→D
反应D→C
(4)检验D中阳离子的方法:
您最近半年使用:0次



