在100mL含等物质的量的HBr和H2SO3的溶液里通入0.01molCl2,有一半Br-被氧化为Br2(已知Br2能氧化H2SO3)。原溶液中H2SO3的浓度等于
| A.0.0075 mol/L | B.0.0018mol/L | C.0.075mol/L | D.0.08mol/L |
11-12高一上·黑龙江大庆·期末 查看更多[3]
湖南省岳阳市部分学校2023-2024学年高一上学期11月期中联考化学试题(已下线)2010—2011学年黑龙江省大庆中学高一上学期期末考试化学试卷2015-2016学年安徽省合肥一中等三校高一上期末化学试卷
更新时间:2016-12-09 11:00:57
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是


| A.整个转化过程中Fe3+可以循环使用 |
| B.过程①发生复分解反应 |
| C.过程中n(Fe3+)不变,当有1mol硫生成时,消耗0.5molO2 |
D.过程②中,发生反应的离子方程式为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在反应 11P4 + 60CuSO4 + 96H2O = 20Cu3P + 24H3PO4 + 60H2SO4 中, 6 mol CuSO4 能氧化 P4的物质的量为
| A.0.3 mol | B.1.2 mol | C.1.1 mol | D.0.6 mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向2mL0.2mol/LCuSO4溶液中滴加0.2mol/LNa2SO3溶液时溶液变绿,继续滴加产生棕黄色沉淀,经检验棕黄色沉淀中不含 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2: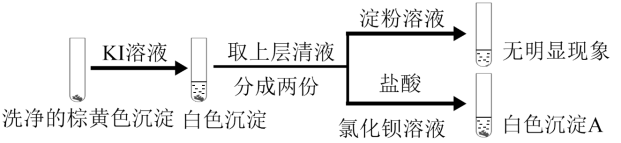
已知: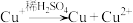 ,
,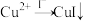 (白色)
(白色)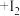 。
。
下列同学对实验现象的分析正确的是
 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2:

已知:
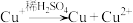 ,
,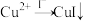 (白色)
(白色)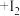 。
。下列同学对实验现象的分析正确的是
A.实验1中加入稀 后溶液变蓝可证实棕黄色沉淀中含有 后溶液变蓝可证实棕黄色沉淀中含有 |
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有 |
C.实验2中加入淀粉溶液后无明显现象,说明不存在 |
D.在 的存在下, 的存在下, 与 与 发生了氧化还原反应,产生CuI沉淀和 发生了氧化还原反应,产生CuI沉淀和 ,说明棕黄色沉淀中含有 ,说明棕黄色沉淀中含有 和 和 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知还原性 >I-。某钠盐溶液可能含有阴离子Cl-、Br-、I-、
>I-。某钠盐溶液可能含有阴离子Cl-、Br-、I-、 、
、 、
、 。为鉴定这些离子,分别取少量溶液进行以下实验:
。为鉴定这些离子,分别取少量溶液进行以下实验:
①用pH试纸测得混合液呈碱性;
②加盐酸后生成无色气体,该气体能使饱和石灰水变浑浊;
③滴加少量氯水,加CCl4振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中产生白色沉淀。
下列有关说法正确的是( )
 >I-。某钠盐溶液可能含有阴离子Cl-、Br-、I-、
>I-。某钠盐溶液可能含有阴离子Cl-、Br-、I-、 、
、 、
、 。为鉴定这些离子,分别取少量溶液进行以下实验:
。为鉴定这些离子,分别取少量溶液进行以下实验:①用pH试纸测得混合液呈碱性;
②加盐酸后生成无色气体,该气体能使饱和石灰水变浑浊;
③滴加少量氯水,加CCl4振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中产生白色沉淀。
下列有关说法正确的是( )
A.由实验①和②可确定溶液中一定含有 | B.由实验③可确定溶液中一定不含Br-、I- |
C.由实验④可确定溶液中一定含有 | D.该溶液中一定含有I-、 ,可能含有 ,可能含有 |
您最近一年使用:0次

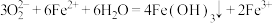
 溶液:
溶液:
 溶液:
溶液:
 溶液暴露在空气中:
溶液暴露在空气中:


