(1)配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3)
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O
_______
(2)此反应配平时可以有多组系数,其原因是_______
(3)请简述检验溶液中的金属阳离子的实验操作及现象_______
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O(2)此反应配平时可以有多组系数,其原因是
(3)请简述检验溶液中的金属阳离子的实验操作及现象
2010·江西·二模 查看更多[1]
(已下线)江西省重点中学协作体2010届高三第二次联考(化学)
更新时间:2016-12-08 16:28:50
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】实验证明,以下六种物质是一个氧化还原反应的反应物和生成物:NO、 、
、 、
、 、
、 和
和 。
。
(1)这六种物质中,_______ 是反应物,_______ 是生成物。
(2)反应物中,氧化剂是_______ ,被还原的元素是_______ 。
 、
、 、
、 、
、 和
和 。
。(1)这六种物质中,
(2)反应物中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求写化学方程式:
(1)一种单质还原一种化合物_____________________________________
(2)一种单质氧化另一种单质_________________________________________
(3)一种非金属单质还原一种氧化物________________________________________
(4)同一物质中一种元素氧化另一种元素______________________________________
(1)一种单质还原一种化合物
(2)一种单质氧化另一种单质
(3)一种非金属单质还原一种氧化物
(4)同一物质中一种元素氧化另一种元素
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氮在自然界中的循环如图所示。
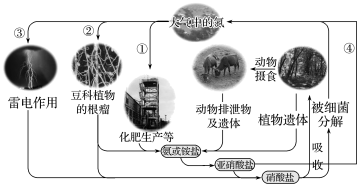
(1)过程①称为___ ,写出合成氨反应的化学方程式:___ ,该反应中氮气显____ 性(填“氧化”或“还原”,下同)。
(2)过程②中能通过____ 的作用将空气中的氮气固定下来,写出③中固氮反应的化学方程式:___ ,该反应中氮气显____ 性。
(3)过程④中的亚硝酸盐有毒,工业上若直接排放将造成对环境的污染。已知NaNO2遇到还原性较强的NH 会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是
会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是___ (填字母)。
a.H2O2 b.NH4Cl c.KNO3 d.NaOH

(1)过程①称为
(2)过程②中能通过
(3)过程④中的亚硝酸盐有毒,工业上若直接排放将造成对环境的污染。已知NaNO2遇到还原性较强的NH
 会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是
会被还原为N2,在废液中加入下列物质不能使NaNO2无害化排放的是a.H2O2 b.NH4Cl c.KNO3 d.NaOH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)合成氨工业生产中所用的αFe催化剂的主要成分是FeO、Fe2O3。
①某FeO、Fe2O3混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、Fe2O3的物质的量之比为____ 。
②当催化剂中+2价Fe与+3价Fe的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物的混合物中铁原子的质量分数为____ (用小数表示,保留2位小数)。
(2)电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
①用FeO稀盐酸、氯气制取FeCl3溶液的离子方程式为____ 、____ 。检验溶液中Fe3+的试剂是____ 。
②写出FeCl3溶液与金属铜发生反应的化学方程式:____ ,当转移电子数为6.02×1024时,被氧化的物质的质量为____ 。
①某FeO、Fe2O3混合物中,铁原子、氧原子的物质的量之比为4∶5,其中FeO、Fe2O3的物质的量之比为
②当催化剂中+2价Fe与+3价Fe的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物的混合物中铁原子的质量分数为
(2)电子工业常用30%的FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。
①用FeO稀盐酸、氯气制取FeCl3溶液的离子方程式为
②写出FeCl3溶液与金属铜发生反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Na2FeO4 的制备方法有次氯酸盐氧化法(湿法):该法是在碱性条件下,利用可溶性次氯酸盐氧化氢氧化铁,试写出并配平这一离子方程式_____________ ,每生成 1molNa2FeO4,转移的电子数目是___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】 是一种重要的化学品,具有广泛的应用
是一种重要的化学品,具有广泛的应用
(1) 的性质研究。
的性质研究。
①理论分析: 具有氧化性和还原性,从O元素的化合价分析原因:
具有氧化性和还原性,从O元素的化合价分析原因:_______ 。
②实验研究:向酸化的 溶液中加入
溶液中加入 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(
溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊( ),继续加入
),继续加入 溶液,红色浑浊又变为蓝色溶液,这个过程可以反复多次。下列关于上述过程的说法
溶液,红色浑浊又变为蓝色溶液,这个过程可以反复多次。下列关于上述过程的说法不正确 的是_______ (填序号)。
A. 是
是 分解反应的催化剂
分解反应的催化剂
B. 既表现氧化性又表现还原性
既表现氧化性又表现还原性
C. 将
将 还原为
还原为
D.发生了反应
(2) 的制备。某种制取过氧化氢的方法如下:
的制备。某种制取过氧化氢的方法如下:
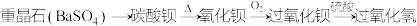
①用氧化钡制取过氧化钡(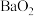 )的反应属于
)的反应属于_______ 反应(填序号)。
A.化合 B.分解 C.氧化还原 D.复分解
②用过氧化钡制取过氧化氢的离子方程式是_______ 。
③上述方法制得的过氧化氢浓度低且能耗高。有人提出下列制取过氧化氢的方案,从原理上分析合理的是_______ (填序号)。
A.在一定条件下,使用适宜的氧化剂氧化
B.在一定条件下, 还原
还原
C.在一定条件下, 氧化
氧化
(3) 的定量检测。用酸性
的定量检测。用酸性 测定
测定 的含量,反应原理如下(该条件下可忽略
的含量,反应原理如下(该条件下可忽略 的分解)。补充完整该离子方程式并配平
的分解)。补充完整该离子方程式并配平__________ 。
□ □
□ ___
___ □
□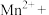 □_____
□_____
 是一种重要的化学品,具有广泛的应用
是一种重要的化学品,具有广泛的应用(1)
 的性质研究。
的性质研究。①理论分析:
 具有氧化性和还原性,从O元素的化合价分析原因:
具有氧化性和还原性,从O元素的化合价分析原因:②实验研究:向酸化的
 溶液中加入
溶液中加入 溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(
溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊( ),继续加入
),继续加入 溶液,红色浑浊又变为蓝色溶液,这个过程可以反复多次。下列关于上述过程的说法
溶液,红色浑浊又变为蓝色溶液,这个过程可以反复多次。下列关于上述过程的说法A.
 是
是 分解反应的催化剂
分解反应的催化剂B.
 既表现氧化性又表现还原性
既表现氧化性又表现还原性C.
 将
将 还原为
还原为
D.发生了反应

(2)
 的制备。某种制取过氧化氢的方法如下:
的制备。某种制取过氧化氢的方法如下: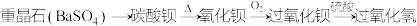
①用氧化钡制取过氧化钡(
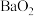 )的反应属于
)的反应属于A.化合 B.分解 C.氧化还原 D.复分解
②用过氧化钡制取过氧化氢的离子方程式是
③上述方法制得的过氧化氢浓度低且能耗高。有人提出下列制取过氧化氢的方案,从原理上分析合理的是
A.在一定条件下,使用适宜的氧化剂氧化

B.在一定条件下,
 还原
还原
C.在一定条件下,
 氧化
氧化
(3)
 的定量检测。用酸性
的定量检测。用酸性 测定
测定 的含量,反应原理如下(该条件下可忽略
的含量,反应原理如下(该条件下可忽略 的分解)。补充完整该离子方程式并配平
的分解)。补充完整该离子方程式并配平□
 □
□ ___
___ □
□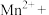 □_____
□_____
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某无色透明溶液中可能大量存在Ag+、Mg2+、Fe3+、Cl-、OH-、NO 中的几种离子。
中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是__________ 。
(2)取少量原溶液,向其中加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定存在的离子是__________ ,有关离子方程式为__________ 。
(3)向(2)的滤液中加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是__________ .
(4)Cl-、OH-、NO 中一定不存在的离子是
中一定不存在的离子是__________ 。
 中的几种离子。
中的几种离子。(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,向其中加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,说明原溶液中肯定存在的离子是
(3)向(2)的滤液中加入过量NaOH溶液,出现白色沉淀,说明原溶液中肯定存在的离子是
(4)Cl-、OH-、NO
 中一定不存在的离子是
中一定不存在的离子是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为检验某种阳离子为Na+的溶液中含有的阴离子是SO 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是____ 。
方案一:检验CO :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
方案二:检验SO :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是方案一:检验CO
 :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成方案二:检验SO
 :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有一包白色粉末,可能含有Na2SO4、CaCO3、KCl、BaCl2、CuSO4中的一种或几种,按以下步骤进行实验:
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是_______ ,一定没有的物质是_______ ,可能含有的物质是_______ (均填写化学式)。
(2)上述实验中第②步反应的离子方程式是_______ 。
①将此粉末溶于水,得到无色溶液和白色沉淀;
②将足量稀盐酸加入白色沉淀中,沉淀部分溶解,并有气泡产生。
(1)根据上述实验现象,判断此粉末中一定含有的物质是
(2)上述实验中第②步反应的离子方程式是
您最近一年使用:0次



