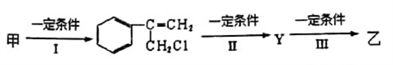FeCl3可通过多种途径转化为FeCl2。
(1)在FeCl3溶液中加入适量氢碘酸,发生反应的离子方程式为
___________________________________________________
(2)工业上常将无水FeCl3在氮气做保护气下加热至300℃―350℃,通入干燥H2,而制得FeCl2。该反应的化学反应方程式为__________________________________________
(3)工业上另一种制备FeCl2的方法是:将无水FeCl3与适量氯苯(C6H5Cl)混合,在130℃持续加热约3小时,可发生如下反应:
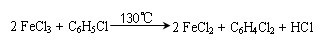
依据有机反应规律,该反应中氯苯发生的是______________ (填有机反应类型)。
(4)分析上述三个反应,下列有关说法正确的是_____________ (填序号)。
①反应(1)中,氢碘酸既表现了酸性,又表现了还原性
②反应(3)中,HCl为氧化产物
③上述三个反应中,FeCl2均为还原产物
(5)请另写出一个FeCl3转化成FeCl2的化学方程式:_______________
(1)在FeCl3溶液中加入适量氢碘酸,发生反应的离子方程式为
(2)工业上常将无水FeCl3在氮气做保护气下加热至300℃―350℃,通入干燥H2,而制得FeCl2。该反应的化学反应方程式为
(3)工业上另一种制备FeCl2的方法是:将无水FeCl3与适量氯苯(C6H5Cl)混合,在130℃持续加热约3小时,可发生如下反应:
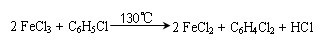
依据有机反应规律,该反应中氯苯发生的是
(4)分析上述三个反应,下列有关说法正确的是
①反应(1)中,氢碘酸既表现了酸性,又表现了还原性
②反应(3)中,HCl为氧化产物
③上述三个反应中,FeCl2均为还原产物
(5)请另写出一个FeCl3转化成FeCl2的化学方程式:
9-10高二下·河北唐山·期中 查看更多[1]
(已下线)2009-2010学年度唐山二中高二第二学期期中化学试卷
更新时间:2010-06-08 10:46:57
|
相似题推荐
【推荐1】ClO2是一种黄绿色或橙黄色的气体,极易溶于水,可用于水的消毒杀菌、水体中Mn2+等重金属离子的除去及烟气的脱硫脱硝。回答下列问题:
(1)将过硫酸钠(Na2S2O8,结构、性质与过氧化钠相似)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价是___ 价,该反应中氧化剂和还原剂的数目之比为___ 。
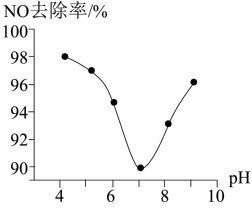
(2)为研究ClO2脱硝(将氮氧化物转化成NO )的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
)的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
已知:NO的去除率=(1- )×100%
)×100%
①要使NO的去除率更高,应控制的条件是___ 。
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应生成更强的吸收剂NaClO2,写出碱性条件下NaClO2脱除NO反应的离子方程式___ 。
(1)将过硫酸钠(Na2S2O8,结构、性质与过氧化钠相似)溶液加入亚氯酸钠(NaClO2)中可制备ClO2,NaClO2中Cl元素的化合价是
(2)为研究ClO2脱硝(将氮氧化物转化成NO
 )的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
)的适宜条件,在1L含200mgClO2的溶液中加NaOH溶液调节pH,通入NO气体并测定NO的去除率,其关系如图所示:
已知:NO的去除率=(1-
 )×100%
)×100%①要使NO的去除率更高,应控制的条件是
②当溶液pH>7时,NO的去除率增大的原因是ClO2与NaOH溶液反应生成更强的吸收剂NaClO2,写出碱性条件下NaClO2脱除NO反应的离子方程式
您最近一年使用:0次
【推荐2】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是_____ (填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为______ mol。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_________ 。
(1)浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】关于As的反应中,反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
①已知KBrO3在反应中得到电子,则该反应的还原剂是_______ 。
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为_______ 。
③根据上述反应可推知_______ 。(填序号)
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
④在该反应中,氧化剂与还原剂的物质的量之比为_______ 。
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
④在该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】多酚氧化酶是自然界中分布极广的一种金属蛋白酶,与植物的抗病性有关。配合物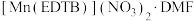 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。___________ 组峰,上述反应的反应类型为___________ ; 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:___________ 。
(2)已知EDTA的相对分子质量为292,熔点为250℃,烃 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是___________ 。
(3)图中有机物在镍催化及加热条件下,不能与 反应的是
反应的是___________ 。EDTA中存在的化学键有___________ (填字母)。
A.离子键 B. 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键
(4)EDTB中氮原子的杂化类型是___________ ,X的VSEPR模型名称是___________ 。
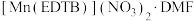 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。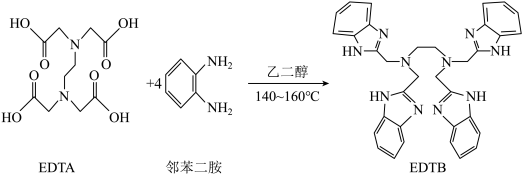 +8X
+8X
 是碱性官能团,从结构角度解释原因:
是碱性官能团,从结构角度解释原因:(2)已知EDTA的相对分子质量为292,熔点为250℃,烃
 (无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是
(无支链)的相对分子质量为296,熔点为40℃,导致这种差异的主要原因是(3)图中有机物在镍催化及加热条件下,不能与
 反应的是
反应的是A.离子键 B.
 键 C.非极性键 D.氢键
键 C.非极性键 D.氢键(4)EDTB中氮原子的杂化类型是
您最近一年使用:0次
【推荐2】按要求填写下列空白:
(1)CH3CH=CH2+_______ →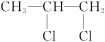 ,反应类型:
,反应类型:_______ ;
(2)CH3CH=CH2+Cl2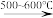
_______ +HCl,反应类型:_______ ;
(3)_______ +Br2→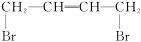 ,反应类型:
,反应类型:_______ ;
(4)_______ 
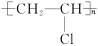 ,反应类型:
,反应类型:_______ 。
(1)CH3CH=CH2+
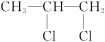 ,反应类型:
,反应类型:(2)CH3CH=CH2+Cl2
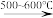
(3)
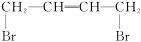 ,反应类型:
,反应类型:(4)

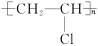 ,反应类型:
,反应类型:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】利用细菌处理有机废水产生的电能可以进行脱硫,从而达到废物利用同时有利于环境保护。脱硫原理:利用羟基自由化基(·OH,氧元素为-1价)将燃煤中的含硫物质(主要是 )氧化除去,其装置示意图如图所示。
)氧化除去,其装置示意图如图所示。

(1)a为___________ 极,电极反应式为___________ 。
(2)X为___________ (填“阳离子”或“阴离子”)交换膜。
(3)利用羟基自由基除去煤中 的反应的离子方程式:
的反应的离子方程式:___________ 。理论上处理12.0g  ,b极消耗标况下空气(氧气占空气体积分数21%)约为
,b极消耗标况下空气(氧气占空气体积分数21%)约为___________ L。
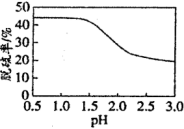
(4)利用上述装置对某含 的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。pH大于1.5后脱硫率下降的可能原因有:
的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。pH大于1.5后脱硫率下降的可能原因有:
①随着pH的升高,反应物的氧化性或还原性降低;
②___________ 。
 )氧化除去,其装置示意图如图所示。
)氧化除去,其装置示意图如图所示。
(1)a为
(2)X为
(3)利用羟基自由基除去煤中
 的反应的离子方程式:
的反应的离子方程式: ,b极消耗标况下空气(氧气占空气体积分数21%)约为
,b极消耗标况下空气(氧气占空气体积分数21%)约为(4)利用上述装置对某含
 的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。pH大于1.5后脱硫率下降的可能原因有:
的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。pH大于1.5后脱硫率下降的可能原因有:
①随着pH的升高,反应物的氧化性或还原性降低;
②
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某再回收利用公司对一厨房铁铝合金废旧家具进行回收利用,其流程如下图所示:
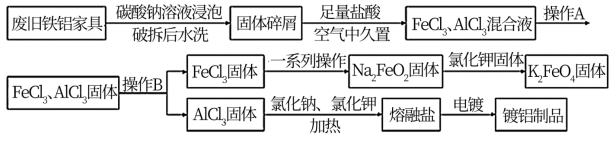
请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是_______________ ;在空气中久置的目的是_________________ 。
(2)同条件下Na2FeO4溶解度__________ K2FeO4溶解度(填“低于”,“高于”, “不确定”),推测K2FeO4在净水方面的作用_______________ 。(至少答两条)
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用__________ 。
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为___________________ 。(写出一个电极反应即可)
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为______________________ 。
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为____________ 。

请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是
(2)同条件下Na2FeO4溶解度
(3)已知K2FeO4水解显碱性。在洗涤K2FeO4固体时最好选用
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电镀的主要电极反应式为
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)4]-。已知25℃时氢氧化铝在pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解方式的溶度积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某研究所对含硫酸亚铁和硫酸铜的工业废料进行相关的研究。实验过程如下:
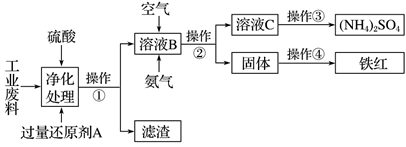
回答下列问题:
(1)滤渣的成分为________ ,操作②的名称为_____________________ 。
(2)上图溶液B中所发生反应的离子方程式为____________________________ 。
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是____________________________________________________ 。
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要_______________ 。
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。
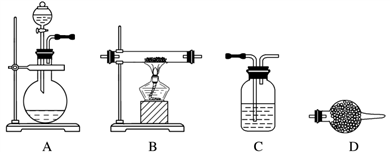
①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→________ →________ →________ →D(除D装置外,其他装置不能重复使用),最后D装置中所加药品为____________ ,其作用是________________________ 。
②点燃B处酒精灯之前必须进行的操作是____________________________ 。

回答下列问题:
(1)滤渣的成分为
(2)上图溶液B中所发生反应的离子方程式为
(3)实验要求先向溶液B中通入过量的空气,证明通入空气过量的方法是
(4)操作③第一步需要的仪器除了酒精灯、铁架台外,还需要
(5)某同学利用下面装置制备氢气并利用氢气还原某金属氧化物,根据要求回答问题。

①请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是A→
②点燃B处酒精灯之前必须进行的操作是
您最近一年使用:0次