短周期的五种主族元素A、B、C、D、E原子序数依次变小。A的单质在常温下为气态,B、D属于同一主族,C为自然界含量最多的金属元素,D的最外层电子数为次外层的2倍,E为周期表中原子半径最小的元素。
(1)A、B的元素名称为___________ 、___________ 。
(2)B、D的原子半径大的是___________ (填元素符号)。
(3)A、C的最高价氧化物的水化物反应的离子方程式_________________________ 。
(4)A、D的最高价氧化物的水化物的酸性弱的是_______ ,氢化物稳定性强的是________ (用化学用语填写)。
(1)A、B的元素名称为
(2)B、D的原子半径大的是
(3)A、C的最高价氧化物的水化物反应的离子方程式
(4)A、D的最高价氧化物的水化物的酸性弱的是
更新时间:2016-12-09 14:54:49
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表的一部分如图,根据①~⑨在元素周期表中的位置,按题目要求回答下列问题:
(1)在元素①~⑨中,金属性最强的元素是_____ (填元素符号)。
(2)③~⑥四种元素的原子半径由大到小的顺序是_____ (填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是_____ (填化学式)。
(4)写出由元素⑤和元素④形成的原子个数比为1:1的化合物的电子式:_____ 。
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:_____ 。
(6)高温灼烧仅由元素⑤和元素⑧形成的常见化合物时,火焰呈_____ 色。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)③~⑥四种元素的原子半径由大到小的顺序是
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是
(4)写出由元素⑤和元素④形成的原子个数比为1:1的化合物的电子式:
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:
(6)高温灼烧仅由元素⑤和元素⑧形成的常见化合物时,火焰呈
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表前20号元素的有关信息:
已知:Li的半径为0.152nm,Be的半径为0.111nm。回答下列问题:
(1)元素e在周期表中的位置为_______ ,元素y与e同主族且多一电子层,y的原子结构示意图为_______ 。
(2)c、d、g原子半径由大到小的顺序为_______ (填元素符号)。
(3)BaCl2溶液中先加入d元素最高价氧化物对应的水化物,再通入eb2,可观察到的现象是_______ ,发生反应的离子方程式为_______ 。
| 元素 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.030 | 0.066 | 0.117 | 0.232 | 0.106 | 0.186 | 0.143 | 0.099 |
| 最高正化合价 | +1 | +4 | +1 | +6 | +1 | +3 | +7 | |
| 最低负化合价 | -2 | -4 | -2 | -1 |
(1)元素e在周期表中的位置为
(2)c、d、g原子半径由大到小的顺序为
(3)BaCl2溶液中先加入d元素最高价氧化物对应的水化物,再通入eb2,可观察到的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)锂在元素周期表的位置是___________ 。锂原子核外能量最高的电子所处的轨道是___________ 。
(2)写出一条判断锂与相邻同主族金属元素金属性强弱的实验依据。___________
(3)氢化锂(LiH)是离子化合物,写出其电子式___________ ,LiH中阴离子半径大于阳离子半径,其原因是___________ 。
LiBr可作锂电池中电解质材料。用 、荌水和液溴制备
、荌水和液溴制备 的流程如下:
的流程如下:

(4)合成时,除生成LiBr外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:___________
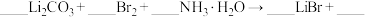
写出该反应所涉及物质中属于非电解质的电子式___________ 。
溴化锂的溶解度随温度变化曲线如图所示。
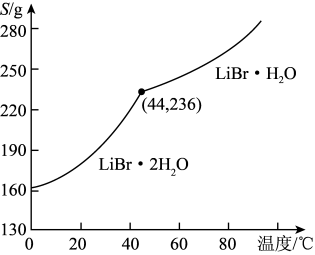
(5)从溶液中得到 晶体的实验步骤依次为:
晶体的实验步骤依次为:___________ ,___________ ,过滤,用乙醇洗涤,干燥。
(1)锂在元素周期表的位置是
(2)写出一条判断锂与相邻同主族金属元素金属性强弱的实验依据。
(3)氢化锂(LiH)是离子化合物,写出其电子式
LiBr可作锂电池中电解质材料。用
 、荌水和液溴制备
、荌水和液溴制备 的流程如下:
的流程如下:
(4)合成时,除生成LiBr外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
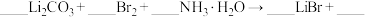
写出该反应所涉及物质中属于非电解质的电子式
溴化锂的溶解度随温度变化曲线如图所示。

(5)从溶液中得到
 晶体的实验步骤依次为:
晶体的实验步骤依次为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】A、B、C、D、E、F、G是七种常见的短周期元素,其原子序数依次增大,请根据所给信息填写表中空白,并回答下列问题:
(1)仅由表中信息还不能确定的元素是________ (填字母序号),若要确定其是何种元素,还需要的条件是________________ (填序号)。
a.单质能与氧气反应 b.最高价氧化物对应的水化物呈强酸性
c.单质在常温下为固体 d.简单氢化物的稳定性比E的简单氢化物强
(2)基本信息②中,两种元素的氧化物分别与足量的NaOH溶液反应的离子方程式为______________________________ ,____________________ 。
(3)上述某两种元素间可形成原子个数比为1∶1及1∶2的两种化合物,写出前者与H2O反应的离子方程式:______________________ 。
| 编号 | 基本信息 | 解决问题 |
| ① | 其中两种元素的原子核外电子层数与最外层电子数之比分别为1∶3,3∶1 | 这两种元素是 |
| ② | 其中一种元素的氧化物与强酸、强碱均能反应;另一种元素的单质、氧化物及氧化物对应的水化物均能与NaOH溶液反应 | 这两种元素分别是 |
| ③ | G能与A、E形成原子个数比均为4∶1的分子X、Y | X的分子式为 |
(1)仅由表中信息还不能确定的元素是
a.单质能与氧气反应 b.最高价氧化物对应的水化物呈强酸性
c.单质在常温下为固体 d.简单氢化物的稳定性比E的简单氢化物强
(2)基本信息②中,两种元素的氧化物分别与足量的NaOH溶液反应的离子方程式为
(3)上述某两种元素间可形成原子个数比为1∶1及1∶2的两种化合物,写出前者与H2O反应的离子方程式:
您最近一年使用:0次
【推荐2】有a、b、c、d、e、f、g七种元素,原子序数依次增大,前5种为短周期主族元素,f、g为第四周期的元素。有关信息如下,请回答以下问题:
(1)a、f的元素符号为______ 、______ ,分别位于元素周期表的______ 区和______ 区。
(2)e的基态原子中能量最高的电子所占的轨道形状是______ 其电子云在空间有______ 个伸展方向。
(3)d基态原子的价层电子的轨道表示式为______ ,某元素在元素周期表中位置处于d元素的左上角对角线处,它们具有部分相似的性质,请写出该元素组成的单质与氢氧化钠溶液反应的化学方程式______
(4)g基态原子的简化电子排布式为______
(5)元素f基态原子的第二电离能______ 元素g基态原子的第二电离能(填“>”、“<或“=”)
a | a能形成一种硬度最大的固体单质 |
b | b的单质为空气中百分含量最多的一种气体 |
c | c元素基态原子的电子排布式为 |
d | d基态原子的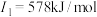 ; ; ; ; ; ; |
e | e基态原子核外3p轨道半满 |
f | f在周期表中第11纵行 |
g | g基态原子最外层电子数为2 |
(2)e的基态原子中能量最高的电子所占的轨道形状是
(3)d基态原子的价层电子的轨道表示式为
(4)g基态原子的简化电子排布式为
(5)元素f基态原子的第二电离能
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】a、b、c、d、e、f是原子序数依次增大的非0族元素,位于元素周期表的前四周期。a的一种核素无中子,b的s能级电子数与p能级的电子数之比为4:3,c与e同主族,未成对电子数为2,d在同周期元素中的原子半径最大,f在同周期元素中的未成对电子数最多。请回答下列问题:
(1)上述元素中,位于元素周期表p区的元素有________ (填元素符号),其中基态c原子中电子占据的最高能级的原子轨道形状是________ 。
(2)基态e原子的核外电子排布式为_______ ,其核外有____ 种不同空间运动状态的电子。
(3)b、c、d、e简单离子半径由大到小的顺序为_____ (用离子符号表示)。
(4)基态f原子的未成对电子数与成对电子数之比为______ 。
(1)上述元素中,位于元素周期表p区的元素有
(2)基态e原子的核外电子排布式为
(3)b、c、d、e简单离子半径由大到小的顺序为
(4)基态f原子的未成对电子数与成对电子数之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D、E 、F是分属三个短周期的六种主族元素,且原子序数依次增大。①B是植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染。②D原子的最外层电子数是最内层电子数的二分之一、③C和D能形成电子总数为30和38的两种化合物。④E与C同主族。请回答下列问题:
(1)元素F在元素周期表中的位置是_______ 。
(2) C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是______ (用离子符号回答)。
(3) C和D形成电子总数为38的化合物中化学键类型有______ (填“离子键”“极性共价键” 或“非极性共价键”)。
(4)写出D的最高价氧化物对应的水化物的电子式_______ 。
(5)E、F两种元素形成的氢化物中还原性较强的是____ (填化学式) ;用电子式表示该化合物的形成过程___________ 。
(6)写出B的10电子氢化物与足量单质F反应的化学方程式,并用双线桥法表示电子转移_________
(1)元素F在元素周期表中的位置是
(2) C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是
(3) C和D形成电子总数为38的化合物中化学键类型有
(4)写出D的最高价氧化物对应的水化物的电子式
(5)E、F两种元素形成的氢化物中还原性较强的是
(6)写出B的10电子氢化物与足量单质F反应的化学方程式,并用双线桥法表示电子转移
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、M、N为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与N分别同主族,在周期表中X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,Z、W的最外层电子数之和与M的核外电子总数相等。试回答下列问题:
(1)N元素在周期表中的位置为_____ ;Y的简单氢化物的稳定性_____ (填“>”“<”或“=”)W的简单氢化物的稳定性。
(2)X、Z形成的含18电子的化合物的结构式为_____ 。
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式_____ 。
(4)X和W组成的化合物中,既含有极性共价键又含有非极性共价键的是_____ (填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为_____ 。
(1)N元素在周期表中的位置为
(2)X、Z形成的含18电子的化合物的结构式为
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式
(4)X和W组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
(1)Y在元素周期表中的位置是___ 。
(2)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是___ 。
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为___ 。
(4)元素X的金属性比元素Y___ (填“强”或“弱”),用原子结构的知识解释原因___ 。
(5)元素Q、元素Z的含量影响钢铁性能,采用如图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。

①气体a的成分是__ (填化学式)。
②若钢样中元素Z以FeZ的形式存在,在A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是___ 。
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +5,-3 | +4,-4 | +1 |
(2)元素Q和R形成的化合物A是果实催熟剂,用A制备乙醇的化学方程式是
(3)单质铜和元素M的最高价氧化物对应水化物的稀溶液发生反应的离子方程式为
(4)元素X的金属性比元素Y
(5)元素Q、元素Z的含量影响钢铁性能,采用如图装置A在高温下将钢样中元素Q、元素Z转化为QO2、ZO2。

①气体a的成分是
②若钢样中元素Z以FeZ的形式存在,在A中反应生成ZO2和稳定的黑色氧化物,则反应的化学方程式是
您最近一年使用:0次



