某无色溶液,其中可能存在Na+、Ba2+、AlO2-、S2-、SO32-、SO42-。取该溶液进行有关实验,实验结果如下图所示。
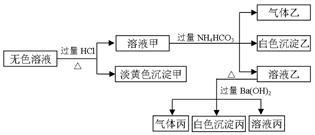
请回答下列问题:
(1)沉淀甲的化学式为_________________ ;
(2)由溶液甲生成沉淀乙的离子方程式为____________________ ;
(3)沉淀丙中一定含有____________ (填化学式,下同),可能含有_____________ ;
(4)综合上述信息,该溶液中肯定存在的离子有____________________ 。

请回答下列问题:
(1)沉淀甲的化学式为
(2)由溶液甲生成沉淀乙的离子方程式为
(3)沉淀丙中一定含有
(4)综合上述信息,该溶液中肯定存在的离子有
10-11高三上·宁夏银川·阶段练习 查看更多[1]
(已下线)2010年宁夏银川二中高三上学期第一次月考化学试题
更新时间:2016-12-09 00:52:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某盐的无色溶液中同时有Cl-、SO42-,检验时,应先检验________ 离子,首先取少量待测液于试管中,向其中加入试剂__________ 且至________ 时,经过________ 操作后,再用试剂___________ 检验另一种离子。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】由几种离子组成的混合物中可能含有下列离子中的若干种:K+、Na+、NH 、Mg2+、Cu2+、CO
、Mg2+、Cu2+、CO 、SO
、SO 。将该混合物溶于水后得到澄清的溶液,现取三份各 100mL 该溶液分别进行如下实验:
。将该混合物溶于水后得到澄清的溶液,现取三份各 100mL 该溶液分别进行如下实验:
请回答下列问题:
(1)实验 1 说明存在的离子是________ (填离子符号,下同),一定不存在的离子是___________ 。
(2)由实验 2 可知,100mL 溶液中c(NH )=
)= _______ mol•L-1。
(3)由实验3可知,100mL 溶液中n(SO )=
)= __________ mol。
(4)溶液中 c(Na+)的范围是_______________ 。
 、Mg2+、Cu2+、CO
、Mg2+、Cu2+、CO 、SO
、SO 。将该混合物溶于水后得到澄清的溶液,现取三份各 100mL 该溶液分别进行如下实验:
。将该混合物溶于水后得到澄清的溶液,现取三份各 100mL 该溶液分别进行如下实验:| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加入盐酸 | 有气泡产生 |
| 2 | 加入足量浓NaOH 溶液并加热 | 收集到标准状况下的气体1.12L |
| 3 | 加入足量 BaCl2 溶液,对所得沉淀进行洗涤、干燥、称量; | 第一次称量读数为 6.27g; 再向沉淀中加入足量盐酸,然后过滤、洗涤、干燥、称量 第二次称量读数为 2.33g |
(1)实验 1 说明存在的离子是
(2)由实验 2 可知,100mL 溶液中c(NH
 )=
)= (3)由实验3可知,100mL 溶液中n(SO
 )=
)= (4)溶液中 c(Na+)的范围是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钴酸锂一般用作锂离子电池的正极材料,需求量大,而我国极度缺乏钴资源,主要依赖进口,因而从废旧电池中进行回收具有重要意义。以废旧钴酸锂电池材料(主要成分为LiCoO2,含单质Cu及为改善电池性能添加的单质Al等)回收钴酸锂的--种工艺流程如下:

回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理,粉碎的目的是_____ 。
(2)“碱浸”所得滤液中主要溶质的化学式为__________ 、NaOH。
(3)H2O2的电子式为________ 。“酸浸”时H2O2作还原剂,还原产物为Co2+,反应的离子方程式为_________ ;上述反应的氧化产物又将铜氧化而溶解浸出,该反应的化学方程式为____________ 。
(4)“萃取铜”中的有机萃取剂用HR表示,发生萃取的反应可表示为Cu2+ +2HR CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为
CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为___________ (溶液体积变化忽略,保留小数点后两位);为回收铜,可用一定浓度的H2SO4将有机相中的铜反萃取到水相,其原理是______________________
(5)“碱浸”时少量未浸出的残余铝可在“酸浸”时浸出,萃取铜后的溶液需调pH至5.0以上将铝离子沉淀除去。若c(Co2+ ) =0.16mol·L-1,为避免析出Co(OH)2沉淀,则调pH不能超过___________ 。(已知K[Co(OH)2]=1.6×10-15)
(6)“钴、锂共沉淀”时析出CoCO3和li2CO3,经过滤、无水乙醇洗涤、80°C干燥后在750°C煅烧,反应的化学方程式为_________________ 。

回答下列问题:
(1)废旧钴酸锂电池需经放电、拆解、粉碎预处理,粉碎的目的是
(2)“碱浸”所得滤液中主要溶质的化学式为
(3)H2O2的电子式为
(4)“萃取铜”中的有机萃取剂用HR表示,发生萃取的反应可表示为Cu2+ +2HR
 CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为
CuR2++.2H+。若酸浸后的浸取液pH=1.000,c(Cu2+ ) =0.01001mol·L-1,多次萃取后水相中c(H+)为0.1200mol·L-1,则铜的萃取率为(5)“碱浸”时少量未浸出的残余铝可在“酸浸”时浸出,萃取铜后的溶液需调pH至5.0以上将铝离子沉淀除去。若c(Co2+ ) =0.16mol·L-1,为避免析出Co(OH)2沉淀,则调pH不能超过
(6)“钴、锂共沉淀”时析出CoCO3和li2CO3,经过滤、无水乙醇洗涤、80°C干燥后在750°C煅烧,反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某工业废水中存在大量的 和
和 ,欲除去废水中的Cu2+和
,欲除去废水中的Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:___________ 。
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2)a溶液和b溶液分别是___________ ,___________ (填溶质化学式)。
(3)溶液A→混合物B过程中可观察到有白色沉淀___________ 生成(填化学式),如何证明溶液中含有硫酸根离子:_______________ 。
(4)混合物B→溶液C过程中所涉及的离子方程式是___________ 。
(5)加入适量盐酸的作用是___________ 。
 和
和 ,欲除去废水中的Cu2+和
,欲除去废水中的Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2)a溶液和b溶液分别是
(3)溶液A→混合物B过程中可观察到有白色沉淀
(4)混合物B→溶液C过程中所涉及的离子方程式是
(5)加入适量盐酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硝酸铈(Ⅳ)铵的化学式为(NH4)xCe(NO3)y,是一种橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,主要用作分析试剂和氧化剂。实验室设计如下实验进行制备并测定其化学式。

步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;
②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。
步骤二:制备硝酸铈(Ⅳ)铵

步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2 m g。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1 mL水吸收。将吸收液滴入甲基橙,用c mol/LH2SO4标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2 mL。
(1)装置A中仪器的名称为_______ ,装置C的作用是_______ 。该实验以氮化钙和水制备NH3应选择装置_______ (填“A”或“D”)。
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为_______ 。装置B中发生反应的离子方程式为_______ 。
(3)该实验装置存在的一处缺陷为_______ 。
(4)“氧化沉淀”反应的离子方程式为_______ 。
(5)“烘干”采取自然干燥的原因为_______ 。
(6)计算y=_______ (用上述字母表示)。

步骤一:NH4HCO3溶液与CeCl3溶液反应制备Ce2(CO3)3。
已知:①氮化钙遇水可迅速产生NH3;
②Ce(Ⅲ)易被空气氧化成Ce(Ⅳ)。
步骤二:制备硝酸铈(Ⅳ)铵

步骤三:测定化学式
①称取一定质量的硝酸铈(Ⅳ)铵,充分灼烧得CeO2 m g。
②另称取相同质量的硝酸铈(Ⅳ)铵,加入足量NaOH溶液微热,将产生的气体全部用V1 mL水吸收。将吸收液滴入甲基橙,用c mol/LH2SO4标准溶液滴定,重复2~3次,平均消耗H2SO4标准溶液V2 mL。
(1)装置A中仪器的名称为
(2)实验时,“a”、“b”、“c”三个旋塞的打开顺序为
(3)该实验装置存在的一处缺陷为
(4)“氧化沉淀”反应的离子方程式为
(5)“烘干”采取自然干燥的原因为
(6)计算y=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】磷酸亚铁锂(LiFePO4)能可逆地嵌入、脱出锂,使其作为锂离子电池正极材料的研究及应用得到广泛关注。通过水热法制备磷酸亚铁锂的一种方法如下(装置如图所示):

I.在A中加入40 mL蒸馏水、0.01 mol H3PO4和0.01 mol FeSO4·7H2O,用搅拌器搅拌溶解后,缓慢加入0.03 mol LiOH·H2O,继续搅拌。
II.向反应液中加入少量抗坏血酸(即维生素C),继续搅拌5min。
III.快速将反应液装入反应釜中,保持170℃恒温5 h。
IV.冷却至室温,过滤。
V.用蒸馏水洗涤沉淀。
VI.干燥,得到磷酸亚铁锂产品。
回答下列问题:
(1)装置图中仪器A的名称是_______ ,根据上述实验药品的用量,A的最适宜规格为_______ (填选项)
A.100mL B.250mL C.500mL D.1000mL
(2)步骤II中,抗坏血酸的作用是_______ ,也可以用Na2SO3代替抗坏血酸,其原理是_______ (用离子方程式表示)。
(3)步骤IV过滤用到的玻璃仪器除烧杯外还有_______ 。
(4)步骤V检验LiFePO4是否洗涤干净的方法是_______ 。
(5)干燥后称量,产品的质量是1.2 g,本实验的产率为_______ %(保留小数点后1位)。

I.在A中加入40 mL蒸馏水、0.01 mol H3PO4和0.01 mol FeSO4·7H2O,用搅拌器搅拌溶解后,缓慢加入0.03 mol LiOH·H2O,继续搅拌。
II.向反应液中加入少量抗坏血酸(即维生素C),继续搅拌5min。
III.快速将反应液装入反应釜中,保持170℃恒温5 h。
IV.冷却至室温,过滤。
V.用蒸馏水洗涤沉淀。
VI.干燥,得到磷酸亚铁锂产品。
回答下列问题:
(1)装置图中仪器A的名称是
A.100mL B.250mL C.500mL D.1000mL
(2)步骤II中,抗坏血酸的作用是
(3)步骤IV过滤用到的玻璃仪器除烧杯外还有
(4)步骤V检验LiFePO4是否洗涤干净的方法是
(5)干燥后称量,产品的质量是1.2 g,本实验的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有一瓶澄清溶液,可能含有 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、
、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、 、
、 、
、 中的一种或几种。取该溶液进行以下实验:
中的一种或几种。取该溶液进行以下实验:
①用pH试纸检验,表明溶液呈强酸性;
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色;
③另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性变为碱牲,在滴加过程中先生成白色沉淀后完全溶解;取部分碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
④另取部分③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
根据以上实验事实回答下列问题:
(1)该溶液中肯定存在的离子是___________________ ,肯定不存在的离子是________ ;
(2)步骤③加入NaOH溶液过程中先生成白色沉淀后完全溶解的离子方程式为_______ 。
 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、
、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、 、
、 、
、 中的一种或几种。取该溶液进行以下实验:
中的一种或几种。取该溶液进行以下实验:①用pH试纸检验,表明溶液呈强酸性;
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色;
③另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性变为碱牲,在滴加过程中先生成白色沉淀后完全溶解;取部分碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
④另取部分③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
根据以上实验事实回答下列问题:
(1)该溶液中肯定存在的离子是
(2)步骤③加入NaOH溶液过程中先生成白色沉淀后完全溶解的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】Ⅰ.某无色透明溶液可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,现进行如下实验:
中的几种,现进行如下实验:
①滴加 溶液,有白色沉淀产生,将沉淀滤出。
溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,沉淀部分溶解。
③向①滤液加入 溶液,有白色沉淀生成,该沉淀不溶于稀
溶液,有白色沉淀生成,该沉淀不溶于稀 。
。
(1)试判断:该溶液中肯定有_____ ,肯定没有_____ ,可能有_____ (填离子符号)。
(2)写出步骤②发生反应的离子方程式_____ 。
(3)若要检验溶液中可能存在的离子是否存在,可以进行的实验操作为_____ 。
Ⅱ.某溶液中含有较大量的 、
、 、
、 ,如果只取一次该溶液就能够分别将3种阴离子依次检验出来:
,如果只取一次该溶液就能够分别将3种阴离子依次检验出来:
(4)下列实验操作顺序正确的是_____ 。(填写序号,可重复使用)
①滴加 溶液②过滤③滴加
溶液②过滤③滴加 溶液④滴加
溶液④滴加 溶液
溶液
 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,现进行如下实验:
中的几种,现进行如下实验:①滴加
 溶液,有白色沉淀产生,将沉淀滤出。
溶液,有白色沉淀产生,将沉淀滤出。②向上述沉淀中加入足量的稀硝酸,沉淀部分溶解。
③向①滤液加入
 溶液,有白色沉淀生成,该沉淀不溶于稀
溶液,有白色沉淀生成,该沉淀不溶于稀 。
。(1)试判断:该溶液中肯定有
(2)写出步骤②发生反应的离子方程式
(3)若要检验溶液中可能存在的离子是否存在,可以进行的实验操作为
Ⅱ.某溶液中含有较大量的
 、
、 、
、 ,如果只取一次该溶液就能够分别将3种阴离子依次检验出来:
,如果只取一次该溶液就能够分别将3种阴离子依次检验出来:(4)下列实验操作顺序正确的是
①滴加
 溶液②过滤③滴加
溶液②过滤③滴加 溶液④滴加
溶液④滴加 溶液
溶液
您最近一年使用:0次



