向含0.02mol Al3+的明矾溶液中逐滴加入0.2mol/L的Ba(OH)2溶液时,测得产生沉淀的质量m和逐滴加入Ba(OH)2溶液的体积V的关系如下图,试填写空白:
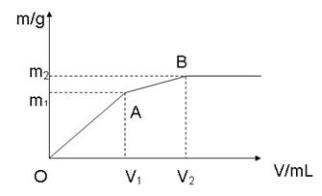
(1)写出OA段反应的离子方程式:OA_______________________ ;
(2)m1=________________ V1=_______________ ;m2=_______________ V2=_________________

(1)写出OA段反应的离子方程式:OA
(2)m1=
10-11高三上·湖南长沙·阶段练习 查看更多[1]
(已下线)2010年湖南省长沙一中高三上学期第三次月考化学试题
更新时间:2010-10-09 11:38:24
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)2 mol O3和3 mol O2的质量之比________ ,体积之比________ .
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是________ X的相对原子质量是________ .
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】I.现有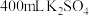 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗
溶液,至恰好不再产生沉淀,消耗 ,将沉淀过滤、洗涤、干燥,称其质量为
,将沉淀过滤、洗涤、干燥,称其质量为 ;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了
;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了 。试计算:
。试计算:
(1)
_______ 。
(2)则原溶液中 的物质的量浓度为
的物质的量浓度为_______ 
II.某化工厂以某种黄铁矿(含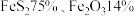 、不反应杂质
、不反应杂质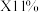 )为原料生产硫酸。黄铁矿与氧气反应的方程式为
)为原料生产硫酸。黄铁矿与氧气反应的方程式为 。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
(1)假设生产过程中硫的损失为零,理论上每天可以制得98%的浓硫酸_______ 吨。
(2)假设煅烧后得到的固体只含有 和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁_______ 吨。(写出计算过程)
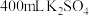 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗
溶液,至恰好不再产生沉淀,消耗 ,将沉淀过滤、洗涤、干燥,称其质量为
,将沉淀过滤、洗涤、干燥,称其质量为 ;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了
;向另一份溶液中加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了 。试计算:
。试计算:(1)

(2)则原溶液中
 的物质的量浓度为
的物质的量浓度为
II.某化工厂以某种黄铁矿(含
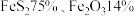 、不反应杂质
、不反应杂质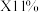 )为原料生产硫酸。黄铁矿与氧气反应的方程式为
)为原料生产硫酸。黄铁矿与氧气反应的方程式为 。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:
。若该厂每天煅烧这种矿石100吨,煅烧后得到固体75吨。试计算:(1)假设生产过程中硫的损失为零,理论上每天可以制得98%的浓硫酸
(2)假设煅烧后得到的固体只含有
 和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
和不反应杂质X,若用来炼铁,理论上每天能得到含碳4%的生铁
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将5.405gX中Cr元素全部氧化成Cr2O ,酸性的Cr2O
,酸性的Cr2O 可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O
可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O 被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。
被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。
(1)写出Cr2O 与I-反应的离子方程式
与I-反应的离子方程式__________________
(2)通过计算得出X的化学式__________________
 ,酸性的Cr2O
,酸性的Cr2O 可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O
可与过量的KI发生氧化还原反应氧化出7.62g I2,同时Cr2O 被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。
被还原成Cr3+,如果取溶有X 5.405g的溶液,加入过量的AgNO3,可得12.915gAgCl沉淀。(1)写出Cr2O
 与I-反应的离子方程式
与I-反应的离子方程式(2)通过计算得出X的化学式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取20mL硫酸和盐酸的混合液体,加入过量的氯化钡溶液,产生4.66g白色沉淀,然后继续向溶液中加入ag(足量)铁粉,产生的气体的体积为896mL(标准状况下)。
(1)写出上述过程中发生的离子方程式_______________________________________
________________________________________________________________________ 。
(2)计算原混合液体中,硫酸物质的量浓度是_________________ mol/L,盐酸物质的量浓度是_____________________ mol/L(写出计算过程)。
(1)写出上述过程中发生的离子方程式
(2)计算原混合液体中,硫酸物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】现有四种溶液:A.盐酸B.稀硫酸C.NaOH溶液D.Ba(OH)2溶液。这些溶液溶质物质的量浓度均为0.3mol/L。根据溶液取用情况,判断得到的溶液中存在的主要离子及其浓度;或者根据最终离子的情况,推断最终溶液可能是哪些溶液按怎样的体积比混合的结果(忽略溶液混合后的体积变化)
| 溶液取用情况 | 溶液中存在的主要离子及其浓度 |
| 溶液A和B按体积比2:1混合 | ① |
| ② | Na+和Cl﹣物质的量浓度均为0.15 mol/L |
| 等体积混合溶液B和C | ③ |
| 溶液A和D按体积比2:1混合 | ④ |
| ⑤ | Ba2+物质的量浓度为0.1 mol/L,OH﹣物质的量浓度为0.2 mol/L |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】天然碱的组成可以用aNa2CO3·bNaHCO3·cH2O(a、b、c为整数)表示。现有2种不同的天然碱样品,分别进行如下实验以确定其化学式。
(1)将质量为62.0 g的样品A平均分成两份,一份在300℃下充分灼烧(Na2CO3不分解),固体质量减轻9.8g;另一份溶于水后加入足量的Ba(OH)2溶液,得到白色沉淀59.1 g。样品A的化学式可以表示为_____ ;
(2)将质量为4.71 g的样品B溶于水,逐滴滴加一定浓度的稀盐酸,产生气体的质量与加入盐酸的质量有下表所示关系:
【已知在盐酸不足时会发生反应:Na2CO3 + HCl = NaHCO3 + NaCl + H2O 】
盐酸的质量分数为_______ ;样品B的化学式可以表示为________ 。
(1)将质量为62.0 g的样品A平均分成两份,一份在300℃下充分灼烧(Na2CO3不分解),固体质量减轻9.8g;另一份溶于水后加入足量的Ba(OH)2溶液,得到白色沉淀59.1 g。样品A的化学式可以表示为
(2)将质量为4.71 g的样品B溶于水,逐滴滴加一定浓度的稀盐酸,产生气体的质量与加入盐酸的质量有下表所示关系:
| 盐酸质量/g | 20 | 40 | 60 | 80 |
| 气体质量/g | 0 | 0.44 | 1.32 | 1.98 |
【已知在盐酸不足时会发生反应:Na2CO3 + HCl = NaHCO3 + NaCl + H2O 】
盐酸的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)钠、镁、铝与1mol·L-1的盐酸100mL反应,在相同条件下产生氢气的体积相同,则消耗钠、镁、铝的物质的量比为______ 。等物质的量的Na2CO3和NaHCO3与足量的盐酸反应,在相同条件下产生二氧化碳的体积之比是__________ 。
(2)把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是__________ 。
(3)向30毫升1 mol/L的AlCl3溶液中逐渐加入浓度为2 mol/L的NaOH溶液,若产生0.78克白色沉淀,则加入的NaOH溶液的体积可能为__________ 毫升。
(4)某溶液中含有下列六种离子:①HCO3- ②SO32- ③K+ ④CO32- ⑤NH4+ ⑥NO3-,向其中加入稍过量Na2O2后,溶液中离子浓度基本保持不变的是( )
A. ③⑥ B. ④⑥ C. ③④⑥ D. ①②⑤
(2)把Ba(OH)2溶液滴入明矾溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是
(3)向30毫升1 mol/L的AlCl3溶液中逐渐加入浓度为2 mol/L的NaOH溶液,若产生0.78克白色沉淀,则加入的NaOH溶液的体积可能为
(4)某溶液中含有下列六种离子:①HCO3- ②SO32- ③K+ ④CO32- ⑤NH4+ ⑥NO3-,向其中加入稍过量Na2O2后,溶液中离子浓度基本保持不变的是
A. ③⑥ B. ④⑥ C. ③④⑥ D. ①②⑤
您最近一年使用:0次

 ,该金属的相对原子质量为
,该金属的相对原子质量为


