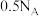某氯化镁溶液的密度为1.1g/cm3,其中镁离子的质量分数为2.4%,300mL该溶液中Cl-离子的物质的量约等于
| A.1.5mol | B.1.32mol | C.0.66mol | D.0.33mol |
10-11高三上·福建·期中 查看更多[1]
(已下线)2011届福建师大附中高三上学期期中考试化学卷
更新时间:2016-12-09 01:06:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 的盐酸浴液中的 的盐酸浴液中的 离子数目为NA 离子数目为NA |
| B.常温常压下,11.2L氧气中Cl原子数目为NA |
C. 中的 中的 数目为NA 数目为NA |
D.400gNaOH溶解在1L蒸馏水中,所得溶液每100mL中的 数目为NA个 数目为NA个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各组物质中,分子数相同的是
| A.2L SO2和2L CO2 | B.9g水和标准状况下11.2L CO2 |
| C.标准状况下1mol氧气和22.4L 水 | D.0.1 mol氢气和2.24L氯化氢气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.4.4gCO2和N2O的混合气体中含有的原子总数为0.3NA |
| B.物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |
| C.标准状况下,33.6L氯仿(CHCl3)中含有氯原子的数目为4.5NA |
| D.10mL12mol/L盐酸与足量MnO2加热反应,制得Cl2的分子数为0.03NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于0.1mol·L-1 Na2CO3溶液的叙述错误的是( )
| A.0.5 L该溶液中,Na+的物质的量浓度为0.2mol·L-1 |
| B.1 L该溶液中,含CO32—的数目小于0.1NA(NA是阿伏加 德罗常数) |
| C.从1 L该溶液中取出100 mL,则取出的溶液中Na2CO3的物质的量浓度为0.01mol·L-1 |
| D.取该溶液10 mL,加水稀释至100 mL后,Na2CO3的物质的量浓度为0.01mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.常温常压下,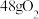 与 与 的混合气体中含有的原子总数为 的混合气体中含有的原子总数为 |
B.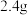 金属镁变成镁离子时失去的电子数为 金属镁变成镁离子时失去的电子数为 |
C.标准状况下, 水中所含电子的数目为 水中所含电子的数目为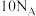 |
D.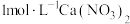 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某一 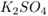 和
和 的混合溶液,已知其中
的混合溶液,已知其中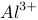 的物质的量浓度为0.4
的物质的量浓度为0.4 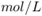 ,
,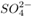 的物质的量浓度为0.7
的物质的量浓度为0.7 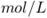 ,则此溶液中
,则此溶液中 的物质的量浓度为
的物质的量浓度为
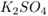 和
和 的混合溶液,已知其中
的混合溶液,已知其中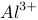 的物质的量浓度为0.4
的物质的量浓度为0.4 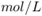 ,
,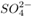 的物质的量浓度为0.7
的物质的量浓度为0.7 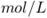 ,则此溶液中
,则此溶液中 的物质的量浓度为
的物质的量浓度为A.0.1  | B.0.15 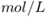 |
C.0.2 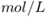 | D.0.25 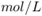 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于物质的量浓度表述错误的是
| A.将0.5mol/LCaCl2溶液10mL加水稀释至100mL,所得溶液的c(Cl-)为0.1mol/L |
| B.将10mL1mol·L-1的H2SO4稀释成0.1mol·L-1的H2SO4,可向其中加入100mL水 |
| C.T℃时,50mLcmol/L的NaNO3饱和溶液蒸发掉10g水,冷却到T℃时,其体积小于50mL,它的物质的量浓度仍为cmol/L |
| D.20℃时,0.023mol·L-1的氢氧化钙饱和溶液100mL加入5g生石灰,冷却到20℃时,其体积小于100mL,它的物质的量浓度仍为0.023mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列方程式书写正确的是
| A.NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++HSO4- |
| B.H2SO4溶液与NaOH溶液发生中和反应的热化学方程式为(已知H2SO4 溶液与NaOH溶液发生反应的中和热为57.3 kJ/mol):H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H=-57.3kJ/mol |
C.CO32-的水解方程式:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| D.CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质在水溶液中的电离方程式书写正确的是
A. | B. |
C. | D.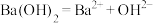 |
您最近一年使用:0次

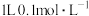 的碳酸钠溶液中,氧原子总数为
的碳酸钠溶液中,氧原子总数为
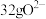 中所含电子的数目为
中所含电子的数目为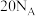
 的
的 溶液中,含有
溶液中,含有 个数为
个数为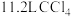 中含有分子的数目为
中含有分子的数目为