为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
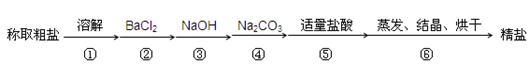
(1)按照该同学设计的实验步骤,并不能得到精盐,原因在于步骤中少了一个操作,该操作是_______ ,应加在_____ 和____ 之间。
(2)判断BaCl2已过量的方法是( )
(3)写出④中相应的离子方程式__________________ ,______________ 。
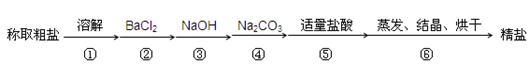
(1)按照该同学设计的实验步骤,并不能得到精盐,原因在于步骤中少了一个操作,该操作是
(2)判断BaCl2已过量的方法是
| A.取②后的上层清液少许放入试管中,再滴入几滴Na2SO4溶液,若溶液未变浑浊,则证明BaCl2已过量。 |
| B.取②后的上层清液少许放入试管中,再滴入几滴BaCl2溶液,若溶液未变浑浊,则证明BaCl2已过量。 |
| C.取②后的上层清液少许放入试管中,再滴入几滴AgNO3溶液,若溶液变浑浊,则证明BaCl2已过量。 |
| D.取②后的上层清液少许放入试管中,再滴入几滴BaCl2溶液,若溶液变浑浊,则证明BaCl2已过量。 |
(3)写出④中相应的离子方程式
10-11高一上·重庆万州·阶段练习 查看更多[1]
(已下线)2010年重庆市万州二中高一12月月考化学试卷
更新时间:2016/12/09 01:23:49
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】孔雀石的主要成分为Cu2(OH)2CO3,还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:

(1)试剂A的化学式是_____________ ;操作Ⅰ的名称是______________ ;
(2)生成气体X的化学方程式为:_________________________________ 。
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用_________
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)已知:
① 试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用__________ :
② 为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为__________ 。
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)________________________ 。

(1)试剂A的化学式是
(2)生成气体X的化学方程式为:
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
(4)已知:
| 物质 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.8 |
| 完全沉淀时的pH | 3.7 | 6.7 |
① 试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用
A.稀硫酸 B.NaOH溶液 C .氨水 D.CuO
② 为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】海洋是巨大的资源宝库,大部分的镁是从海水中提取的。某课题小组模拟工业海水提取镁的工艺流程,设计了如图所示的方案:
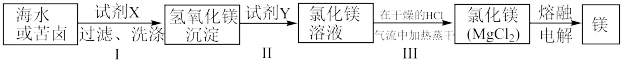
已知:①海水和苦卤中都含有NaCl、Na2SO4、MgCl2、CaCl2等;
②苦卤是海水晒盐后剩余的溶液;
③如表所示为某品牌不同碱的价格:
回答下列问题:
(1)工业生产的第1步操作中,试剂X选用表格中Ca(OH)2的原因是___________ 。
(2)根据海水或苦卤的成分,为除去其中的杂质得到NaCl,可采取的措施如下:
①加入过量的Na2CO3溶液
②加入过量的BaCl2溶液
③加入过量的NaOH溶液
④过滤除去沉淀,再加入适量的盐酸
操作顺序为___________ (填序号)。
(3)第II步操作中发生反应的离子方程式为___________ 。
(4)电解过程需要直流电源,与直流电源___________ (填“正”或“负”)极相连的电极产生Mg,每产生12kgMg,在另一极产生气体的体积为___________ L(标准状况)。
(5)MgCl2溶液直接蒸干得不到无水MgCl2,用平衡移动的原理解释原因___________ ,而将SOCl2与MgCl2·6H2O混合并加热,可得到无水MgCl2,写出SOCl2与MgCl2·6H2O总反应的化学方程式___________ 。
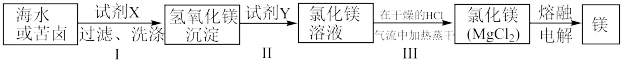
已知:①海水和苦卤中都含有NaCl、Na2SO4、MgCl2、CaCl2等;
②苦卤是海水晒盐后剩余的溶液;
③如表所示为某品牌不同碱的价格:
| 试剂 | NaOH | Ca(OH)2 | Ba(OH)2 | KOH |
| 价格(元/吨) | 2400 | 850 | 5300 | 5500 |
(1)工业生产的第1步操作中,试剂X选用表格中Ca(OH)2的原因是
(2)根据海水或苦卤的成分,为除去其中的杂质得到NaCl,可采取的措施如下:
①加入过量的Na2CO3溶液
②加入过量的BaCl2溶液
③加入过量的NaOH溶液
④过滤除去沉淀,再加入适量的盐酸
操作顺序为
(3)第II步操作中发生反应的离子方程式为
(4)电解过程需要直流电源,与直流电源
(5)MgCl2溶液直接蒸干得不到无水MgCl2,用平衡移动的原理解释原因
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为________________ 。
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为________ 。
(3)从理论上考虑,,下列物质也能吸收Br2的是___ (填标号)。
A H2O B NaCl溶液C NaSO3溶液 D FeCl3溶液
(4)查阅资料知,Br2的沸点为58.8℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是_____ 。

(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(3)从理论上考虑,,下列物质也能吸收Br2的是
A H2O B NaCl溶液C NaSO3溶液 D FeCl3溶液
(4)查阅资料知,Br2的沸点为58.8℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】通过海水晾晒可得粗盐,粗盐中除含有 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。制备精盐的各步操作流程如下:
以及泥沙等杂质。制备精盐的各步操作流程如下:
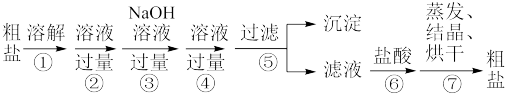
(1)第②、④步操作中需要加入的试剂依次是___________ (填化学式)。
(2)在第③步操作中,不能将除杂试剂改为 溶液,原因是
溶液,原因是___________ 。
(3)第⑤步操作中,需要的玻璃仪器有___________ 。
(4)第⑥步操作的目的是___________ 。
(5)在蒸发过程中要用玻璃棒搅拌,目的是___________ 。
 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。制备精盐的各步操作流程如下:
以及泥沙等杂质。制备精盐的各步操作流程如下:
(1)第②、④步操作中需要加入的试剂依次是
(2)在第③步操作中,不能将除杂试剂改为
 溶液,原因是
溶液,原因是(3)第⑤步操作中,需要的玻璃仪器有
(4)第⑥步操作的目的是
(5)在蒸发过程中要用玻璃棒搅拌,目的是
您最近一年使用:0次
【推荐2】海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
(1)步骤③和⑤的实验操作名称分别是________________ 、____________ 。
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是________ ,该装置的操作名称为__________ 。___________________________ 。
(4)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘:______ 。

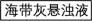

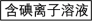



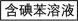
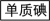
(1)步骤③和⑤的实验操作名称分别是
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是
(4)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘:
您最近一年使用:0次
【推荐3】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)除去自来水中的Ca2+、Mg2+、Cl—、SO42—等杂质,选择装置_____________ (填代表装置图的字母)。
(2)用CCl4萃取碘水中的I2,有机层的颜色为___________________ 。
(3)装置A中①的名称是_____________ ,进水的方向是_____________ 。装置B在分液时为使液体顺利滴下,应进行的具体操作是_____________ 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液; ③加入过量的NaOH溶液;④调节溶液的pH等于7; ⑤溶解; ⑥过滤;⑦蒸发。
正确的操作顺序是_____________ (填写字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤③②①⑥④⑦ d.⑤②①③④⑥⑦
问题2:由海水到氯化钠晶体的实验过程中要用到的主要装置是_____________ (从给定的四种装置中选择,填字母)。

(1)除去自来水中的Ca2+、Mg2+、Cl—、SO42—等杂质,选择装置
(2)用CCl4萃取碘水中的I2,有机层的颜色为
(3)装置A中①的名称是
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

问题1:粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液; ③加入过量的NaOH溶液;④调节溶液的pH等于7; ⑤溶解; ⑥过滤;⑦蒸发。
正确的操作顺序是
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤③②①⑥④⑦ d.⑤②①③④⑥⑦
问题2:由海水到氯化钠晶体的实验过程中要用到的主要装置是
您最近一年使用:0次



