海带含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
(1)步骤③和⑤的实验操作名称分别是________________ 、____________ 。
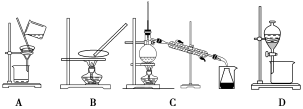
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是________ ,该装置的操作名称为__________ 。___________________________ 。
(4)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘:______ 。





(1)步骤③和⑤的实验操作名称分别是
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤应选择的实验装置是
(4)请设计一个简单的实验方案,检验提取碘后的水溶液中是否还含有单质碘:
更新时间:2018/09/08 16:32:16
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
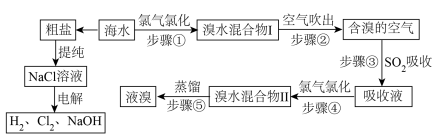
【推荐1】天然海水中含有非常丰富的化学元素,具有很大的利用价值。工业上对海水资源综合利用的部分工艺流程如下图所示。
(1)请列举海水淡化的两种方法:________________ 、________________ 。
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入少量二氧化碳发生反应的离子方程式________________________ 。
(3)海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如上图。步骤①反应的离子方程式是_________ ;步骤③通入二氧化硫的目的是_____________ ,其反应的化学方程式是______________ 。
(4)步骤⑤蒸馏的过程中,温度应控制在80-90℃。温度过高或过低都不利于生产,请解释其原因:___________________________ 。

(1)请列举海水淡化的两种方法:
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入少量二氧化碳发生反应的离子方程式
(3)海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如上图。步骤①反应的离子方程式是
(4)步骤⑤蒸馏的过程中,温度应控制在80-90℃。温度过高或过低都不利于生产,请解释其原因:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】我国科学家侯德榜发明了联合制碱法。联合以氯化钠、氨及二氧化碳为原料,同时生产纯碱和氯化铵两种产品,又称“侯氏制碱法”,对世界制碱工业做出了卓越贡献。下列是制备纯碱的工艺流程,回答下列问题。
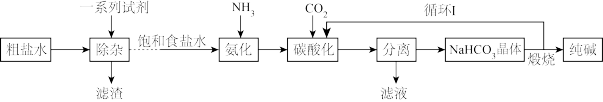
(1)写出实验室用NH4Cl固体和Ca(OH)2固体制备NH3的化学方程式___________ ;
(2)粗盐水中含大量 、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3提纯NaCl。用离子方程式说明加入Na2CO3的目的
、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3提纯NaCl。用离子方程式说明加入Na2CO3的目的___________ 。要证明提纯后的食盐水中没有 ,取样后先加
,取样后先加___________ (填名称,下同),再加___________ 。
(3)若在实验室中进行“分离”操作的名称___________ 。
(4)循环Ⅰ中参与循环的物质是___________ 。
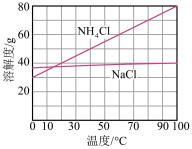
(5)向滤液中加入NaCl粉末,存在NaCl(固体)+NH4Cl(溶液)→NaCl(溶液)+NH4Cl(固体)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。

(1)写出实验室用NH4Cl固体和Ca(OH)2固体制备NH3的化学方程式
(2)粗盐水中含大量
 、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3提纯NaCl。用离子方程式说明加入Na2CO3的目的
、Mg2+,“除杂”时依次加入过量的NaOH、BaCl2、Na2CO3提纯NaCl。用离子方程式说明加入Na2CO3的目的 ,取样后先加
,取样后先加(3)若在实验室中进行“分离”操作的名称
(4)循环Ⅰ中参与循环的物质是
(5)向滤液中加入NaCl粉末,存在NaCl(固体)+NH4Cl(溶液)→NaCl(溶液)+NH4Cl(固体)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】某厂废水中含5.00×10-3mol·L-1的Cr2O ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价有+3,+2),设计了如下实验流程:
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价有+3,+2),设计了如下实验流程:

(1)第①步反应的离子方程式是__________________________________________
(2)第②步中用pH试纸测定溶液pH的操作是______________________________
(3)用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,铁变为______________ ,加碱调节至pH为________ 时,铁元素刚好沉淀完全(离子浓度小于1×10-5mol·L-1时,即可认为该离子沉淀完全);继续加碱至pH为________ 时,锌开始沉淀(假定Zn2+浓度为0.1 mol·L-1)。若上述过程不加H2O2后果是______________________ ,原因是________________________________________________ 。
 ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价有+3,+2),设计了如下实验流程:
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价有+3,+2),设计了如下实验流程:
(1)第①步反应的离子方程式是
(2)第②步中用pH试纸测定溶液pH的操作是
(3)用废电池的锌皮制备ZnSO4·7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是加稀H2SO4和H2O2溶解,铁变为
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行以下实验:
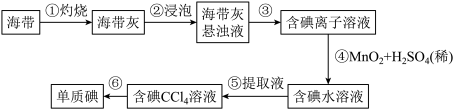
请填写下列空白:
(1)CCl4是____ 色、比水____ 的液体。步骤⑤后静置,下层液体的颜色为______ 色,上层液体的成分为___________ 。该步骤所用主要玻璃仪器的名称是__________ 。
(2)能选用CCl4获取碘的原因是_____________________ 、___________________ 、_______

请填写下列空白:
(1)CCl4是
(2)能选用CCl4获取碘的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】碘在工农业生产和日常生活中有重要用途。
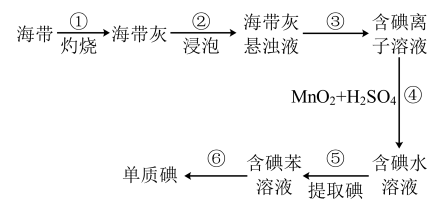
(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_____________ (从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
步骤④发生反应的离子方程式为____________________________________ 。
(2)若步骤⑤采用裂化汽油提取碘,后果是__________________________ 。
(3)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为:IBr+H2O=HBr+HIO等,下列有关IBr的叙述中错误的是( ) 。
(4)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的碘以碘酸钾(KIO3)存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,下列说法正确的是( ) 。

(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
步骤④发生反应的离子方程式为
(2)若步骤⑤采用裂化汽油提取碘,后果是
(3)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为:IBr+H2O=HBr+HIO等,下列有关IBr的叙述中错误的是
| A.固体溴化碘熔沸点较高 |
| B.在许多反应中,溴化碘是强氧化剂 |
| C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂 |
| D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O |
| A.碘易溶于有机溶剂,可用酒精萃取碘水中的I2 |
B.检验加碘盐原理: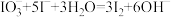 |
| C.在KIO3溶液中加入几滴淀粉溶液,溶液变蓝色 |
| D.向某无色溶液中加入氯水和四氯化碳,振荡,静置,下层呈紫色,说明原溶液中有I— |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】海洋植物如:海带、海藻中含有丰富的碘元素,碘元素经过灼烧之后以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:

某化学兴趣小组将上述流程②③设计成如下流程:
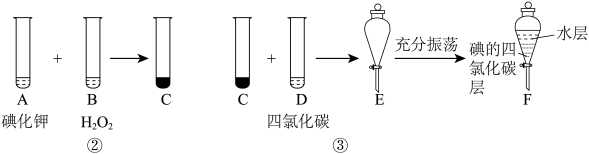
已知:实验②中发生反应的离子方程式:2I-+ H2O+2H+=2H2O+I2。回答下列问题:
(1)写出提取流程中实验③的操作名称:_____ ,从E到F的正确操作方法为:_______ ,实验①的操作为过滤,如果滤液仍然浑浊应该采取的措施是:___ .
(2)从F的下层液体中得到固态碘单质还需要进行的操作是:____ 。
(3)当实验②中的反应转移的电子数为2.408×1023时,理论上可以提取___ mol I2。

某化学兴趣小组将上述流程②③设计成如下流程:

已知:实验②中发生反应的离子方程式:2I-+ H2O+2H+=2H2O+I2。回答下列问题:
(1)写出提取流程中实验③的操作名称:
(2)从F的下层液体中得到固态碘单质还需要进行的操作是:
(3)当实验②中的反应转移的电子数为2.408×1023时,理论上可以提取
您最近一年使用:0次



