在CaCO3、CO2、CO、Na2CO3、NaHCO3、Cl2物质中
⑴大气中过多会造成温室效应的是_______________ .
⑵俗名是小苏打,且是制糕点发酵粉的主要成分的是________
⑶能和血液中血红蛋白结合而使人中毒的是_________________
⑷是水垢的主要成分_______________
⑸能用于制造漂白粉的是__________________
⑹俗名是纯碱,工业上用于造纸业的是___________
⑴大气中过多会造成温室效应的是
⑵俗名是小苏打,且是制糕点发酵粉的主要成分的是
⑶能和血液中血红蛋白结合而使人中毒的是
⑷是水垢的主要成分
⑸能用于制造漂白粉的是
⑹俗名是纯碱,工业上用于造纸业的是
10-11高一上·福建厦门·阶段练习 查看更多[3]
(已下线)2010—2011年福建省厦门市杏南中学高一12月月考化学卷天津市第一中学2020-2021高一上学期期中考试化学试题天津市外国语大学附属外国语学校2022~2023学年高一上学期阶段性检测化学试题
更新时间:2016-12-09 01:27:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=___________ 时杀菌效果强。
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是________ ;在使用时也不能与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为_______ 。
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为∶ ,X的化学式为
,X的化学式为_________ ,每生成1molClO2,反应中转移电子___________ mol。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为∶
 ,X的化学式为
,X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中 Cl2(aq)、HClO和 ClO-的物质的量分数(a)随pH变化的关系如图所示。
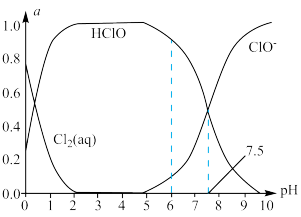
由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=___________ 时杀菌效果强,当pH=7.5时,氯水中含氯元素的微粒有 HClO、ClO-和___________ 。
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是___________ ;在使用时也不能与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为___________ 。
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为∶2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2CO2+2H2O ,每生成 1 mol ClO2,反应中转移电子___________ mol。
②在进行饮用水消毒时,ClO2可转化为Cl-,1 mol ClO2与___________ g(保留两位小数)NaClO氧化消毒能力相当(用得电子数目多少衡量氧化消毒能力强弱)。
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气-氯水体系,该体系中 Cl2(aq)、HClO和 ClO-的物质的量分数(a)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是
(3)ClO2是国际上公认的高效、安全的杀菌消毒剂。
①工业制备ClO2的反应原理为∶2KClO3+H2C2O4+H2SO4=K2SO4+2ClO2+2CO2+2H2O ,每生成 1 mol ClO2,反应中转移电子
②在进行饮用水消毒时,ClO2可转化为Cl-,1 mol ClO2与
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,保护水资源人人有责。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为_______ 。
(2)反应中高铁酸钠是_______ 产物(填“氧化”或“还原”)。
(3)写出制备高铁酸钠的离子方程式_______ 。
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称_______ 。
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。
(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于_______ 变化(填“物理”或“化学”)。
(6)在溶液中Cr2O 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应_______ 氧化还原反应(填“属于”或“不属于”)。
(7)写出处理工业酸性废水时发生反应的离子方程式_______ 。
Ⅰ.高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法是:在强碱性条件下,NaClO溶液和FeCl3溶液反应生成高铁酸钠和氯化钠。
(1)高铁酸钠中铁元素的化合价为
(2)反应中高铁酸钠是
(3)写出制备高铁酸钠的离子方程式
(4)使用氯气对自来水消毒时,氯气与水中的有机物反应生成对人体有害的物质,人们开始使用新的自来水消毒剂,如氯元素的某种氧化物,写出这种新消毒剂的名称
Ⅱ.工业酸性废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,将Cr2O 转化为Cr3+。
转化为Cr3+。(5)绿矾是结晶水合物,风化是指在室温和干燥的空气里,结晶水合物失去结晶水的现象,则风化属于
(6)在溶液中Cr2O
 存在反应:Cr2O
存在反应:Cr2O +H2O⇌2CrO
+H2O⇌2CrO +2H+,该反应
+2H+,该反应(7)写出处理工业酸性废水时发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与我们的生活、生产、环境、资源利用等息息相关。回答下列问题:
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是_______ ,会造成酸雨的物质是_______ ,会导致光化学烟雾的物质是_______ 。
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式_______ 。
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是_______ (填化学式)。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl—形式存在。现要消毒1.00 m3生活污水,分别用Cl2和ClO2来消毒处理,所耗Cl2与ClO2的质量比值为 _______ (保留小数点后2位)。
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84”消毒液,可以说化学让生活更美好。图为“84”消毒液说明书。请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按53.25g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式_______ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为_______ ,从氧化还原角度分析Cl2表现了______ 性。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是______ (用离子方程式表达)。(已知:酸性:H2CO3>HClO>HCO ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会_______ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的_____ 。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1:200水溶液餐饮具,瓜果等1:100水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按53.25g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
 ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题
(1)铜在潮湿的空气中易出绿花,后者的常见化学式为:___________ 。侯氏制碱法最终制得的“碱”的化学式为:___________ 。
(2)用化学方程式表示漂白粉漂白作用(在空气中)原理:___________ 。
(3)用化学方程式表示炽热的铁水不能注入潮湿的模具中的原因:___________ 。
(4)用氢氧化铝或小苏打消除胃酸过多的离子方程式依次为:___________ 。
(1)铜在潮湿的空气中易出绿花,后者的常见化学式为:
(2)用化学方程式表示漂白粉漂白作用(在空气中)原理:
(3)用化学方程式表示炽热的铁水不能注入潮湿的模具中的原因:
(4)用氢氧化铝或小苏打消除胃酸过多的离子方程式依次为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Na2CO3、NaHCO3是生活中常见的盐,某实验小组通过以下实验探究这两种物质的性质。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,_______ 。
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。
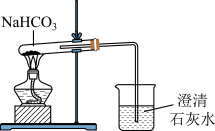
①试管中发生的化学反应方程式为_______ 。
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)_______ 。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_______ 。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为_______ 。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。

①试管中发生的化学反应方程式为
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】二氧化碳的循环对生活、生产和环境有着重要的影响。
Ⅰ、传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生 ,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入
,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入 可调节面团酸度。
可调节面团酸度。
(1)等质量的碳酸钠和碳酸氢钠,消耗酸更多的是______ 。
(2)若面团发得不好,面团内的气孔少,会略有酸味。厨师会选择向面团中添加 ,而不再用
,而不再用 ,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加
,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加 的两个作用
的两个作用______ 。
(3)已知磷的含氧酸盐难分解,复合膨松剂发酵的效果更明显。某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂(防止膨松剂分解、吸潮结块而失效)。推测焦磷酸二氢二钠的作用是______ 。
Ⅱ、二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
(4)科学家设计出烧碱溶液捕捉 法,原理如图所示
法,原理如图所示
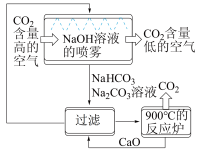
①该过程中能实现NaOH溶液再生的反应为 和
和______ 。
②若喷洒完100mL5mol/L的NaOH溶液后,测得吸收液中的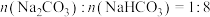 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为______ L。
③下列溶液中,也能用作“捕捉”二氧化碳试剂的是______ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸
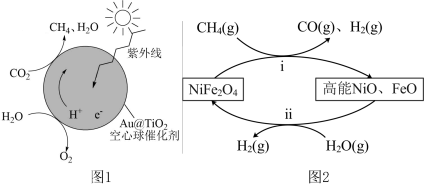
(5)Au@ 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图1所示。制得的甲烷(
封存和能量储存双重效果,其原理如图1所示。制得的甲烷( )通过两步法可制取
)通过两步法可制取 ,原理如图2所示。
,原理如图2所示。
①已知 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的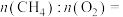
______ 。
②若不考虑过程中原料损失,则16g 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为______ mol。
Ⅰ、传统蒸馒头常采用酵头发面,酵头可使面团在微生物作用下产生
 ,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入
,从而使面团疏松,同时生成乳酸和醋酸等酸性物质,再加入 可调节面团酸度。
可调节面团酸度。(1)等质量的碳酸钠和碳酸氢钠,消耗酸更多的是
(2)若面团发得不好,面团内的气孔少,会略有酸味。厨师会选择向面团中添加
 ,而不再用
,而不再用 ,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加
,继续揉面后,上锅蒸也能蒸出松软的馒头。请解释添加 的两个作用
的两个作用(3)已知磷的含氧酸盐难分解,复合膨松剂发酵的效果更明显。某品牌复合膨松剂的说明书如图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂(防止膨松剂分解、吸潮结块而失效)。推测焦磷酸二氢二钠的作用是
| 【名称】xx复合膨松剂 【保质期】24个月 【净含量】1kg 【使用量】面粉用量的0.5%~2.5% 【配料】碳酸氢钠、焦磷酸二氢二钠、碳酸钙、葡萄糖酸-δ-内酯、淀粉 【适用范围】适用于各类馒头、包子等发酵面制品以及面包、糕点等的制作 【保存方法】阴凉干燥处存储 |
Ⅱ、二氧化碳的捕捉与封存是未来实现低碳经济转型的重要途径。
(4)科学家设计出烧碱溶液捕捉
 法,原理如图所示
法,原理如图所示
①该过程中能实现NaOH溶液再生的反应为
 和
和②若喷洒完100mL5mol/L的NaOH溶液后,测得吸收液中的
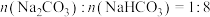 ,则被吸收的
,则被吸收的 在标况下的体积为
在标况下的体积为③下列溶液中,也能用作“捕捉”二氧化碳试剂的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.稀硫酸
溶液 D.稀硫酸(5)Au@
 蛋黄型空心球催化剂技术实现了
蛋黄型空心球催化剂技术实现了 封存和能量储存双重效果,其原理如图1所示。制得的甲烷(
封存和能量储存双重效果,其原理如图1所示。制得的甲烷( )通过两步法可制取
)通过两步法可制取 ,原理如图2所示。
,原理如图2所示。
①已知
 中H为+1价,则空心球催化剂技术中获得的
中H为+1价,则空心球催化剂技术中获得的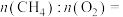
②若不考虑过程中原料损失,则16g
 通过两步法最多可制得
通过两步法最多可制得 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】补齐物质与其用途之间的连线。 _________
| 物质 | 用途 |
| A.氧化铁 | a.作红色颜料 |
| B.硝酸钾 | b.作膨松剂 |
| C.次氯酸钠 | c.作肥料 |
| D.碳酸氢钠 | d.作消毒剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】食品添加剂是指为改善食品品质而加入食品中的化学物质。常用食品添加剂有抗氧化剂、增味剂、消泡剂、膨松剂、着色剂等。
(1)现代食品工业中,食品添加剂占据重要地位,下列添加剂的使用方式不合理的是_______。
(2)维生素 常用作抗氧化剂,体现了维生素
常用作抗氧化剂,体现了维生素 的
的_______ (选填“氧化”或“还原”)性。
(3)小苏打(NaHCO3)是一种常用的膨松剂,小苏打属于_______ 。
A.电解质 B.碱 C.离子化合物 D.有机物
使用时在食材中同时加入_______ (选填“酸性”或“碱性”)物质效果更佳。
(4)碘酸钾( )是一种重要的食品添加剂,可作为食盐中的补碘剂。酸性溶液中
)是一种重要的食品添加剂,可作为食盐中的补碘剂。酸性溶液中 与
与 反应生成
反应生成 :
: ,若在家中检验某食盐是否含有碘酸钾,填写需要的试剂:家用食盐、干海带(含有
,若在家中检验某食盐是否含有碘酸钾,填写需要的试剂:家用食盐、干海带(含有 )、
)、_______ 、_______ (限选居家生活中常用的物质)。卫生部《食用盐碘含量》标准规定了食用盐产品碘含量的平均水平(以碘离子计)为 至
至 ,若测得某
,若测得某 食盐样品中含
食盐样品中含
 ,则该样品碘含量(以碘离子计)为
,则该样品碘含量(以碘离子计)为_______ 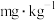 。(保留一位小数)
。(保留一位小数)
(1)现代食品工业中,食品添加剂占据重要地位,下列添加剂的使用方式不合理的是_______。
| A.高铁麦片中添加铁粉 | B.葡萄酒中添加二氧化硫 |
| C.水发毛肚中添加甲醛 | D.高钙牛奶中添加碳酸钙 |
 常用作抗氧化剂,体现了维生素
常用作抗氧化剂,体现了维生素 的
的(3)小苏打(NaHCO3)是一种常用的膨松剂,小苏打属于
A.电解质 B.碱 C.离子化合物 D.有机物
使用时在食材中同时加入
(4)碘酸钾(
 )是一种重要的食品添加剂,可作为食盐中的补碘剂。酸性溶液中
)是一种重要的食品添加剂,可作为食盐中的补碘剂。酸性溶液中 与
与 反应生成
反应生成 :
: ,若在家中检验某食盐是否含有碘酸钾,填写需要的试剂:家用食盐、干海带(含有
,若在家中检验某食盐是否含有碘酸钾,填写需要的试剂:家用食盐、干海带(含有 )、
)、 至
至 ,若测得某
,若测得某 食盐样品中含
食盐样品中含
 ,则该样品碘含量(以碘离子计)为
,则该样品碘含量(以碘离子计)为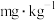 。(保留一位小数)
。(保留一位小数)
您最近一年使用:0次



