甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数均为14。
已知:甲为原子;乙、丙、丁为双原子分子或离子。
(1)甲单质与氢氧化钠溶液反应的离子方程式为______________ ;
(2)乙是双原子分子,在高温时是一种还原剂。14 g乙燃烧放出的热量是141.5 kJ。写出乙燃烧的热化学方程式__________________________________________ 。
(3)丙为双原子二价阴离子,与钙离子组成的化合物能跟水反应产生一种可燃性气体。该可燃性气体能与乙酸在一定条件下,按物质的量比1∶1发生加成反应生成一种酯,该化学方程式是为__________________________________________________ 。
(4)由丁分子组成的物质属于单质,组成丁的元素最高价氧化物对应的水化物X有下图所示转化关系(反应条件和其他物质已略)
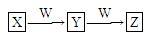
已知W为金属单质,W在周期表中的位置______________________ 。
写出X的稀溶液与Z反应的离子方程式:______________________________ 。
已知:甲为原子;乙、丙、丁为双原子分子或离子。
(1)甲单质与氢氧化钠溶液反应的离子方程式为
(2)乙是双原子分子,在高温时是一种还原剂。14 g乙燃烧放出的热量是141.5 kJ。写出乙燃烧的热化学方程式
(3)丙为双原子二价阴离子,与钙离子组成的化合物能跟水反应产生一种可燃性气体。该可燃性气体能与乙酸在一定条件下,按物质的量比1∶1发生加成反应生成一种酯,该化学方程式是为
(4)由丁分子组成的物质属于单质,组成丁的元素最高价氧化物对应的水化物X有下图所示转化关系(反应条件和其他物质已略)
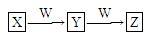
已知W为金属单质,W在周期表中的位置
写出X的稀溶液与Z反应的离子方程式:
10-11高三·河北衡水·阶段练习 查看更多[1]
(已下线)2011届河北省冀州中学高三一轮复习检测一化学试卷
更新时间:2016-12-09 01:28:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】填空。
(1)写出重晶石的化学式_______ 。计算机芯片的主要成分为___________ 。
(2)用电子式表示H2S的形成过程____________ 。
(3)一种金属离子与多种酸根离子所构成的盐称之为“混盐”,写出可溶性混盐CaOCl2溶于浓盐酸发生的离子方程式_______________ 。
(1)写出重晶石的化学式
(2)用电子式表示H2S的形成过程
(3)一种金属离子与多种酸根离子所构成的盐称之为“混盐”,写出可溶性混盐CaOCl2溶于浓盐酸发生的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高纯硅广泛应用于信息技术和新能源技术等领域。改良西门子法生产高纯硅的流程如图所示,回答下列问题:______ (填化学式),其与NaOH溶液反应的离子方程式为__________ 。
(2)制取粗硅时会生成一种有毒气体,该气体为______ (填化学式),粗硅与HCl反应生成 和
和 的化学方程式为
的化学方程式为____________________ 。
(3)还原炉中反应生成的氧化产物为______ (填化学式),若还原炉中有氧气混入,会造成的不良后果有________________________________________________ 答一点即可)。
(4)下列说法正确的是 (填标号)。

(2)制取粗硅时会生成一种有毒气体,该气体为
 和
和 的化学方程式为
的化学方程式为(3)还原炉中反应生成的氧化产物为
(4)下列说法正确的是 (填标号)。
| A.装KOH溶液的试剂瓶使用的是磨口玻璃塞 | B.改良西门子法提高了原料的利用率 |
| C.自然界中游离态的硅的含量较大 | D.单质硅是应用最广泛的半导体材料 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池板的是_________ (填化学式)。
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为_________ 。
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(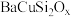 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
(4)工业上提纯硅有多种路线,其中一种工艺流程如图:

①电弧炉中发生反应的化学方程式为_________ 。
②在流化床反应的产物中, 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和_________ 。
③整个制作过程必须严格控制无水、无氧, 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为_________ 。
(1)可用于制作计算机芯片和太阳能电池板的是
(2)工艺师常用氢氟酸雕刻玻璃,该反应的化学方程式为
(3)兵马俑中所用颜料成分之一为蓝紫色的硅酸铜钡(
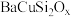 铜为
铜为 价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。
价),下列有关硅酸铜钡的说法不正确的是_________(填字母)。A.可用氧化物形式表示为 | B.性质稳定,不易脱色 |
| C.x等于6 | D.易溶解于强酸和强碱 |

①电弧炉中发生反应的化学方程式为
②在流化床反应的产物中,
 大约占85%,还有
大约占85%,还有 等,有关物质的沸点数据如表,则提纯
等,有关物质的沸点数据如表,则提纯 的主要工艺操作依次是沉降、冷凝和
的主要工艺操作依次是沉降、冷凝和| 物质 |  |  |  | 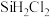 | 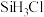 |  |  |
沸点/ | 2355 | 57.6 | 31.8 | 8.2 |  |  |  |
③整个制作过程必须严格控制无水、无氧,
 遇水剧烈反应生成
遇水剧烈反应生成 、
、 气体和另一种物质,该反应的化学方程式为
气体和另一种物质,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂的工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:

(1)操作a的名称为___________ 。
(2)②中物质为___________ ,试剂④为___________ ,鉴别溶液⑥中的金属阳离子时,应滴加的试剂依次是___________ ,请写出该鉴别过程中属于氧化还原反应的离子方程式___________ 。将FeSO4·7H2O溶于水配成溶液,并向该溶液中滴入稀H2SO4酸化的H2O2溶液,观察到溶液由浅绿色变成棕黄色,请写出该反应的离子方程式___________ 。
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ 。
(4)工业上常用绿矾( )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中___________ 是还原剂(填离子符号);若消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为___________ 。
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:
(1)操作a的名称为
(2)②中物质为
(3)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
(4)工业上常用绿矾(
 )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中 ,则转移电子的物质的量为
,则转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了______ 性,则56g Fe参加反应时,被还原的HNO3为____ g。
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有__________ 性。鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,你认为必须选用的物质有______ (填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______ 。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式______ Al+______ NaNO3+______ NaOH=______ NaAlO2+______ N2↑+______ H2O;若反应过程中转移5mol 电子,则生成标准状况下N2的体积为______ 。
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠、铝、铁是三种重要的金属。
(1)将一小块金属钠投入水中,反应的离子方程式为___________ ;钠能与冷水剧烈反应而铁不能,证明金属活动性:钠___________ 铁(填“>”或“<”)。
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为___________
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入___________ ,出现血红色溶液,证明氧化产物为Fe3+。
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为___________ 色,证明氧化产物为Fe3+,该反应的离子方程式为___________ (已知:淀粉遇I2变蓝)。
(1)将一小块金属钠投入水中,反应的离子方程式为
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求写热化学方程式:
(1)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式____________________________ 。.
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)⇌2NH3(g)△H=a kJ•mol﹣1.有关键能数据如表:
试根据表中所列键能数据估算a的数值_______ .
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g)△H1=﹣393.5kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l)△H2=﹣571.6kJ•mol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=﹣2599kJ•mol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:
△H=______________ .
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3﹣.两步反应的能量变化示
意图如图:

第一步反应是________ 反应(填“放热”或“吸热”),原因是___________________________________ .
(1)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)⇌2NH3(g)△H=a kJ•mol﹣1.有关键能数据如表:
化学键 | H﹣H | N﹣H | N≡N |
键能(kJ•mol﹣1) | 436 | 391 | 945 |
试根据表中所列键能数据估算a的数值
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g)△H1=﹣393.5kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l)△H2=﹣571.6kJ•mol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=﹣2599kJ•mol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:
△H=
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3﹣.两步反应的能量变化示
意图如图:

第一步反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
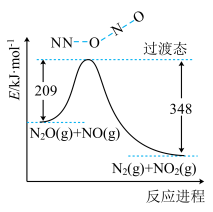
【推荐2】(1)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2,其△H=___ kJ·mol-1。
(2)已知:①C(s)+O2(g)=CO2(g) ΔH=akJ·mol-1
②CO2(g)+C(s)=2CO(g) ΔH=bkJ·mol-1
③Si(s)+O2(g)=SiO2(s) ΔH=ckJ·mol-1
工业上生产粗硅的热化学方程式为__ 。
(3)在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需117kJ/mol~125kJ/mol的热量,但1,3—环己二烯失去2个氢原子变成苯是放热反应,△H=-23.4kJ/mol,以上事实表明苯加氢生成环己烷是__ 反应。(填放热或吸热)
(4)X、Y两元素的原子,当它们分别获得两个电子形成稀有气体元素电子层结构时,X放出的热量大于Y放出的热量;Z、W两元素的原子,当它们分别失去一个电子形成稀有气体元素原子的电子层结构时,吸收能量W大于Z。则X、Y和Z、W分别形成的化合物中,离子化合物可能性最大的是__ 。(填化合物的化学式)
(5)称取等质量为(ag)胆矾两份。把一份溶于bg水中,测知其溶解时吸收Q1kJ热量;把另一份脱水后溶于bg水中,测得其溶解时放热Q2kJ。从以上数据可知,1mol胆矾脱水需__ kJ热量。

(2)已知:①C(s)+O2(g)=CO2(g) ΔH=akJ·mol-1
②CO2(g)+C(s)=2CO(g) ΔH=bkJ·mol-1
③Si(s)+O2(g)=SiO2(s) ΔH=ckJ·mol-1
工业上生产粗硅的热化学方程式为
(3)在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需117kJ/mol~125kJ/mol的热量,但1,3—环己二烯失去2个氢原子变成苯是放热反应,△H=-23.4kJ/mol,以上事实表明苯加氢生成环己烷是
(4)X、Y两元素的原子,当它们分别获得两个电子形成稀有气体元素电子层结构时,X放出的热量大于Y放出的热量;Z、W两元素的原子,当它们分别失去一个电子形成稀有气体元素原子的电子层结构时,吸收能量W大于Z。则X、Y和Z、W分别形成的化合物中,离子化合物可能性最大的是
(5)称取等质量为(ag)胆矾两份。把一份溶于bg水中,测知其溶解时吸收Q1kJ热量;把另一份脱水后溶于bg水中,测得其溶解时放热Q2kJ。从以上数据可知,1mol胆矾脱水需
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)用下列各组物质序号填空:
①O2和O3 ; ②12C、13C、14C; ③C2H6和C5H12; ④C3H6和C5H10; ⑤14N、14C ⑥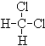 和
和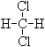 ;⑦CH3(CH2)3CH3和
;⑦CH3(CH2)3CH3和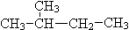
互为同位素的是_____ ;互为同素异形体的是_____ ;互为同系物的是_____ ;互为同分异构体的是_____ ;属于同一物质的是______ 。
(2)除去溴苯中的溴:试剂是:_____ ,反应的化学方程式为__________
(3)一定质量的乙醇在氧气不足时燃烧,得到CO、CO2和H2O质量共为27.6g,若H2O的质量为10.8g,则CO2的质量为______ g
(4)2gC2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,则C2H2燃烧热的热化学方程式:______ 。
①O2和O3 ; ②12C、13C、14C; ③C2H6和C5H12; ④C3H6和C5H10; ⑤14N、14C ⑥
 和
和 ;⑦CH3(CH2)3CH3和
;⑦CH3(CH2)3CH3和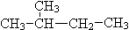
互为同位素的是
(2)除去溴苯中的溴:试剂是:
(3)一定质量的乙醇在氧气不足时燃烧,得到CO、CO2和H2O质量共为27.6g,若H2O的质量为10.8g,则CO2的质量为
(4)2gC2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,则C2H2燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 将水杨酸
将水杨酸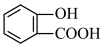 与
与________ 溶液作用,可以生成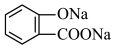 ;请写出将
;请写出将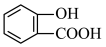 转化为
转化为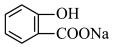 的化学方程式
的化学方程式_______ 。
 有机化合物B在浓硫酸存在条件下,相互作用生成一种环状酯
有机化合物B在浓硫酸存在条件下,相互作用生成一种环状酯 如下图
如下图 ,
,
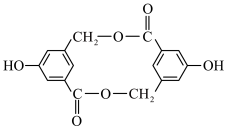
则有机化合物B的结构简式为______ ,等物质的量的B分别与Na、NaOH、 充分反应,消耗的Na、NaOH、
充分反应,消耗的Na、NaOH、 的物质的量之比为
的物质的量之比为____ 。
 有机物A的结构简式是
有机物A的结构简式是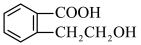 ,它可以通过不同的反应得到下列物质: B
,它可以通过不同的反应得到下列物质: B  C
C 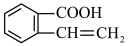 D
D  。
。
①A中官能团的名称是__________ 。
②写出由A制取C、D两种物质的有机反应类型,
A C:
C:_______  A
A D:
D:_____ 。
③写出由A制取B的化学方程式:____ 。
④写出由A制取C的化学方程式:__________
 将水杨酸
将水杨酸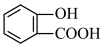 与
与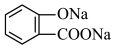 ;请写出将
;请写出将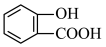 转化为
转化为 的化学方程式
的化学方程式 有机化合物B在浓硫酸存在条件下,相互作用生成一种环状酯
有机化合物B在浓硫酸存在条件下,相互作用生成一种环状酯 如下图
如下图 ,
, 
则有机化合物B的结构简式为
 充分反应,消耗的Na、NaOH、
充分反应,消耗的Na、NaOH、 的物质的量之比为
的物质的量之比为 有机物A的结构简式是
有机物A的结构简式是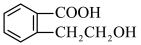 ,它可以通过不同的反应得到下列物质: B
,它可以通过不同的反应得到下列物质: B  C
C 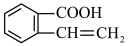 D
D  。
。①A中官能团的名称是
②写出由A制取C、D两种物质的有机反应类型,
A
 C:
C: A
A D:
D:③写出由A制取B的化学方程式:
④写出由A制取C的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】肉桂酸甲酯(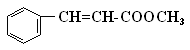 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
(1)肉桂酸甲酯的分子式是_________ ;
(2)有关肉桂酸甲酯的叙述中,正确的是__________ (填标号);
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键)。G的结构简式为_________ ;
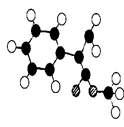
(4)用芳香烃A为原料合成G的路线如下:

① 化合物E中的官能团有_____________________ (填名称)。
② F→G的反应类型是________________ ,该反应的化学方程式为____________________________________________________________ 。
③ 写出符合下列条件的F的同分异构体的结构简式______________________ 。
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。
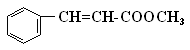 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。(1)肉桂酸甲酯的分子式是
(2)有关肉桂酸甲酯的叙述中,正确的是
| A.能与溴的四氯化碳溶液发生加成反应 | B.无法使酸性高锰酸钾溶液褪色 |
| C.在碱性条件下能发生水解反应 | D.不可能发生加聚反应 |
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图所示(图中球与球之间连线表示单键或双键)。G的结构简式为

(4)用芳香烃A为原料合成G的路线如下:

① 化合物E中的官能团有
② F→G的反应类型是
③ 写出符合下列条件的F的同分异构体的结构简式
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。
您最近一年使用:0次
【推荐3】某脱水偶联反应的反应式如下:
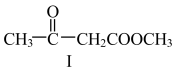 +
+ 
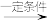
 + H2O
+ H2O
回答下列问题:
(1)化合物I的分子式为_______ ;化合物II中官能团的名称是_______ 。
(2)该脱水偶联反应的反应类型为_______ 。
(3)化合物II与氢气发生反应所得产物的结构简式为_______ 。
(4)下列关于化合物II的说法正确的是_______ 。
A.化合物II可以使溴水和高锰酸钾溶液褪色,二者褪色的原理相同
B.乙醇与化合物II不互为同系物
C.将灼热的铜丝插入化合物II的溶液中,反复几次,受热的铜丝将交替出现变红、变黑的现象
D.在加热条件下,化合物II可以与新制氢氧化铜发生反应形成砖红色沉淀
E.化合物II不能发生加聚反应形成高分子化合物
(5)写出化合物II与乙酸发生酯化反应的化学方程式:_______ 。
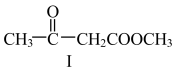 +
+ 
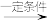
 + H2O
+ H2O回答下列问题:
(1)化合物I的分子式为
(2)该脱水偶联反应的反应类型为
(3)化合物II与氢气发生反应所得产物的结构简式为
(4)下列关于化合物II的说法正确的是
A.化合物II可以使溴水和高锰酸钾溶液褪色,二者褪色的原理相同
B.乙醇与化合物II不互为同系物
C.将灼热的铜丝插入化合物II的溶液中,反复几次,受热的铜丝将交替出现变红、变黑的现象
D.在加热条件下,化合物II可以与新制氢氧化铜发生反应形成砖红色沉淀
E.化合物II不能发生加聚反应形成高分子化合物
(5)写出化合物II与乙酸发生酯化反应的化学方程式:
您最近一年使用:0次



