某工厂排出的废水,经测定含0.012mol·L-1的游离Br2和8×10-4mol·L-1的H+离子。若用加Na2SO3的方法除去Br2,化学反应为:Na2SO3+Br2+H2O—Na2SO4+HBr(方程式未配平),现处理这种废水5L,问①需加入0.05mol·L-1的Na2SO3溶液多少升才能把Br2除尽?②除尽后的废水中H+离子的物质的量浓度是多少?(溶液的体积变化忽略不计)
11-12高三上·浙江杭州·阶段练习 查看更多[1]
(已下线)2011届浙江省杭州师范大学附属中学高三上学期第一次月考化学卷
更新时间:2011-03-12 11:07:07
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】某铁的氧化物中含氧化亚铁14.37%,三氧化二铁47.91%及四氧化三铁; 37.72%。称取此混合物10.0 g,加入100.0 mLx mol·L-1HCl溶液,立即通入N2 ,溶解完成后,加入7.2493 g铁粉(假定铁粉与HCl不反应)。待溶液变澄清后,滴入5.00 mol·L-1NaOH溶液200.0 mL。此时恰好完全生成白色沉淀,试求x值。___________________________
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】ClO2是一种易溶于水的黄绿色气体,可用作安全高效的水处理剂,某溶液X中所含ClO2浓度(g·L-1)的实验测定步骤如下:步骤1. 配制Na2S2O3溶液:准确称取1.984 0 g Na2S2O3·5H2O,用新煮沸并冷却的蒸馏水配成100.00 mL溶液。步骤2. 准确移取1.00 mL溶液X加入锥形瓶中,加入丙二酸静置后,再加入适量硫酸及稍过量的KI溶液(2ClO2+10I-+8H+===5I2+2Cl-+4H2O),在暗处放置5 min。步骤3. 向步骤2的锥形瓶的反应液中加入1 mL淀粉溶液作指示剂,再向其中滴加步骤1配制的Na2S2O3溶液(发生反应I2+2Na2S2O3===2NaI+Na2S4O6),至恰好完全反应时消耗Na2S2O3溶液25.00 mL。
(1)步骤1中所配Na2S2O3溶液的物质的量浓度为____ mol·L-1,所用玻璃仪器除烧杯、胶头滴管外还有____ 。(2)配制Na2S2O3溶液时,蒸馏水需煮沸的原因是____ 。
(3)计算溶液X中所含ClO2浓度(g·L-1)(写出计算过程)____ 。
(1)步骤1中所配Na2S2O3溶液的物质的量浓度为
(3)计算溶液X中所含ClO2浓度(g·L-1)(写出计算过程)
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐1】在实验室里,用足量的浓盐酸与一定量的MnO2反应,来制取氯气。
⑴用“双线桥法”标出电子转移情况_______________
MnO2+4HCl(浓)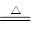 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
⑵若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克MnO2参加反应_________
②被氧化的HCl的物质的量为多少__________
⑴用“双线桥法”标出电子转移情况
MnO2+4HCl(浓)
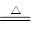 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O⑵若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克MnO2参加反应
②被氧化的HCl的物质的量为多少
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】把 4.6g的Na放入足量的水中,至充分完全反应。 请写出计算过程:
(1)写出化学方程式,画出双线桥。_____________________
(2)该反应电子转移的物质的量。________________________
(3)生成的 H2 在标准状况下的体积。_____________________
(4)反应后溶液体积为2L,计算所得溶液的物质的量浓度。__________
(1)写出化学方程式,画出双线桥。
(2)该反应电子转移的物质的量。
(3)生成的 H2 在标准状况下的体积。
(4)反应后溶液体积为2L,计算所得溶液的物质的量浓度。
您最近一年使用:0次




