氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生反应是2Cu+=Cu2++Cu。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是_______________ (填“氧化剂”或“还原剂”)。
(2)写出CuH在氯气中燃烧的化学反应方程式____________________ 。
(3)CuH溶液在稀盐酸中生成的气体是______________ (填化学式)。
根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶液在稀盐酸中生成的气体是
更新时间:2016-07-21 22:19:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Na2O2中氧元素化合价为﹣1价,根据氧化还原反应的知识可以推知Na2O2既有______ 性又有______ 性.Na2O2和KMnO4的H2SO4溶液反应,生成Na2SO4,MnSO4,K2SO4,O2和水,在这个反应中氧化剂为______ ,还原剂为______ .
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】已知:氧化性:KMnO4>HNO3;Bi位于周期表中ⅤA族,+3价较稳定,Bi2O3为碱性氧化物,Bi3+的溶液为无色。取一定量硝酸酸化的Mn(NO3)2溶液依次进行下列实验,现象记录如下:
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式:________________________________________ 。
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为________________________________ 。
(3)向反应③得到的溶液中通入SO2气体,看到的现象是____________________________________________________________ 。
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为_______ mol。
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式:
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
(3)向反应③得到的溶液中通入SO2气体,看到的现象是
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)氧化亚铜( )是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
ⅰ.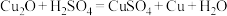
ⅱ.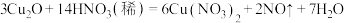
①反应ⅰ中还原剂为_______ (填化学式,下同),ⅱ的还原产物为_______ 。
②用单线桥标出反应ⅱ中电子转移的方向和数目:_______ 。
(2)高铁酸钠( )有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:
)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制备高铁酸钠的离子方程式:
。写出并配平湿法制备高铁酸钠的离子方程式:_______ 。
(3) 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。请配平上述化学方程式:
。请配平上述化学方程式:_______ 。
(4)产生1个 ,转移的电子的个数为
,转移的电子的个数为_______ 个。
(5)酸性高锰酸钾用_______ (填酸的化学式)酸酸化。
(1)氧化亚铜(
 )是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:
)是一种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应与硫酸、硝酸的反应如下:ⅰ.
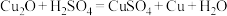
ⅱ.
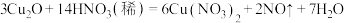
①反应ⅰ中还原剂为
②用单线桥标出反应ⅱ中电子转移的方向和数目:
(2)高铁酸钠(
 )有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒:
)有强氧化性,可以有效杀灭水中的细菌和病毒。已知湿法制备高铁酸钠的反应体系有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制备高铁酸钠的离子方程式:
。写出并配平湿法制备高铁酸钠的离子方程式:(3)
 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ 。请配平上述化学方程式:
。请配平上述化学方程式:(4)产生1个
 ,转移的电子的个数为
,转移的电子的个数为(5)酸性高锰酸钾用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等。如图所示流程是工业上制取纯硅的一种方法。

请回答下列问题:
(1)在上述生产过程中,属于置换反应的有___________ (填标号)。
(2)写出反应①的化学方程式:___________ 。
(3)化合物W的用途很广,可用于制备硅胶和木材防火剂等,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至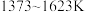 反应,可生成化合物W,其化学方程式是
反应,可生成化合物W,其化学方程式是_____ 。
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是_____ (填化学式)。

请回答下列问题:
(1)在上述生产过程中,属于置换反应的有
(2)写出反应①的化学方程式:
(3)化合物W的用途很广,可用于制备硅胶和木材防火剂等,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至
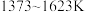 反应,可生成化合物W,其化学方程式是
反应,可生成化合物W,其化学方程式是(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO2)制备锰。
资料:①MnCO3难溶于水,可溶于稀酸。
②在Mn2+催化下,SO2在水溶液中被氧化成H2SO4。
I.制备
(1)写出铝热法还原MnO2制备锰的化学方程式_______ 。
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO2的烟气,可用以下方法处理。
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO2进行脱硫的化学方程式_______ 。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:

过程I:……
过程II :2Fe3++SO2+2H2O=2Fe2++ +4H+
+4H+
过程I的离子方程式是_______ 。
处理方法二:
③用MnCO3进行脱硫,可提高脱硫率。结合化学用语解释原因:_______ 。
II.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO4,将溶液中的Mn2+氧化为Mn3+,用c mol/L (NH4)2 Fe(SO4)2溶液进行滴定,达到滴定终点时,滴定管刻度由V0mL变为V1 mL,废水中锰的含量为____ g/mL。
资料:①MnCO3难溶于水,可溶于稀酸。
②在Mn2+催化下,SO2在水溶液中被氧化成H2SO4。
I.制备
(1)写出铝热法还原MnO2制备锰的化学方程式
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO2的烟气,可用以下方法处理。
处理方法一:
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用MnO2进行脱硫的化学方程式
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如下所示:

过程I:……
过程II :2Fe3++SO2+2H2O=2Fe2++
 +4H+
+4H+过程I的离子方程式是
处理方法二:
③用MnCO3进行脱硫,可提高脱硫率。结合化学用语解释原因:
II.废水中锰含量的测定
(3)取1 mL废水置于20 mL磷酸介质中,加入HClO4,将溶液中的Mn2+氧化为Mn3+,用c mol/L (NH4)2 Fe(SO4)2溶液进行滴定,达到滴定终点时,滴定管刻度由V0mL变为V1 mL,废水中锰的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将一定量的 溶液、
溶液、 溶液、
溶液、 溶液混合,充分反应后有白色沉淀产生,白色沉淀中只含有
溶液混合,充分反应后有白色沉淀产生,白色沉淀中只含有 元素与另一种元素,且该物质摩尔质量为
元素与另一种元素,且该物质摩尔质量为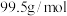 。请回答下列问题:
。请回答下列问题:
(1)白色沉淀的化学式为___________ 。
(2)上述反应的离子方程式为___________ 。
(3) 固体加热分解也会产生上述白色沉淀,则反应的另一产物是
固体加热分解也会产生上述白色沉淀,则反应的另一产物是___________ 。
(4)下列说法错误的是___________(填序号)。
 溶液、
溶液、 溶液、
溶液、 溶液混合,充分反应后有白色沉淀产生,白色沉淀中只含有
溶液混合,充分反应后有白色沉淀产生,白色沉淀中只含有 元素与另一种元素,且该物质摩尔质量为
元素与另一种元素,且该物质摩尔质量为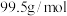 。请回答下列问题:
。请回答下列问题:(1)白色沉淀的化学式为
(2)上述反应的离子方程式为
(3)
 固体加热分解也会产生上述白色沉淀,则反应的另一产物是
固体加热分解也会产生上述白色沉淀,则反应的另一产物是(4)下列说法错误的是___________(填序号)。
A. 难溶于水 难溶于水 | B. 是电解质 是电解质 | C. 是白色固体 是白色固体 | D. 属于正盐 属于正盐 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铜在自然界多以+1价存在于矿石中,在固态特别是高温下,+1价铜的化合物比+2价稳定。用辉铜矿(Cu2S)炼铜的方法如下:
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是_____________ 。
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是____________ 。
(1)将辉铜矿在空气中高温焙烧,生成两种氧化物,反应的化学方程式是
(2)向焙烧得到的矿石中,再加上原矿石一半质量的未经焙烧过的矿石,混合后隔绝空气进行高温煅烧,得到金属铜和一种具有刺激性气味的气体,反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】地球上的金属矿物资源是有限的,应合理开发利用。
(1)金属冶炼的实质是金属离子被______ (填“氧化”或“还原”)生成金属单质。
(2)铜在自然界存在于多种矿石中,如:
请回答下列问题:
① 上表所列铜化合物中,推断铜的质量百分含量最高的是______ 。
② CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有______ 。
③ 工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是______ 。
④ Cu2(OH)2 CO3 与稀硫酸反应的离子方程式为______ 。
(1)金属冶炼的实质是金属离子被
(2)铜在自然界存在于多种矿石中,如:
| 矿石名称 | 黄铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu2S | Cu2(OH)2 CO3 |
请回答下列问题:
① 上表所列铜化合物中,推断铜的质量百分含量最高的是
② CuFeS2其中 Cu 为+1 价、Fe 为+3 价,高温焙烧时发生的反应是CuFeS2 + O2
 SO2 +FeS +Cu,焙烧过程中被还原的元素有
SO2 +FeS +Cu,焙烧过程中被还原的元素有③ 工业上以黄铜矿为原料,采用火法熔炼工艺生产铜,火法炼铜的反应为:Cu2S+O2
 2Cu+SO2,该反应中氧化剂是
2Cu+SO2,该反应中氧化剂是④ Cu2(OH)2 CO3 与稀硫酸反应的离子方程式为
您最近一年使用:0次



