一定条件下,乙醛可发生分解:CH3CHO(l)→CH4+CO,已知该反应的活化能为190 kJ·mol-1。 在含有少量I2的溶液中,该反应的机理如下:
反应Ⅰ:CH3CHO+I2 CH3I+HI+CO(慢)
CH3I+HI+CO(慢)
反应Ⅱ:CH3I+HI CH4+I2(快)
CH4+I2(快)
下列有关该反应的叙述正确的是 ( )
反应Ⅰ:CH3CHO+I2
 CH3I+HI+CO(慢)
CH3I+HI+CO(慢)反应Ⅱ:CH3I+HI
 CH4+I2(快)
CH4+I2(快)下列有关该反应的叙述正确的是 ( )
| A.反应速率与I2的浓度有关 | B.HI在反应Ⅰ中是氧化产物 |
| C.反应焓变的绝对值等于190 kJ·mol-1 | D.乙醛的分解速率主要取决于反应Ⅱ |
更新时间:2016-12-09 16:25:00
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方案达不到相应实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 分别测定稀NaOH溶液和稀氨水与稀盐酸发生中和反应的反应热 | 确定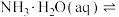 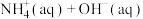 的 的 |
| B | 将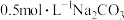 溶液逐渐升温,用pH传感器测量溶液的pH 溶液逐渐升温,用pH传感器测量溶液的pH | 探究温度对 水解平衡的影响 水解平衡的影响 |
| C | 常温下,向两支盛有5mL  溶液的试管中分别加入5mL 溶液的试管中分别加入5mL 硫酸、5mL 硫酸、5mL 硫酸 硫酸 | 探究浓度对反应速率的影响 |
| D | 将5mL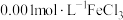 溶液和5mL 溶液和5mL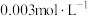 KSCN溶液混合后,再加入KCl固体 KSCN溶液混合后,再加入KCl固体 | 探究浓度对化学平衡: 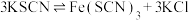 的影响 的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】2023年10月7日,《临汾日报》发表题为《全省首家氢能源公共自行车,落地曲沃》的报道。氢能源是清洁的二次能源,水煤气的变换反应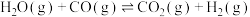 是一种重要的制氢手段,金基二元合金团簇
是一种重要的制氢手段,金基二元合金团簇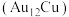 催化水煤气变换反应发生的氧化还原机理有A和B两种途径(*表示物质吸附在催化剂上)。
催化水煤气变换反应发生的氧化还原机理有A和B两种途径(*表示物质吸附在催化剂上)。
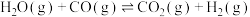 是一种重要的制氢手段,金基二元合金团簇
是一种重要的制氢手段,金基二元合金团簇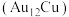 催化水煤气变换反应发生的氧化还原机理有A和B两种途径(*表示物质吸附在催化剂上)。
催化水煤气变换反应发生的氧化还原机理有A和B两种途径(*表示物质吸附在催化剂上)。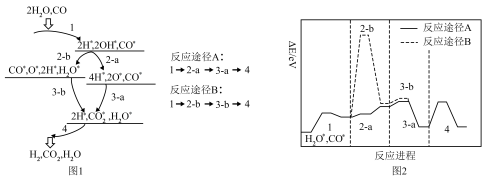
A.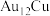 不参与制氢的化学反应 不参与制氢的化学反应 |
B.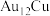 可提高 可提高 的平衡产率 的平衡产率 |
| C.水煤气的变换反应历程中同时存在极性键、非极性键的断裂和形成 |
| D.根据图2,反应途径A更有利于水煤气的变换反应 |
您最近一年使用:0次
【推荐1】京津冀地区的 大气污染问题已成影响华北环境的重要因素,有人想利用下列反应:2CO(g)+SO2(g) 2CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1 来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是
2CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1 来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是
 2CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1 来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是
2CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1 来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是 A.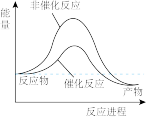 | B. | C.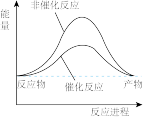 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
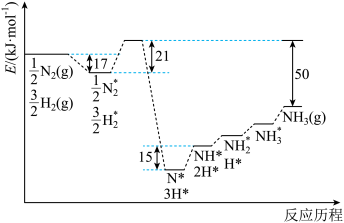
【推荐2】NH3可用于制造铵态氮肥和硝态氮肥。20世纪初,德国化学家哈伯首次用锇作催化剂在1.75×107Pa、550℃的条件下以N2和H2为原料合成了NH3:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。我国最新报道的氨催化合成反应的机理如图所示(*代表微粒吸附在催化剂表面)下列有关说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。我国最新报道的氨催化合成反应的机理如图所示(*代表微粒吸附在催化剂表面)下列有关说法正确的是
 2NH3(g) ΔH=-92.4 kJ·mol-1。我国最新报道的氨催化合成反应的机理如图所示(*代表微粒吸附在催化剂表面)下列有关说法正确的是
2NH3(g) ΔH=-92.4 kJ·mol-1。我国最新报道的氨催化合成反应的机理如图所示(*代表微粒吸附在催化剂表面)下列有关说法正确的是

| A.使用催化剂提高了反应的活化能 |
B.合成氨的总反应速率由反应 N2*+ N2*+ H2*=N*+3H*的速率决定 H2*=N*+3H*的速率决定 |
| C.反应过程中有非极性键的断裂和形成 |
| D.NH3从催化剂表面脱离时有热量放出 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列对有关事实或解释不正确的是
| 编号 | 事实 | 解释 |
| ① | 锌与稀硫酸反应,加入氯化钠固体,速率加快 | 增大了氯离子浓度,反应速率加快 |
| ② | 锌与稀硫酸反应,滴入较多硫酸铜溶液,生成氢气的速率减慢 | 锌置换铜的反应干扰了锌置换氢的反应,致使生成氢气的速率变慢 |
| ③ | 5%的双氧水中加入二氧化锰粉末,分解速率迅速加快 | 降低了反应的焓变,活化分子数增多,有效碰撞增多,速率加快 |
| ④ | 面粉生产车间容易发生爆炸 | 固体表面积大,反应速率加快 |
| A.①④ | B.②③ | C.①②③ | D.①②④ |
您最近一年使用:0次



