小强同学观看体操和举重比赛时,注意到运动员上场前都要在手上抹一些称为“镁粉”的白色粉末。小强和化学兴趣小组的同学一起探究“镁粉”的组成。
【提出猜想】①是金属镁的粉末;②是氧化镁;③是碳酸镁;④是氢氧化镁。大家一致认为猜想______ 是错误的,原因是______________________________ 。
【收集资料】氧化镁、碳酸镁和氢氧化镁都是白色粉末,三种物质几乎都不溶于水。其中,碳酸镁有很强的吸湿作用。
请你选取一种猜想,设计实验进行验证。你选的猜想是:________ ;设计实验:___________ 。
【提出猜想】①是金属镁的粉末;②是氧化镁;③是碳酸镁;④是氢氧化镁。大家一致认为猜想
【收集资料】氧化镁、碳酸镁和氢氧化镁都是白色粉末,三种物质几乎都不溶于水。其中,碳酸镁有很强的吸湿作用。
请你选取一种猜想,设计实验进行验证。你选的猜想是:
更新时间:2016-12-09 08:39:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】如图图像中,纵坐标为沉淀物的物质的量,横坐标为向溶液中加入反应物的物质的量,则相应的图像序号与(1)—(4)对应的是


| 溶液 | 加入物质 | 对应的图像 |
| (1)饱和石灰水 | 通过量CO2气体 | |
| (2)氯化铝溶液 | 加入过量氨水 | |
| (3)MgCl2、AlCl3的混合液 | 逐滴加入NaOH溶液至过量 | |
| (4)含少量NaOH的NaAlO2溶液 | 逐滴加入稀盐酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化合物 Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:Mg5Al3(OH)19(H2O)4 H2O↑+MgO+A12O3
H2O↑+MgO+A12O3
(1)请配平方程式_______________________ 。
(2)写出该化合物作阻燃剂的两条依据______ 。
(3)已知 MgO 可溶于 NH4Cl 的水溶液,其原理为______ (用化学方程式和必要的文字说明)。
 H2O↑+MgO+A12O3
H2O↑+MgO+A12O3(1)请配平方程式
(2)写出该化合物作阻燃剂的两条依据
(3)已知 MgO 可溶于 NH4Cl 的水溶液,其原理为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学是一门实用性很强的科学。根据题意填空:
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g) Fe3O4+4H2。该反应中H2O作
Fe3O4+4H2。该反应中H2O作__________ (填“氧化剂”或“还原剂”);
(2)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有________ (填“钠”或“钾”)元素;
(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是__________ (填“生石灰”或“盐酸”)。
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g)
 Fe3O4+4H2。该反应中H2O作
Fe3O4+4H2。该反应中H2O作(2)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有
(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)分别取相同质量的钠、镁、铝与足量的盐酸反应,在相同条件下产生H2的体积比_______ ;
(2)分别取0.1mol 钠、镁、铝与足量的盐酸反应,在相同条件下产生H2的体积比是__ ;
(3)若产生相同物质的量的H2,所需钠、镁、铝的质量比为__ ;
(4)若产生相同体积(同温同压下)的H2,所需的钠、镁、铝物质的量比为___ ;
(5)若将0.2mol钠、镁、铝分别投入到含HCl 0.2mol的盐酸中,在标准状况下,产生氢气体积的大小顺序是__ 。
(2)分别取0.1mol 钠、镁、铝与足量的盐酸反应,在相同条件下产生H2的体积比是
(3)若产生相同物质的量的H2,所需钠、镁、铝的质量比为
(4)若产生相同体积(同温同压下)的H2,所需的钠、镁、铝物质的量比为
(5)若将0.2mol钠、镁、铝分别投入到含HCl 0.2mol的盐酸中,在标准状况下,产生氢气体积的大小顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)镁称为“国防金属”,常用作还原剂和脱氧剂,二氧化碳常被用作灭火剂,但是当把点燃的镁条伸入盛有CO2的集气瓶中时,镁条却能继续燃烧。请写出化学方程式____________ 。
(2)下图变化是工业制硝酸的主要途径NH3→NO→NO2→HNO3请写出NH3→NO的化学方程式___________________ 。硝酸生产过程排放出来的NO是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的情况下,用氨把NO还原成无色无毒气体直接排放到空气中,化学方程式为______________ 。
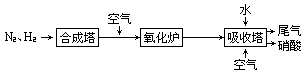
(2)下图变化是工业制硝酸的主要途径NH3→NO→NO2→HNO3请写出NH3→NO的化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求书写方程式:
(1)过氧化钠与CO2反应的化学方程式:__________________________________________
(2)镁条在二氧化碳中燃烧的化学方程式:________________________________________
(3)将少量硫酸铝溶液滴入足量NaOH溶液中的离子方程式:________________________
(4)铁与高温水蒸气反应的化学方程式:______________________________
(1)过氧化钠与CO2反应的化学方程式:
(2)镁条在二氧化碳中燃烧的化学方程式:
(3)将少量硫酸铝溶液滴入足量NaOH溶液中的离子方程式:
(4)铁与高温水蒸气反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(I)为了证明NH3·H2O是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验。0.010mol·L-1氨水、0.1mol·L-1NH4Cl溶液、NH4Cl晶体、酚酞溶液、pH试纸、蒸馏水。
①甲用pH试纸测出0.010mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法________ (填“正确”或“不正确”),并说明理由:__________________________________ 。
②乙取出10mL0.010mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1000mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b值应满足的关系是_____ 。
(II)(1)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=________ 。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________ 性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________ 性,NH4HCO3溶液中物质的量浓度最大的离子是________ (填化学式)。
①甲用pH试纸测出0.010mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法
②乙取出10mL0.010mol·L-1氨水,用pH试纸测其pH=a,然后用蒸馏水稀释至1000mL,再用pH试纸测其pH=b,若要确认NH3·H2O是弱电解质,则a、b值应满足的关系是
(II)(1)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列实验操作正确的是_______ 。
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
A.用量热计测定中和热时,为了操作方便,可用温度计直接搅拌
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,重复几次,完成乙醇氧化为乙醛的实验
C.试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,再加热制取乙酸乙酯
D.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
E.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合加热,充分振荡溶液、静置、待液体冷却后,滴加硝酸银溶液
G.向甲苯中加入酸性高锰酸钾溶液振荡,紫色不能退去
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学是一门以实验为基础的自然科学,化学实验具有极其重要的作用。
(1)在仪器①分液漏斗②烧杯③蒸发皿④蒸馏烧瓶⑤滴定管⑥容量瓶⑦量筒中,允许加热并必须垫上石棉网的有______ (填编号);使用时必须检查是否漏水的有_______ (填编号);可用于分离两种沸点接近且互不相溶的液态混合物的仪器有______ (填编号)。
(2)下面是常用的玻璃仪器组成的实验装置图。

①用装置A收集NH3气体,气体应从___________ (填“①”或“②”)处通入。
②若用装置B做二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶起到防倒吸作用,指出装置中错误之处__________ 。
③关闭图C装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:C装置是否漏气?(填“漏气”、“不漏气”或“无法确定”)______ ,判断理由 __________ 。
④装置D为倾析法分离固体和液体,简述过程中洗涤沉淀的基本操作方法______________ 。
(1)在仪器①分液漏斗②烧杯③蒸发皿④蒸馏烧瓶⑤滴定管⑥容量瓶⑦量筒中,允许加热并必须垫上石棉网的有
(2)下面是常用的玻璃仪器组成的实验装置图。

①用装置A收集NH3气体,气体应从
②若用装置B做二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶起到防倒吸作用,指出装置中错误之处
③关闭图C装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:C装置是否漏气?(填“漏气”、“不漏气”或“无法确定”)
④装置D为倾析法分离固体和液体,简述过程中洗涤沉淀的基本操作方法
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐1】(A)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:

(1)实验1中,沉淀最终变为________ 色,写出沉淀变色的化学方程式_______________________________ 。
(2)实验2甲针筒内的现象是:有___________ 生成,活塞________ 移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______ ,写出NO2与H2O反应的化学方程式为_______________________________ 。
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒内活塞有移动,针筒内有白烟产生外,气体的颜色变为____________ 。最后针筒内剩余气体的体积约为________ mL。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针简的现象 |
| 1 | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
| 2 | 20mLH2S | 10mLSO2 | |
| 3 | 30mLNO2(主要) | 10mLH2O(l) | 剩有无色气体,活塞自动向内压缩 |
| 4 | 15mLCl2 | 40mLNH3 |
(1)实验1中,沉淀最终变为
(2)实验2甲针筒内的现象是:有
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒内活塞有移动,针筒内有白烟产生外,气体的颜色变为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】实验室用如图所示装置制取乙烯。

(1)乙醇和浓硫酸的体积比为___________ 。
(2)①装置在170oC时主要反应的化学方程是___________ ;
②升温经过140oC左右时,发生副反应,主要生成物的结构简为___________ ;
(3)实验后期制得的乙烯气体中常含有两种杂质气体,将此混合气体直接通入溴水中能否证明乙烯发生加成反应的性质?___________ (填“能”或“否”)仪器B中盛装的试剂应是___________ 。

(1)乙醇和浓硫酸的体积比为
(2)①装置在170oC时主要反应的化学方程是
②升温经过140oC左右时,发生副反应,主要生成物的结构简为
(3)实验后期制得的乙烯气体中常含有两种杂质气体,将此混合气体直接通入溴水中能否证明乙烯发生加成反应的性质?
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】我国规定饮用水质量标准必须符合下列要求:
以下是源水处理成自来水的工艺流程示意图
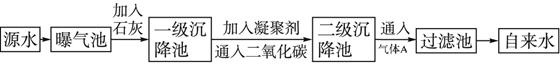
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式:_________________________。
(2)凝聚剂除去悬浮固体颗粒的过程____________(填序号)。FeSO4·7H2O是常用的凝聚剂,它在水中最终生成____________沉淀。
①只是物理过程 ②只是化学过程 ③是物理和化学过程
(3)通入二氧化碳的目的是________________和______________________。
(4)气体A的作用是_________________________。这种作用是基于气体A和水反应的产物具有__________性。
(5)下列物质中____________可以作为气体A的代用品。
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
| pH | 6.5~8.5 |
| Ca2+、Mg2+ | <0.004 5 mol·L-1 |
| 细菌总数 | <100个/mL |
以下是源水处理成自来水的工艺流程示意图

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式:_________________________。
(2)凝聚剂除去悬浮固体颗粒的过程____________(填序号)。FeSO4·7H2O是常用的凝聚剂,它在水中最终生成____________沉淀。
①只是物理过程 ②只是化学过程 ③是物理和化学过程
(3)通入二氧化碳的目的是________________和______________________。
(4)气体A的作用是_________________________。这种作用是基于气体A和水反应的产物具有__________性。
(5)下列物质中____________可以作为气体A的代用品。
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
您最近一年使用:0次



