配平下列方程并改写成离子方程式
(1)SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4___ ,___
(2)Cu+HNO3 → Cu(NO3)2+NO↑+H2O___ ,___
(1)SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
(2)Cu+HNO3 → Cu(NO3)2+NO↑+H2O
更新时间:2016-12-09 16:44:06
|
【知识点】 氧化还原反应方程式的配平解读
相似题推荐
【推荐1】氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾
 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
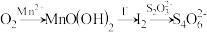
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:__________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程__________ 。
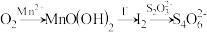
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。(已知反应:I2+2S2O32-=2I-+S4O62-)计算该水样中的溶解氧(以mg·L−1表示),写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)配平反应的离子方程式:_____ XeO3+____ Mn2++_____ H2O →____ MnO4-+____ Xe↑+___ H+
(2)反应现象为:①有气泡产生,②______________________ 。
(3)发生氧化反应的物质(或微粒)是_______________ 。
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子_____________ mol。
②将反应后的溶液稀释至90mL,所得溶液的pH=________ 。
(2)反应现象为:①有气泡产生,②
(3)发生氧化反应的物质(或微粒)是
(4)将适量的XeO3投入30mL 0.1mol⋅L−1 Mn2+的水溶液中,刚好完全反应。
①此时转移电子
②将反应后的溶液稀释至90mL,所得溶液的pH=
您最近一年使用:0次



