某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的一种或几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。
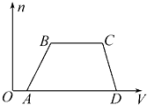
回答下列问题:
(1)溶液中一定含有的溶质是_______ ,一定不含有的溶质是_____ (填化学式)。
(2)溶液中可能含有的溶质是________ (填名称),判断该物质是否存在的实验方法是________ ,现象是________ 。
(3)分别写出AB段、BC段发生反应的离子方程式:①AB段为________ ;②BC段为________ 。

回答下列问题:
(1)溶液中一定含有的溶质是
(2)溶液中可能含有的溶质是
(3)分别写出AB段、BC段发生反应的离子方程式:①AB段为
更新时间:2016-12-09 16:44:37
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】物质A~K有如下的转化关系,其中D、E为气体单质,试回答(图中有些反应的产物和反应的条件没有全部标出):

(1)写出下列物质的化学式:
D是______________ ,G是_______________ ;
(2)写出“C→F”反应的离子方程式_____________________________ ;
(3)写出反应“F→G”的离子方程式_____________________________ ;
(4)写出反应“I→J”的离子方程式_____________________________ ;
(5)在溶液I中滴入NaOH溶液,可观察到的现象是___________________________ ;写出相关的化学反应方程式_________________________ 。
(6)向200 mL 3mol/L溶液J中加入60 g铁、铜混合物(铁和铜的物质的量比为1:1),充分反应后过滤,向滤液中通入足量的氨气,充分反应后再过滤、洗涤、干燥、灼烧,灼烧后得到固体的质量为________ 。

(1)写出下列物质的化学式:
D是
(2)写出“C→F”反应的离子方程式
(3)写出反应“F→G”的离子方程式
(4)写出反应“I→J”的离子方程式
(5)在溶液I中滴入NaOH溶液,可观察到的现象是
(6)向200 mL 3mol/L溶液J中加入60 g铁、铜混合物(铁和铜的物质的量比为1:1),充分反应后过滤,向滤液中通入足量的氨气,充分反应后再过滤、洗涤、干燥、灼烧,灼烧后得到固体的质量为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】某兴趣小组对化合物X开展探究实验:
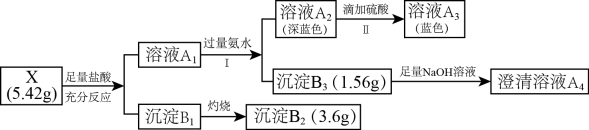
其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有___________ (填元素符号)。
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为___________ 。
(3)步骤I中生成沉淀B3的离子方程式为___________ 。
(4)步骤II中溶液由深蓝色转变为蓝色的原因是___________ 。
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式___________ 。
②确定X的化学式为___________ 。

其中:化合物X有由4种元素组成;沉淀B2是工业生产玻璃的重要原料。
请回答:
(1)组成X的四种元素中除含O外,还有
(2)在澄清溶液A4中通入过量CO2,产生沉淀的离子方程式为
(3)步骤I中生成沉淀B3的离子方程式为
(4)步骤II中溶液由深蓝色转变为蓝色的原因是
(5)为进一步确定X的化学式,往溶液A1中通入足量的SO2,生成0.995g的白色沉淀(其中氯元素的质量分数为35.7%),在反应后的溶液中滴加BaCl2溶液,有白色沉淀生成。
①写出A1中通入SO2的离子反应方程式
②确定X的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】短周期元素形成的物质A、B、C、D、E,它们的转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同)。

请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的电子式:_____________
(2)若E是有臭鸡蛋气味,D是既能溶于强酸,又能溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因:____________________
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系:_______________________________
(3)若C是一种气体,D是一种强酸,且E与A相同,则C与水反应的化学方程式为(请标出电子转移方向和数目):__________________________________________
(4)若A是一种单质,该元素的原子最外层电子数等于最内层,气体E能使湿润的红色石蕊试纸变蓝,那么化合物D是_____________ 。

请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的电子式:
(2)若E是有臭鸡蛋气味,D是既能溶于强酸,又能溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因:
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系:
(3)若C是一种气体,D是一种强酸,且E与A相同,则C与水反应的化学方程式为(请标出电子转移方向和数目):
(4)若A是一种单质,该元素的原子最外层电子数等于最内层,气体E能使湿润的红色石蕊试纸变蓝,那么化合物D是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】Ⅰ、A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示。

(1)若A是淡黄色化合物;常温下D是无色气体;C是一种常见的碱,含有的阴、阳离子均为10电子粒子。写出反应Ⅰ的化学方程式___________ 。
(2)若A是酸,D是一种常见金属,E是一种常见的非金属单质。
①写出反应Ⅱ的离子方程式___________ 。
②检验B中含有少量C的方法是:取少量溶液加入___________ (填序号)后观察现象。
A. 溶液 B.
溶液 B. 溶液 C.淀粉
溶液 C.淀粉 溶液 D.酸性
溶液 D.酸性 溶液
溶液
(3)若A是常见的两性氧化物,E是一种无色无味的气体。
①C的化学式为___________ 。
②写出反应II,E少量的离子方程式___________ 。
Ⅱ、向一定量 、
、 溶液中滴加常用试剂
溶液中滴加常用试剂 与盐酸(t点之前滴加的试剂为a,t点之后改滴试剂b),沉淀的物质的量
与盐酸(t点之前滴加的试剂为a,t点之后改滴试剂b),沉淀的物质的量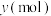 与试剂体积
与试剂体积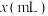 间的关系曲线如图所示。试回答:
间的关系曲线如图所示。试回答:

(4) 段所表示的反应的离子方程式是
段所表示的反应的离子方程式是___________ ;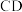 段所表示的反应的离子方程式是
段所表示的反应的离子方程式是___________ ;
(5)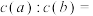
___________ ;原混合液中,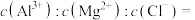
___________ 。

(1)若A是淡黄色化合物;常温下D是无色气体;C是一种常见的碱,含有的阴、阳离子均为10电子粒子。写出反应Ⅰ的化学方程式
(2)若A是酸,D是一种常见金属,E是一种常见的非金属单质。
①写出反应Ⅱ的离子方程式
②检验B中含有少量C的方法是:取少量溶液加入
A.
 溶液 B.
溶液 B. 溶液 C.淀粉
溶液 C.淀粉 溶液 D.酸性
溶液 D.酸性 溶液
溶液(3)若A是常见的两性氧化物,E是一种无色无味的气体。
①C的化学式为
②写出反应II,E少量的离子方程式
Ⅱ、向一定量
 、
、 溶液中滴加常用试剂
溶液中滴加常用试剂 与盐酸(t点之前滴加的试剂为a,t点之后改滴试剂b),沉淀的物质的量
与盐酸(t点之前滴加的试剂为a,t点之后改滴试剂b),沉淀的物质的量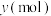 与试剂体积
与试剂体积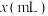 间的关系曲线如图所示。试回答:
间的关系曲线如图所示。试回答:
(4)
 段所表示的反应的离子方程式是
段所表示的反应的离子方程式是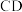 段所表示的反应的离子方程式是
段所表示的反应的离子方程式是(5)
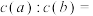
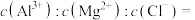
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】四氢铝钠(NaAlH4)是强还原剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:___________ (任写一个)。
(2)“转化”中 的具体作用是
的具体作用是___________ ;“分离”的操作是指___________ 。
(3)由 制备
制备 溶液的离子方程式为
溶液的离子方程式为___________ 。
(4)“沉铝”时通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ ;所得滤液中的溶质有___________ (写化学式)。
(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)___________ 。
(6) 中氢的化合价为
中氢的化合价为___________ ;“有效氢”指单位质量(1g)含氢还原剂的还原能力相当于多少克氢气的还原能力。则 的“有效氢”为
的“有效氢”为___________ (保留三位有效数字)。
 )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 ,含少量
,含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题:
)为原料制备四氢铝钠和高铁酸钠的流程如下,回答下列问题: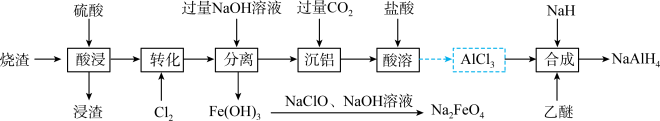
(2)“转化”中
 的具体作用是
的具体作用是(3)由
 制备
制备 溶液的离子方程式为
溶液的离子方程式为(4)“沉铝”时通入过量
 发生反应的离子方程式为
发生反应的离子方程式为(5)“合成”中,发生反应的化学方程式为(乙醚作溶剂,不参与反应)
(6)
 中氢的化合价为
中氢的化合价为 的“有效氢”为
的“有效氢”为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】可根据化学试剂相互之间逐滴滴加所产生的现象不同,来检验化学物质。此方法可以检验 和
和 溶液,现按要求回答下列问题:
溶液,现按要求回答下列问题:
(1)向 溶液中逐滴滴入
溶液中逐滴滴入 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①___________ ②__________ ,对应反应的离子方程式分别是①___________ ②___________ ,并画出相应的图像变化__________
(2)向 溶液中逐滴滴入
溶液中逐滴滴入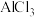 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①__________ ②_________ ,对应反应的离子方程式分别是①__________ ②___________ ,并画出相应的图像变化_______
 和
和 溶液,现按要求回答下列问题:
溶液,现按要求回答下列问题:(1)向
 溶液中逐滴滴入
溶液中逐滴滴入 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①(2)向
 溶液中逐滴滴入
溶液中逐滴滴入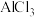 溶液至过量,产生的现象分别是①
溶液至过量,产生的现象分别是①
您最近一年使用:0次
【推荐1】海水是一种丰富的资源,工业生产可以从海水中提取许多有用的物质,这些物质广泛应用于生活、生产、科技等方面。下图是从含碘CCl4溶液得到碘的实验过程:
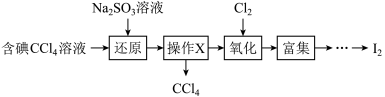
完成下列填空:
(1)向含碘溶液中加入稍过量的Na2SO3溶液,其离子方程式为_________ ;该操作将I2还原为I-的目的是__________ 。
(2)操作X的名称为_______ ,所用的主要仪器是_________ 。
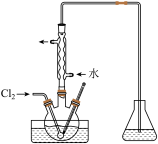
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是_________ ;锥形瓶里盛放的溶液为________ 。
(4)已知:5SO32-+2IO3-+2H+ → I2+5SO42-+H2O某含碘溶液(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘溶液中是否同时含有I-、IO3-的实验方案:_______ 。实验中可供选择的试剂:CCl4、稀盐酸、淀粉溶液
(5)浓海水提取镁的工艺流程如下图:
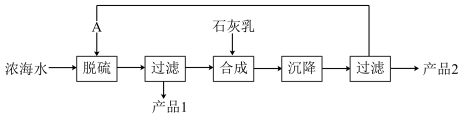
浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的离子方程式为________ ,产品2的化学式为__________ 。1L浓海水最多可得到产品2的质量为____ g。

完成下列填空:
(1)向含碘溶液中加入稍过量的Na2SO3溶液,其离子方程式为
(2)操作X的名称为
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是

(4)已知:5SO32-+2IO3-+2H+ → I2+5SO42-+H2O某含碘溶液(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘溶液中是否同时含有I-、IO3-的实验方案:
(5)浓海水提取镁的工艺流程如下图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】某工业废催化剂含有 SiO2、ZnO、CuS、ZnS、Fe3O4 等物质,为落实“节约资源,变 废为宝”的环保理念,某课外兴趣小组的同学取 20g 该物质进行实验,回收其中的 Cu 和 Zn,实验方案如下:

已知:ZnS 可与稀硫酸反应;CuS 不溶于稀硫酸,也不与其发生反应。 请回答下列问题:
(1)可用图装置进行第一次浸出,烧杯中盛放的是______ 溶液。

(2)滤液Ⅰ中的 Fe2+最好用______ 来检验。
a.氯水 b.双氧水 c.KSCN 溶液 d.K3[Fe(CN)6]溶液
(3)物质 A 是含有 X 元素的氧化物(XO),则 X 是______ (填元素符号),由滤液Ⅱ、Ⅳ滤液获得 ZnSO4•7H2O 的操作是______________ 。
(4)第二次浸出时的化学方程式为_______________ 。
(5)加 A 调节溶液的 pH 约为______ 时,可以完全除去其中的杂质离子。
(当溶液中离子浓度小于等于 10-5mol/L 时视为沉淀完全;实验条件下部分物质的溶度积常数为:Ksp[Fe(OH)3]=10-38,Ksp[Fe(OH)2]=10-17,Ksp[Zn(OH)2]=10-17,Ksp[Cu(OH)2]=10-20)
(6)实验最后获得了 5.74gZnSO4•7H2O 晶体(假设实验中没有损耗),但不能由此确定原催化剂中锌元素的质量分数,原因是_________________ 。

已知:ZnS 可与稀硫酸反应;CuS 不溶于稀硫酸,也不与其发生反应。 请回答下列问题:
(1)可用图装置进行第一次浸出,烧杯中盛放的是

(2)滤液Ⅰ中的 Fe2+最好用
a.氯水 b.双氧水 c.KSCN 溶液 d.K3[Fe(CN)6]溶液
(3)物质 A 是含有 X 元素的氧化物(XO),则 X 是
(4)第二次浸出时的化学方程式为
(5)加 A 调节溶液的 pH 约为
(当溶液中离子浓度小于等于 10-5mol/L 时视为沉淀完全;实验条件下部分物质的溶度积常数为:Ksp[Fe(OH)3]=10-38,Ksp[Fe(OH)2]=10-17,Ksp[Zn(OH)2]=10-17,Ksp[Cu(OH)2]=10-20)
(6)实验最后获得了 5.74gZnSO4•7H2O 晶体(假设实验中没有损耗),但不能由此确定原催化剂中锌元素的质量分数,原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。

已知:阳离子以氢氧化物形式完全沉淀时溶液的pH:
一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。
请回答:
(1)写出A与氢氟酸反应的化学方程式: 。
(2)上述流程中两次使用试剂X,推测试剂X是 (填以下字母编号)
A.水 B.氧化铝 C.氨水 D.氢氧化钠
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是 。(任写2点)
 (4)写出F→H的反应离子方程式: 。
(4)写出F→H的反应离子方程式: 。
(5)证明H溶液的主要阴离子(Cl-除外)的方法是 。

已知:阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.4 | 5.2 | 12.4 |
一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。
请回答:
(1)写出A与氢氟酸反应的化学方程式: 。
(2)上述流程中两次使用试剂X,推测试剂X是 (填以下字母编号)
A.水 B.氧化铝 C.氨水 D.氢氧化钠
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是 。(任写2点)
 (4)写出F→H的反应离子方程式: 。
(4)写出F→H的反应离子方程式: 。(5)证明H溶液的主要阴离子(Cl-除外)的方法是 。
您最近一年使用:0次



