 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:
(2)实验室用两种固体制取NH3的反应化学方程式为
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
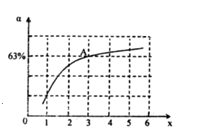
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)\frac{n(NH_{3})}{n(CO_{2})}=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是
(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)⇌2NH3(g),测得甲容器中H2的平衡转化率为40%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:
(7)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(8)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为
更新时间:2016-12-09 17:09:19
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】工业上氧化二氧化硫制三氧化硫反应的化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H=-198kJ•mol-1。假设该反应处于平衡状态,在体积不变的条件下,下列措施会对化学平衡产生怎样的影响?
2SO3(g) △H=-198kJ•mol-1。假设该反应处于平衡状态,在体积不变的条件下,下列措施会对化学平衡产生怎样的影响?
(1)增加二氧化硫____
(2)升高温度____
(3)增大压强____
(4)移出三氧化硫____
 2SO3(g) △H=-198kJ•mol-1。假设该反应处于平衡状态,在体积不变的条件下,下列措施会对化学平衡产生怎样的影响?
2SO3(g) △H=-198kJ•mol-1。假设该反应处于平衡状态,在体积不变的条件下,下列措施会对化学平衡产生怎样的影响?(1)增加二氧化硫
(2)升高温度
(3)增大压强
(4)移出三氧化硫
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】将水分解制得氢气的一种工业方法是“硫﹣碘循环法”,依次涉及下列三步反应:
I.SO2+2H2O+I2=H2SO4+2HI
II.2HI(g)⇌H2(g)+I2(g)
III.2H2SO4=2SO2+O2+2H2O
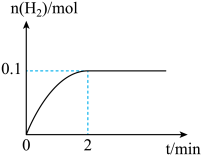
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)=___ 。相同温度下,若起始加入的HI改为2mol,反应达平衡时H2的量为___ mol。
(2)分析上述反应,下列判断错误的是___ (填写选项编号,只有一个正确选项)。
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂
I.SO2+2H2O+I2=H2SO4+2HI
II.2HI(g)⇌H2(g)+I2(g)
III.2H2SO4=2SO2+O2+2H2O
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)=

(2)分析上述反应,下列判断错误的是
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐3】某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据填空:
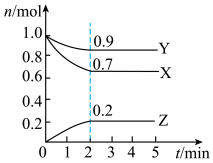
(1)该反应的化学方程式为______ 。
(2)反应开始至2min末,以气体X表示的平均反应速率为_____ ;反应开始时与反应达平衡状态时的压强之比为_____ 。
(3)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是_____ 。
①混合气体的压强不再变化
②混合气体的密度不再变化
③X的百分含量不再变化
④混合气体的平均相对分子质量不再变化
⑤v(X):v(Y)=3:1

(1)该反应的化学方程式为
(2)反应开始至2min末,以气体X表示的平均反应速率为
(3)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是
①混合气体的压强不再变化
②混合气体的密度不再变化
③X的百分含量不再变化
④混合气体的平均相对分子质量不再变化
⑤v(X):v(Y)=3:1
| A.①②⑤ | B.①③④ | C.②③④ | D.③④⑤ |
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】说出下列反应中的焓变,熵变,及自发性
CO2(s)→ CO2(g)____________
2Mg(s)+O2(g)=2MgO(s)____________
2K(s)+2H2O(l)=2K+(aq)+2OH-(aq)+H2(g)____________
CO2(s)→ CO2(g)
2Mg(s)+O2(g)=2MgO(s)
2K(s)+2H2O(l)=2K+(aq)+2OH-(aq)+H2(g)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】请你判断以下过程是熵增加过程还是熵减小过程。
(1)C2H5OH(l)=C2H5OH(s)____
(2)N2O4(g)=2NO2(g)____
(3) O2(g)+Cu(s)=CuO(s)
O2(g)+Cu(s)=CuO(s)____
(4)NH3(g)+HCl(g)=NH4Cl(s)____
(5)N2(g)+3H2(g)=2NH3(g)____
(1)C2H5OH(l)=C2H5OH(s)
(2)N2O4(g)=2NO2(g)
(3)
 O2(g)+Cu(s)=CuO(s)
O2(g)+Cu(s)=CuO(s)(4)NH3(g)+HCl(g)=NH4Cl(s)
(5)N2(g)+3H2(g)=2NH3(g)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3 与 ΔH1、ΔH2 之间的关系是:ΔH3=________ 。
(2)白磷与氧气反应生成P4O10 固体。下表所示是部分化学键的键能参数:
根据右图的分子结构和有关数据通过计算写出该反应的热化学方程式为_____________ 。
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右下图)之间脱去两个水分子产物,其结构式为_________________ ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为____________ 。


(4)已知298 K时白磷不完全燃烧的热化学方程式为:
P4(s,白磷)+3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。
在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________ 。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)
 (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1反应Ⅱ:NH3(l)+H2O(l)+CO2(g)
 NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)
 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3则ΔH3 与 ΔH1、ΔH2 之间的关系是:ΔH3=
(2)白磷与氧气反应生成P4O10 固体。下表所示是部分化学键的键能参数:
| 化学键 | P—P | P—O | P===O | O===O |
| 键能/kJ·mol-1 | a | b | c | d |
根据右图的分子结构和有关数据通过计算写出该反应的热化学方程式为
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右下图)之间脱去两个水分子产物,其结构式为


(4)已知298 K时白磷不完全燃烧的热化学方程式为:
P4(s,白磷)+3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。
在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为
您最近一年使用:0次



