将一定质量的镁铝合金投入到200 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加 5 mol • L-1的NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。求:

(1)原合金中Mg的质量________ g;Al的质量________ g
(2)盐酸的物质的量浓度______ mol/L。

(1)原合金中Mg的质量
(2)盐酸的物质的量浓度
更新时间:2016-11-25 16:38:22
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】铝及其化合物在生活、生产中有广泛应用。
(1)Na3AlF6是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上,用HF、Na2CO3和Al(OH)3制备冰晶石。化学反应原理是,2Al(OH)3+3Na2CO3+12H=2Na3AlF6+3CO2↑+9H2O.属于盐的有Na2CO3和_______ 。上述反应不能在玻璃容器中反应,其原因是________ (用化学方程式表示)。
(2)明矾[KAl(SO4)2·12H2O]常作净水剂。在明矾溶液中滴加氢氧化钡溶液至Al3+恰好完全沉淀,写出该反应的离子方程式____________ 。
(3)铝合金广泛用于建筑材料。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生氢气体积相等(同温同压)。则该合金中铁、硅的质量之比为______ 。(已知:Si+2NaOH+H2O=Na2SiO3+ 2H2↑)
(4)铝氢化钠(NaAlH4)是有机合成的重要还原剂。它的制备方法是将氢化钠和氯化铝在乙醚中反应制备铝氢化钠。
①写出化学方程式________________ 。
②在化学上,含氢还原剂的还原能力用“有效氢”表示,”有效氢”含义是单位质量的含氢还原剂的还原能力相当于多少克氢气。一般地含氢还原剂的氢被氧化成H2O,“还原能力”用氢失去电子数多少表示。NaAlH4、NaH的“有效氢”之比为________ 。
(1)Na3AlF6是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上,用HF、Na2CO3和Al(OH)3制备冰晶石。化学反应原理是,2Al(OH)3+3Na2CO3+12H=2Na3AlF6+3CO2↑+9H2O.属于盐的有Na2CO3和
(2)明矾[KAl(SO4)2·12H2O]常作净水剂。在明矾溶液中滴加氢氧化钡溶液至Al3+恰好完全沉淀,写出该反应的离子方程式
(3)铝合金广泛用于建筑材料。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生氢气体积相等(同温同压)。则该合金中铁、硅的质量之比为
(4)铝氢化钠(NaAlH4)是有机合成的重要还原剂。它的制备方法是将氢化钠和氯化铝在乙醚中反应制备铝氢化钠。
①写出化学方程式
②在化学上,含氢还原剂的还原能力用“有效氢”表示,”有效氢”含义是单位质量的含氢还原剂的还原能力相当于多少克氢气。一般地含氢还原剂的氢被氧化成H2O,“还原能力”用氢失去电子数多少表示。NaAlH4、NaH的“有效氢”之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】在标准状况下进行甲、乙、丙三组实验,三组各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据如表:
(1)乙组实验中,盐酸_______ (填“过量”“适量”或“不足量”),理由是_______ 。
(2)要算出盐酸的物质的量浓度,题中可作计算依据的数据是_______ (填“甲”、“乙”、“丙”),求得的盐酸的物质的量浓度为_______ 。
(3)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是_______ (填“甲”、“乙”、“丙”),求得的Mg、A1的物质的量之比为_______ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 生成气体体积(mL) | 280 | 336 | 336 |
(1)乙组实验中,盐酸
(2)要算出盐酸的物质的量浓度,题中可作计算依据的数据是
(3)求合金中Mg、Al的物质的量之比,题中可作计算依据的数据是
您最近一年使用:0次
【推荐3】高锰酸钾是一种典型的强氧化剂。完成下列填空:
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
② MnO +CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:___________
___________MnO +___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
+___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为___________ g。需要的玻璃仪器有___________
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(4)用软锰矿制备K2MnO4的化学方程式是:___________ 。
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为___________ 。
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO
 +Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)
+Cu2S+H+→Cu2++SO2↑+Mn2++H2O(未配平)② MnO
 +CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)
+CuS +H+→Cu2++SO2↑+Mn2++H2O(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
d.还原性的强弱关系是:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
___________MnO
 +___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O
+___________Fe2++___________H+=___________Mn2++___________Fe3++___________ H2O(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。
请回答:
(4)用软锰矿制备K2MnO4的化学方程式是:
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】镁的单质及其化合物在储氢及大气治理等方面用途非常广泛。
I.工业上可以采用热还原法制备金属镁(沸点1107℃,熔点648.8℃)。将碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]和焦炭按一定比例混合,放入真空管式炉中先升温至700℃保持一段时间,然后升温至1450℃反应制得镁(同时生成可燃性气体)。
(1)用碳还原法制备金属镁需要在真空中而不在空气中进行,其原因是____________ 。
(2)碱式碳酸镁分解如图所示,写出在1450℃反应制得镁的化学方程式:_____________ 。

II.工业上利用纳米MgH2和LiBH4组成的体系储放氢(如题图所示)。

(3)写出放氢过程中发生反应的化学方程式:___________ 。
III.工业上MgO浆液是高活性的脱硫剂,常用来脱除烟气中的SO2。主要包含的反应有:① Mg(OH)2+ SO2=MgSO3+H2O ② MgSO3+SO2+H2O= Mg(HSO3)2③ Mg(HSO3)2+ Mg(OH)2=2MgSO3+2H2O ④ 2MgSO3+O2=2MgSO4
脱硫时,MgO的脱硫效率、pH及时间的关系如题图所示。

已知20℃时,H2SO3的K1=l.54×10-2,K2=1.02×10-7,25℃时,Ksp[MgSO3]= 3.86×10-3,Ksp(CaSO3)= 3.1×10-7。
(4)脱硫过程中使浆液pH减小最显著的反应是______________ (填①、②、③或④)。
(5)约9000s之后,脱硫效率开始急速降低,其原因是______________ 。
(6)其他条件相同时,镁基和钙基脱硫效率与液、气摩尔流量比如题图所示。镁基脱硫效率总比钙基大,除生成的MgSO4具有良好的水溶性外,还因为______________ 。

I.工业上可以采用热还原法制备金属镁(沸点1107℃,熔点648.8℃)。将碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]和焦炭按一定比例混合,放入真空管式炉中先升温至700℃保持一段时间,然后升温至1450℃反应制得镁(同时生成可燃性气体)。
(1)用碳还原法制备金属镁需要在真空中而不在空气中进行,其原因是
(2)碱式碳酸镁分解如图所示,写出在1450℃反应制得镁的化学方程式:

II.工业上利用纳米MgH2和LiBH4组成的体系储放氢(如题图所示)。

(3)写出放氢过程中发生反应的化学方程式:
III.工业上MgO浆液是高活性的脱硫剂,常用来脱除烟气中的SO2。主要包含的反应有:① Mg(OH)2+ SO2=MgSO3+H2O ② MgSO3+SO2+H2O= Mg(HSO3)2③ Mg(HSO3)2+ Mg(OH)2=2MgSO3+2H2O ④ 2MgSO3+O2=2MgSO4
脱硫时,MgO的脱硫效率、pH及时间的关系如题图所示。

已知20℃时,H2SO3的K1=l.54×10-2,K2=1.02×10-7,25℃时,Ksp[MgSO3]= 3.86×10-3,Ksp(CaSO3)= 3.1×10-7。
(4)脱硫过程中使浆液pH减小最显著的反应是
(5)约9000s之后,脱硫效率开始急速降低,其原因是
(6)其他条件相同时,镁基和钙基脱硫效率与液、气摩尔流量比如题图所示。镁基脱硫效率总比钙基大,除生成的MgSO4具有良好的水溶性外,还因为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1 mol·L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。

(1)写出OA段的离子反应方程式________
(2)写出BC段的化学方程式________
(3)合金中镁的质量__________ g。
(4)盐酸的物质的量浓度___________ mol·L-1。

(1)写出OA段的离子反应方程式
(2)写出BC段的化学方程式
(3)合金中镁的质量
(4)盐酸的物质的量浓度
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。回答下列问题。_________ ,合金中Mg与Al的物质的量之比是________ ;
(2)所加NaOH溶液的物质的量浓度是________________ ;
(3)原HCl溶液的物质的量浓度是_____________________ 。
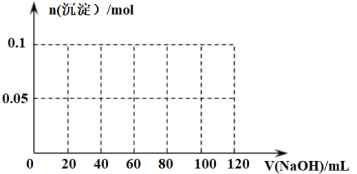
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。________
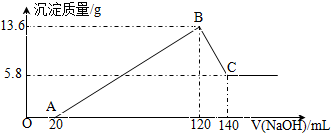
(2)所加NaOH溶液的物质的量浓度是
(3)原HCl溶液的物质的量浓度是
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】现有一定量铝粉和铁粉的混合物与一定体积稀硝酸充分反应,反应过程中无气体放出(硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入2mol∙L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量的关系如图所示。
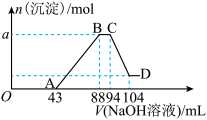
(1)写出OA段反应的离子方程式:____________________________ 。
(2)B点时溶液中含有溶质的化学式为____________ 。
(3)a的数值为__________ 。
(4)原硝酸溶液中HNO3的物质的量为__________ mol。

(1)写出OA段反应的离子方程式:
(2)B点时溶液中含有溶质的化学式为
(3)a的数值为
(4)原硝酸溶液中HNO3的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】阅读相关信息,结合所学知识,回答下列问题:
(1)铝和锌都是两性金属元素。其氢氧化物都是白色沉淀,既能溶于强酸,又能溶于强碱(生成 或ZnO
或ZnO )。但氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
)。但氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
①写出锌和氢氧化钠溶液反应的化学方程式___________ 。
②用氨水除去Al(OH)3中的Zn(OH)2的离子方程式为___________ 。
③写出向AlCl3溶液中滴入过量氨水的离子方程式___________ ;
④下列各组中的两种溶液,只用胶头滴管和试管即可鉴别的是___________ 。
A.硫酸铝和氢氧化钠 B.硫酸铝和氨水
C.硫酸锌和氢氧化钠 D.硫酸锌和氨水
(2)Cu2O是一种红色难溶于水的固体,在空气中灼烧Cu2O会生成CuO;Cu2O溶于稀硫酸可生成Cu和Cu2+;Cu2O和Cu都能溶于稀硝酸。
研究性学习小组为检测Cu样品中是否含有Cu2O设计以下实验方案:
方案Ⅰ:取该红色样品溶于足量的稀硝酸中,观察是否有残渣剩余
方案Ⅱ:取该红色样品溶于足量的稀硫酸中,观察溶液颜色变化
方案Ⅲ:称量a g红色样品,在空气中充分灼烧至恒重,得到bg黑色固体。
①比较方案Ⅰ和方案Ⅱ,你认为合理的是方案___________ (填“Ⅰ”或“Ⅱ”),合理方案的反应原理为___________ (用离子方程式表示)。
②方案Ⅲ中,如果___________ <b<___________ (用含a的代数式表示),可确认红色粉末含有Cu2O。
(1)铝和锌都是两性金属元素。其氢氧化物都是白色沉淀,既能溶于强酸,又能溶于强碱(生成
 或ZnO
或ZnO )。但氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。
)。但氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。①写出锌和氢氧化钠溶液反应的化学方程式
②用氨水除去Al(OH)3中的Zn(OH)2的离子方程式为
③写出向AlCl3溶液中滴入过量氨水的离子方程式
④下列各组中的两种溶液,只用胶头滴管和试管即可鉴别的是
A.硫酸铝和氢氧化钠 B.硫酸铝和氨水
C.硫酸锌和氢氧化钠 D.硫酸锌和氨水
(2)Cu2O是一种红色难溶于水的固体,在空气中灼烧Cu2O会生成CuO;Cu2O溶于稀硫酸可生成Cu和Cu2+;Cu2O和Cu都能溶于稀硝酸。
研究性学习小组为检测Cu样品中是否含有Cu2O设计以下实验方案:
方案Ⅰ:取该红色样品溶于足量的稀硝酸中,观察是否有残渣剩余
方案Ⅱ:取该红色样品溶于足量的稀硫酸中,观察溶液颜色变化
方案Ⅲ:称量a g红色样品,在空气中充分灼烧至恒重,得到bg黑色固体。
①比较方案Ⅰ和方案Ⅱ,你认为合理的是方案
②方案Ⅲ中,如果
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】将一定质量的Mg—Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。回答下列问题。_________ ,合金中Mg与Al的物质的量之比是________ ;
(2)所加NaOH溶液的物质的量浓度是________________ ;
(3)原HCl溶液的物质的量浓度是_____________________ 。
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。________

(2)所加NaOH溶液的物质的量浓度是
(3)原HCl溶液的物质的量浓度是
(4)向含有0.1molNH4Al(SO4)2的溶液中逐滴加入5 mol·L-1NaOH溶液,开始发现熔液中出现白色沉淀并逐渐增多;一段时间后有刺激性气味的气体(NH3)逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】分如图所示图像中,纵坐标为沉淀物的物质的量,横坐标为某溶液中加入反应物的物质的量,按试题将相应图的字母填入下列空格中,并写出所发生反应的离子方程式。

(1)表示向饱和AlCl3溶液中滴加氨水至过量的是______________ ,离子方程式:___________________ 。
(2)表示向饱和AlCl3溶液中滴加NaOH溶液至过量的是________________ ,离子方程式:___________________ ,_____________________ 。
(3)表示向饱和石灰水中通入CO2至过量的离子方程式:______________ ,________________ 。

(1)表示向饱和AlCl3溶液中滴加氨水至过量的是
(2)表示向饱和AlCl3溶液中滴加NaOH溶液至过量的是
(3)表示向饱和石灰水中通入CO2至过量的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】将一定质量的镁铝合金投入100mL一定物质的量浓度的盐酸中,若合金全部溶解,向所得溶液中滴加10.0 mol/L NaOH溶液至过量(设镁离子与铝离子同时沉淀),生成沉淀的质量与加入氢氧化钠溶液体积的关系如图所示。

(1)当加入NaOH溶液80mL到90mL时,发生反应的离子方程式为:_______ 。
(2)当沉淀达到最大值时,溶液中的溶质为_______ ,其中Al(OH)3的质量为_______ g;
(3)原盐酸的物质的量浓度为_______ mol/L;
(4)若所取盐酸的体积和浓度均保持不变,为保证加入100mL 10.0 mol/L NaOH溶液时最终无 Al(OH)3生成,则此时所取合金中含Al的物质的量即n(Al)的取值范围为_______ 。

(1)当加入NaOH溶液80mL到90mL时,发生反应的离子方程式为:
(2)当沉淀达到最大值时,溶液中的溶质为
(3)原盐酸的物质的量浓度为
(4)若所取盐酸的体积和浓度均保持不变,为保证加入100mL 10.0 mol/L NaOH溶液时最终无 Al(OH)3生成,则此时所取合金中含Al的物质的量即n(Al)的取值范围为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为________ 。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________ 、_____________ ;Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________ 。
(3)由Ⅲ中得到滤液c的实验操作为__________ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________ 、冷却结晶、过滤洗涤。
(4)滤液c显________ 性,日常生活中常用其溶质来________________ (任写一点);
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________ 。

请回答下列问题:
(1)固体a的化学式为
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式
(3)由Ⅲ中得到滤液c的实验操作为
(4)滤液c显
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为
您最近一年使用:0次



