电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4。下列判断中不正确的是
| A.阴离子的半径:X>Y>Z |
| B.单质的氧化性:X>Y>Z |
| C.元素的非金属性:X>Y>Z |
| D.气态氢化物的稳定性:X>Y>Z |
更新时间:2017-03-30 21:56:38
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X的单质是粮仓中常用的保护气;Y的+3价阳离子的核外电子排布与氖原子相同;Y和Z原子的最外层电子数之和等于W原子的最外层电子数;Z原子核外电子数是W原子最外层电子数的2倍。下列说法正确的是
| A.原子半径:r(Y)<r(X)<r(W)<r(Z) |
| B.元素X的最高价含氧酸的酸性比Z的强 |
| C.电解Y、W形成的化合物可制取Y单质 |
| D.Z的简单气态氢化物的热稳定性比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,N和Z的原子序数之差为8。下列说法正确的是
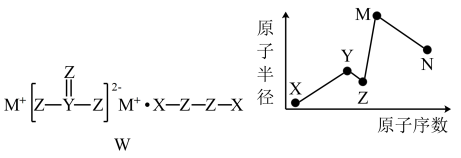

| A.X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 |
| B.可通过比较Y单质与N单质的还原性强弱来判断Y、N的非金属性强弱 |
| C.Z的氢化物的沸点一定大于Y的氢化物的沸点 |
| D.化合物W常用作氧化剂,宜在高温下使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验方案设计现象和结论都正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将 溶于水,进行导电性实验 溶于水,进行导电性实验 |  溶液可导电 溶液可导电 | 由此可证明 中含有离子键 中含有离子键 |
| B | 在试管中仅加入 无水乙醇和 无水乙醇和 冰醋酸,混合后,酒精灯缓缓加热,将产生的蒸汽经导管通入到饱和碳酸钠溶液中,反应结束后充分振荡盛有饱和碳酸钠溶液的试管 冰醋酸,混合后,酒精灯缓缓加热,将产生的蒸汽经导管通入到饱和碳酸钠溶液中,反应结束后充分振荡盛有饱和碳酸钠溶液的试管 | 溶液分层 | 制备获得乙酸乙酯 |
| C | 加热铜与浓硫酸的混合物,充分反应后冷却,将试管里的物质慢慢倒入盛水的烧杯中 | 试管底部有灰白色固体,稀释后溶液变蓝 | 浓硫酸具有氧化性,与铜反应生成硫酸铜 |
| D | 用pH试纸分别测定等物质的量浓度的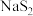 和 和 溶液的pH 溶液的pH | 前者pH大 | 非金属性:S<Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z为原子序数依次增大的短周期主族元素,Y的原子序数等于W与X的原子序数之和,Z的最外层电子数为K层的一半,W与X可形成原子个数比为2:1的18e-分子。下列说法错误的是
| A.简单离子半径:X>Y>Z |
| B.W与Y能形成含有非极性键的化合物 |
| C.X和Y的最简单氢化物的沸点:Y>X |
| D.由W、X、Y三种元素所组成化合物的水溶液均显酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】我国科学家用如图所示大阴离子的盐作水系锌离子电池的电解质溶液,显示了优良的循环性能。X、Y、Z、W均为短周期元素且原子序数依次增大,其中X、Y、Z位于同一周期,Y、W核外最外层电子数相等。下列叙述正确的是
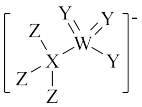

| A.简单离子半径大小顺序为W>Z>Y |
| B.W氧化物对应的水化物是一定是强酸 |
| C.X氢化物的沸点一定低于W氢化物的沸点 |
| D.X和Z形成的简单化合物各原子均满足8电子稳定结构 |
您最近一年使用:0次

 ,其中W、X、Y、Z为原子半径依次增大的短周期非金属元素,W位于元素周期表的p区。下列说法正确的是
,其中W、X、Y、Z为原子半径依次增大的短周期非金属元素,W位于元素周期表的p区。下列说法正确的是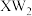 中元素X为
中元素X为 杂化
杂化

