共价键都有键能之说,键能是指拆开1 mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。
(1)已知H—Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是______________。
(2)参考下表中的数据,判断下列分子受热时最稳定的是___________。
(3)能用键能大小解释的是____________。
(4)已知:4HCl+O2=2Cl2+2H2O,常温下,4mol HCl被氧化,放出115.6kJ的热量.写出该反应的热化学方程式_____________________ .
(5)在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的ΔH表示生成1mol产物的数据)
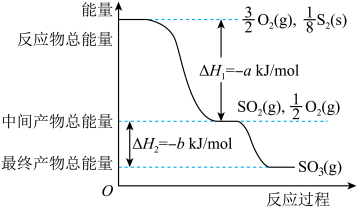
①写出表示S8燃烧热的热化学方程式:______________ .
②写出SO3分解生成SO2和O2的热化学方程式:______________ .
(1)已知H—Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是______________。
| A.每生成1 mol H—Cl键吸收431.4 kJ能量 |
| B.每生成1 mol H—Cl键放出431.4 kJ能量 |
| C.每拆开1 mol H—Cl键放出431.4 kJ能量 |
| D.每拆开1 mol H—Cl键吸收431.4 kJ能量 |
化学键 | H—H | H—F | H—Cl | H—Br |
键能/kJ/mol | 436 | 565 | 431 | 368 |
| A.H2 | B.HF | C.HCl | D.HBr |
| A.常温常压下,溴呈液态,碘呈固态 | B.氮气的化学性质比氧气稳定 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
(5)在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的ΔH表示生成1mol产物的数据)

①写出表示S8燃烧热的热化学方程式:
②写出SO3分解生成SO2和O2的热化学方程式:
更新时间:2017-04-09 14:50:36
|
相似题推荐
【推荐1】完成下列小题
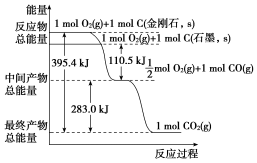
(1)金刚石和石墨在燃烧时,若氧气不足生成一氧化碳,若氧气充足生成二氧化碳,反应中放出的热量如图所示。______ (填“金刚石”或“石墨”)放出的热量更多,在通常状况下,______ (填“金刚石”或“石墨”)更稳定,1mol石墨完全转化为金刚石的反应______ (填“吸收”或“释放”)______ kJ热量,断开1mol石墨中的化学键所吸收的能量______ (填“大于”或“小于”)断开1mol金刚石中的化学键所吸收的能量。
(2)将V1mL1.0mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50)。______ (填“吸收”或“释放”)能量,通过上图分析可以得出,做该实验时,环境温度______ (填“高于”“低于”或“等于”)22℃。
②根据上图可以得出,该NaOH溶液的浓度约是______ 。
(1)金刚石和石墨在燃烧时,若氧气不足生成一氧化碳,若氧气充足生成二氧化碳,反应中放出的热量如图所示。
(2)将V1mL1.0mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50)。
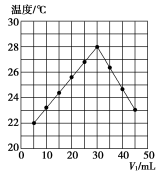
②根据上图可以得出,该NaOH溶液的浓度约是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮及其化合物在人们的生活经常出现
(1)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,1mol N2和1molO2完全反应生成NO,会_______________ (填“吸收”或“放出”)________ kJ能量。
(2)一定温度下,在体积为0.5 L的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。
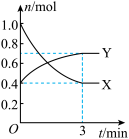
①该反应的化学反应方程式:______________________ 。
②在0~3 min内,用Y表示的反应速率为____________ 。
③下列叙述能说明该反应已达到化学平衡状态的是________ (填字母)。
a.容器内压强不再发生变化
b.X的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolY的同时生成2nmol X
④反应达到平衡后,若降低温度,则υ(正)______ ,υ(逆)________ 。(填“增大”“减小”或“不变”)。
(3)反应 A(g)+3B(g)═2C(g)+3D(g)在四种不同情况下的反应速率分别为:
①υ (A)=0.015mol (L•s)﹣1 ②υ (B)=0.09mol (L•s)﹣1
③υ (C)=2.4mol (L•min )﹣1 ④υ (D)=0.045mol (L•s)﹣1
该反应在四种不同情况下速率由大到小的顺序为(用序号填空)________ 。
(1)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,1mol N2和1molO2完全反应生成NO,会
(2)一定温度下,在体积为0.5 L的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。

①该反应的化学反应方程式:
②在0~3 min内,用Y表示的反应速率为
③下列叙述能说明该反应已达到化学平衡状态的是
a.容器内压强不再发生变化
b.X的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolY的同时生成2nmol X
④反应达到平衡后,若降低温度,则υ(正)
(3)反应 A(g)+3B(g)═2C(g)+3D(g)在四种不同情况下的反应速率分别为:
①υ (A)=0.015mol (L•s)﹣1 ②υ (B)=0.09mol (L•s)﹣1
③υ (C)=2.4mol (L•min )﹣1 ④υ (D)=0.045mol (L•s)﹣1
该反应在四种不同情况下速率由大到小的顺序为(用序号填空)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O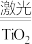 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)分解海水时,实现了从_______ 能转变为_______ 能,二氧化钛作_______ 。
(2)生成的氢气用于燃料电池时,实现_______ 能转变为_______ 能。
(3)水分解时,断裂的化学键为_______ 键,分解海水的反应属于_______ (填“放热”或“吸热”)反应。
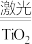 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:(1)分解海水时,实现了从
(2)生成的氢气用于燃料电池时,实现
(3)水分解时,断裂的化学键为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学反应中伴随着能量变化。
(1)下列反应中,属于吸热反应的是_______。
(2)按下图所示装置进行实验。
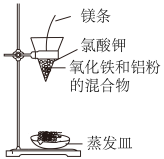
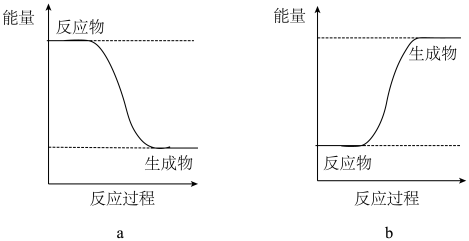
【实验现象】反应剧烈,火星四射,漏斗下方有红热熔融物流出。由此判断该反应是_______ (填“吸热”或“放热”)反应,其反应的化学方程式是_______ ,其能量变化可用图中的_______ (填“a”或“b”)表示。
(3)依据事实,写出下列反应的热化学方程式。
①已知拆开1molH﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
②25℃时,1gCH4气体完全燃烧生成二氧化碳和液态水,放出55.6kJ的热量,该反应的热化学方程式为_______ 。
③已知:P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+ O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1
P4O10(s) ΔH=-738.5kJ·mol-1
则白磷转化为红磷的热化学方程式为_______ 。
(1)下列反应中,属于吸热反应的是_______。
| A.燃烧CO |
| B.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 |
| C.铝和稀盐酸反应 |
| D.NaOH溶液和稀盐酸反应 |

【实验现象】反应剧烈,火星四射,漏斗下方有红热熔融物流出。由此判断该反应是

(3)依据事实,写出下列反应的热化学方程式。
①已知拆开1molH﹣H键,1molN﹣H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
②25℃时,1gCH4气体完全燃烧生成二氧化碳和液态水,放出55.6kJ的热量,该反应的热化学方程式为
③已知:P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2kJ·mol-1
P(红磷,s)+
 O2(g)=
O2(g)= P4O10(s) ΔH=-738.5kJ·mol-1
P4O10(s) ΔH=-738.5kJ·mol-1则白磷转化为红磷的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
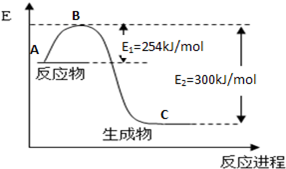
(1)上图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:_______ 。
(2)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g) 2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a
2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a_______ (填“增大”“减小”或“不变”)。
(3)用NH3催化还原NOx可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ/mol①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ/mol②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=_______ kJ·mol-1(用含a、b的式子表示)。
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=—25 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=—47 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:_______ 。

(1)上图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:
(2)NO与CO反应的热化学方程式可以表示为2NO(g)+2CO(g)
 2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a
2CO2(g)+N2(g)ΔH=a kJ/mol,但该反应的速率很小,若使用机动车尾气催化转化器,尾气中的NO与CO可以转化成无害物质排出。上述反应在使用“催化转化器”后,a(3)用NH3催化还原NOx可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ/mol①
N2(g)+O2(g)=2NO(g) ΔH2=-b kJ/mol②
若1molNH3还原NO至N2,则该反应过程中的反应热ΔH3=
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=—25 kJ/mol
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=—47 kJ/mol
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)实验测得,5 g 液态甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 113.5 kJ 的热量,试写出甲醇燃烧的热化学方程式_______ 。
(2)今有如下两个热化学方程式:则 a_______ b(选填“>”、“ < ”或“ = ”)
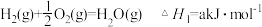

(3)由气态基态原子形成 1 mol 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
已知反应 。试根据表中所列键能数据估算 a 的值:
。试根据表中所列键能数据估算 a 的值: _______ 。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知: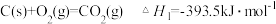
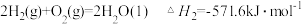

根据盖斯定律,计算 298 K 时由 C(s)和 H2(g)生成 1 mol C2H2(g)反应的反应热△H =_______ 。
(1)实验测得,5 g 液态甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 113.5 kJ 的热量,试写出甲醇燃烧的热化学方程式
(2)今有如下两个热化学方程式:则 a
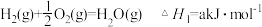

(3)由气态基态原子形成 1 mol 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应
 。试根据表中所列键能数据估算 a 的值:
。试根据表中所列键能数据估算 a 的值: (4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:
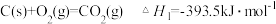
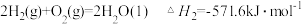

根据盖斯定律,计算 298 K 时由 C(s)和 H2(g)生成 1 mol C2H2(g)反应的反应热△H =
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列物质的电子式:
①CaO______
②NaOH______
③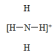
______
①CaO
②NaOH
③
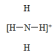
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列各题:
(1)用电子式表示H2O和MgBr2的形成过程:H2O_____ ;MgBr2______ .
(2)写出CO2、Na2O2的电子式:CO2_______ 、Na2O2______ .
(3)A+、B+、C-、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:
①A++C-→D+E:②B++C-→2D。据此,写出①反应的离子方程式________ .
(1)用电子式表示H2O和MgBr2的形成过程:H2O
(2)写出CO2、Na2O2的电子式:CO2
(3)A+、B+、C-、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:
①A++C-→D+E:②B++C-→2D。据此,写出①反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空。
(1)电子式: O2:_______ CO2:_______ NH4Cl:_______ Mg(OH)2:_______
(2)用电子式写出K2S的形成过程_______ 。
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是_______ (填序号,下同),属于电解质的是_______ ,上述条件下能导电的是_______ 。
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是_______ (填序号,下同),互为同素异形体的一组是_______ 。
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成_______ 种不同的氯化氢分子,其对应的相对分子质量有_______ 种。
(1)电子式: O2:
(2)用电子式写出K2S的形成过程
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成
您最近一年使用:0次



