下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 操 作 | 现 象 | 解释或结论 |
| A | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大Cl-浓度,平衡逆向移动 |
| B | 将氯化铝溶液蒸干 | 析出白色固体 | 白色固体是氯化铝 |
| C | 向某溶液中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| D | 石蕊试液中通入氯气 | 溶液先变红后红色褪去 | 氯气与水反应产生了酸和漂白性物质 |
| A.A | B.B | C.C | D.D |
更新时间:2017/04/15 17:42:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于离子或物质的鉴别,判断正确的是
A.加入BaCl2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解,可确定有SO 存在 存在 |
| B.向某无色溶液中滴入酚酞试液后显红色,该溶液一定是碱溶液 |
C.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可能有CO 存在 存在 |
D.在某固体试样加水后的溶液中,滴加NaOH溶液,没有产生使湿润的红色石蕊试纸变蓝的气体,则该固体试样中不含NH |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作或设计与实验现象。结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 取少量某溶液于试管中,加入NaOH浓溶液并加热,用湿润的红色石蕊试纸检验产生气体 | 湿润的红色石蕊试纸变蓝 | 溶液中一定含有 |
| B | 向20.00mL浓度为 的 的 溶液中逐滴加入等浓度的 溶液中逐滴加入等浓度的 溶液 溶液 | 溶液褪色 |  漂白溶液,表现强氧化性 漂白溶液,表现强氧化性 |
| C | 取少量固体 样品溶于蒸馏水,加入足量稀盐酸,再加入适量 样品溶于蒸馏水,加入足量稀盐酸,再加入适量 溶液 溶液 | 白色沉淀产生 | 样品没有变质 |
| D | 向盛有 溶液的甲试管中滴入盐酸,将生成的气体通入盛有 溶液的甲试管中滴入盐酸,将生成的气体通入盛有 的乙试管中 的乙试管中 | 乙试管中有沉淀生成 | 酸性: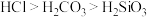 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某无色溶液中可能含有 CrO 、NH
、NH 、SO
、SO 、Mg2+、Al3+、K+、SO
、Mg2+、Al3+、K+、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入 1 mL 该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH 溶液至过量,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是
中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入 1 mL 该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH 溶液至过量,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是
 、NH
、NH 、SO
、SO 、Mg2+、Al3+、K+、SO
、Mg2+、Al3+、K+、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入 1 mL 该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH 溶液至过量,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是
中的一种或几种,已知所含离子的物质的量浓度相等。取甲、乙两支试管分别加入 1 mL 该溶液进行如下实验:①向甲中加入适量稀盐酸,无明显现象;②向乙中逐滴滴加NaOH 溶液至过量,现象为先有白色沉淀产生,进而产生刺激性气味气体,最后白色沉淀完全溶解。对于该溶液中的离子成分,下列说法正确的是A.一定含有 NH 、Al3+、SO 、Al3+、SO 、Cl-、NO 、Cl-、NO |
B.一定不含 CrO 、SO 、SO 、Mg2+、NO 、Mg2+、NO |
C.可能含有 Mg2+、K+、Cl-、NO |
D.一定不含 CrO 、SO 、SO 、Mg2+、SO 、Mg2+、SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列由离子检验有关的实验得出的结论正确的是
选项 | 实验 | 结论 |
A | 溶液X的焰色试验呈黄色 | 溶液X中一定有 ,一定没有 ,一定没有 |
B | 取少量溶液Y于试管中,滴加 溶液后,再滴加 溶液后,再滴加 溶液,溶液变为红色 溶液,溶液变为红色 | 溶液Y中一定有 ,一定没有 ,一定没有 |
C | 取少量溶液Z,向其中加入少量盐酸酸化的 溶液,有白色沉淀产生、无气体生成 溶液,有白色沉淀产生、无气体生成 | 溶液Z中一定有 ,一定没有 ,一定没有 |
D | 取少量溶液W,加入少量淀粉,无明显现象,向其中加入新制氯水,溶液变蓝 | 溶液W中一定有 ,一定没有 ,一定没有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法错误 的是( )。
①向NaClO溶液中滴入少量FeSO4溶液,反应的离子方程式为2Fe2++ClO-+2H+ Cl-+2Fe3++H2O
Cl-+2Fe3++H2O
②向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液,溶液变成血红色,说明Fe2+既有氧化性又有还原性
③将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,有气体生成,溶液呈血红色,则稀硝酸将Fe氧化成了Fe3+
④向某溶液中滴加氯水后再加入KSCN溶液,若溶液呈红色,则溶液中一定含有Fe2+
⑤在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
①向NaClO溶液中滴入少量FeSO4溶液,反应的离子方程式为2Fe2++ClO-+2H+
 Cl-+2Fe3++H2O
Cl-+2Fe3++H2O②向FeSO4溶液中先滴入KSCN溶液,再滴加H2O2溶液,溶液变成血红色,说明Fe2+既有氧化性又有还原性
③将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,有气体生成,溶液呈血红色,则稀硝酸将Fe氧化成了Fe3+
④向某溶液中滴加氯水后再加入KSCN溶液,若溶液呈红色,则溶液中一定含有Fe2+
⑤在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
| A.①②③④ | B.①②③④⑤ |
| C.②③④ | D.②③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】第三周期元素的单质及其化合物具有重要用途。在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品;Al-空气电池具有较高的比能量,在碱性电解液中总反应式为4Al+3O2+6H2O=4[Al(OH)4]-;高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(SiHCl3),再经H2还原得到高纯硅。下列化学反应的表示方法正确的是
| A.钠与水反应的离子方程式:Na+H2O=Na++2OH-+H2↑ |
| B.MgCl2溶液显酸性的原因:Mg2++2H2O=Mg(OH)2↓+2H+ |
| C.该Al-空气电池的负极反应式:Al-3e-+3OH-=Al(OH)3 |
D.SiHCl3转化为高纯硅的化学方程式:SiHCl3+H2 Si+3HCl Si+3HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学用语可以表达化学过程,下列化学用语的表述错误 的是
A.用电子式表示 的形成: 的形成: |
B.用电子轮廓图表示 的 的 键形成的示意图: 键形成的示意图: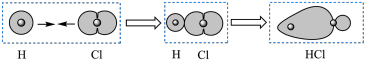 |
C.用离子方程式表示泡沫灭火器的工作原理: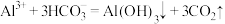 |
D.苯酚和甲醛在酸性条件下反应能生成酚醛树脂: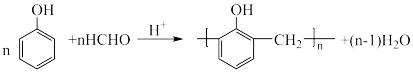 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验的叙述正确的是
| A.分液时分液漏斗的下端与过滤时漏斗的下端均要贴紧烧杯内壁,其原因不相同 |
| B.胶体的分散质粒子直径大小介于溶液与浊液之间 |
| C.配制一定物质的量浓度溶液时,在溶解、移液、洗涤、定容时均要用到玻璃棒 |
| D.不用其它试剂,只用胶头滴管和试管即可鉴别出NaHCO3、Ba(OH)2、稀H2SO4三种溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:碳酸氢钠受热易分解:2NaHCO3 Na2CO3+CO2↑+H2O;碳酸钠Na2CO3热稳定性较好,受热不易分解。用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实验目的的是( )
Na2CO3+CO2↑+H2O;碳酸钠Na2CO3热稳定性较好,受热不易分解。用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实验目的的是( )
 Na2CO3+CO2↑+H2O;碳酸钠Na2CO3热稳定性较好,受热不易分解。用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实验目的的是( )
Na2CO3+CO2↑+H2O;碳酸钠Na2CO3热稳定性较好,受热不易分解。用如图装置(加热及夹持仪器已略去)进行的实验,下列不能达到相应实验目的的是( )| 选项 | A | B | C | D |
| 装置 | 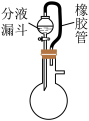 | 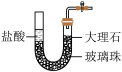 | 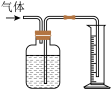 | 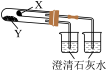 |
| 实验目的 | 分液漏斗内的液体可顺利加入蒸馏烧瓶 | 可实现制取CO2实验中的“即开即用,即关即止”的作用 | 用排水法收集并测量生成O2的体积 | 验证NaHCO3和Na2CO3的热稳定性,X中应放的物质是Na2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液中加入Zn片
溶液中加入Zn片 强
强 溶液中滴加KSCN溶液,再加入少量
溶液中滴加KSCN溶液,再加入少量 固体
固体 溶液,持续煮沸
溶液,持续煮沸 再聚集成
再聚集成

