将32.0 gCu投入50mL 12moL/L的浓硝酸中,充分反应后,收集到4.48L(标准状况)NO和NO2的混合气体。
(1)被还原硝酸的物质的量是_________ mol。
(2)判断32.0gCu和50mL 12moL/L的硝酸反应后有剩余的是___________ ,剩余的物质物质的量为________________ ,生成的NO气体体积为(标况下)_________________ 。
(3)如果往反应后的体系内再加入100mL2mol/L的稀硫酸,充分反应后又有气体逸出。写出反应的离子方程式并用单线桥法表示电子转移的方向和数目_______________________ 。
(1)被还原硝酸的物质的量是
(2)判断32.0gCu和50mL 12moL/L的硝酸反应后有剩余的是
(3)如果往反应后的体系内再加入100mL2mol/L的稀硫酸,充分反应后又有气体逸出。写出反应的离子方程式并用单线桥法表示电子转移的方向和数目
更新时间:2017-04-23 12:03:05
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】把3.04g某铁的氧化物FexO分成两等份,第一份溶于足量盐酸后向溶液中通入标准状况下Cl2112mL,恰好将Fe2+完全氧化;第二份混合物中加入100mL氢碘酸溶液,恰好完全反应,在反应后的溶液中加KSCN溶液,无现象。试计算:
(1)x的值为___________ 。
(2)氢碘酸溶液的物质的量浓度c(HI)___________ 。
(1)x的值为
(2)氢碘酸溶液的物质的量浓度c(HI)
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】大气污染物中的氮氧化物可用NaOH吸收,发生如下反应:


请计算:
(1)若33.6mL(标况下)氮氧化物(只含NO和 )与
)与 恰好完全反应,则
恰好完全反应,则
_______ 。
(2)若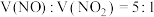 与
与 混合,能与
混合,能与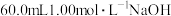 溶液恰好完全反应全部转变成
溶液恰好完全反应全部转变成 ,则
,则
_______ (写出计算过程)


请计算:
(1)若33.6mL(标况下)氮氧化物(只含NO和
 )与
)与 恰好完全反应,则
恰好完全反应,则
(2)若
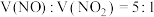 与
与 混合,能与
混合,能与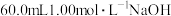 溶液恰好完全反应全部转变成
溶液恰好完全反应全部转变成 ,则
,则
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】硝酸发生氧化还原反应的时候,一般硝酸浓度越稀,对应还原产物中氮的化合价越低。若硝酸现有一定量的铝粉和铁粉的混合物与一定量很稀的HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4mol /LNaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。求:
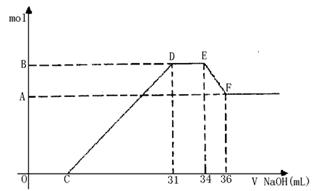
(1)B与A的差值: mol;
(2)B的数值: mol;
(3)C的数值: mL。(要求有计算过程)

(1)B与A的差值: mol;
(2)B的数值: mol;
(3)C的数值: mL。(要求有计算过程)
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,生成的气体为NO、 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗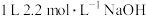 溶液和
溶液和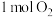 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为_______ 、_______ ,生成硫酸铜的物质的量为_________________ 。
 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗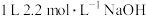 溶液和
溶液和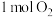 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3- 离子物质的量变化如下图所示,请回答下列问题:
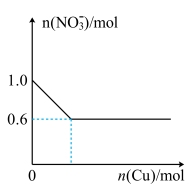
(1)开始反应时浓硝酸的物质的量浓度为____________ mol/L 。
(2)铜与浓硝酸反应生成的气体在标准状况下的体积(不考虑NO2与N2O4的平衡)为_____ L。
(3)硝酸完全反应后消耗铜的物质的量n(Cu)是______ mol。
(4)应再往此反应体系中滴加_________ L 2 mol/L的硫酸才能使剩余的铜恰好完全溶解。已知此过程中NO3-的还原产物为NO。
(5)a g铜全部溶于一定量的浓硝酸中,测得生成的气体在标准状况下的体积(不考虑NO2与N2O4的平衡)为b L,为消除污染,将生成的气体通入NaOH溶液中,气体被完全吸收。已知:NO + NO2 +2NaOH →2NaNO2 + H2O 2NO2 +2NaOH → NaNO3 +NaNO2 + H2O如果NO、NO2混合气体用NOx表示,被NaOH溶液完全吸收时,x的取值范围______ ;生成NaNO2的物质的量是_________ mol;NaNO3的物质的量是_________ mol。
(6)在常温下,把NO气体压缩到1.01×107Pa,再加热到500C,发现气体的压强迅速下降,压强降至略小于原压强的2/3,然后压强就不再改变。已知其中一种产物为N2O,则上述变化的化学方程式为__________________ 。气体的平均摩尔质量为M,则M的取值范围应该是_________________ 。

(1)开始反应时浓硝酸的物质的量浓度为
(2)铜与浓硝酸反应生成的气体在标准状况下的体积(不考虑NO2与N2O4的平衡)为
(3)硝酸完全反应后消耗铜的物质的量n(Cu)是
(4)应再往此反应体系中滴加
(5)a g铜全部溶于一定量的浓硝酸中,测得生成的气体在标准状况下的体积(不考虑NO2与N2O4的平衡)为b L,为消除污染,将生成的气体通入NaOH溶液中,气体被完全吸收。已知:NO + NO2 +2NaOH →2NaNO2 + H2O 2NO2 +2NaOH → NaNO3 +NaNO2 + H2O如果NO、NO2混合气体用NOx表示,被NaOH溶液完全吸收时,x的取值范围
(6)在常温下,把NO气体压缩到1.01×107Pa,再加热到500C,发现气体的压强迅速下降,压强降至略小于原压强的2/3,然后压强就不再改变。已知其中一种产物为N2O,则上述变化的化学方程式为
您最近半年使用:0次
【推荐1】48g CuS和Cu2S的混合物投入足量HNO3中,得到蓝色澄清溶液,并收集到NO和N2O的混合气体10.08L(折算到标准状况),向反应后的溶液中加入足量氢氧化钡溶液,产生沉淀,过滤,洗涤,灼烧,得到固体的质量范围为____________ 。
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________ g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________ 。
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______ L。
(1)m=
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将20.0 g铜镁合金完全溶解于140 mL某浓度的硝酸中,得到NO2和NO的混合气体8.96 L(标准状况),当向反应后的溶液中加入320 mL 4.0 mol/L NaOH溶液时,金属离子全部转化为沉淀,测得沉淀的质量为37 g。通过计算回答下列问题:
(1)该合金中铜与镁的物质的量之比是_______ 。
(2)该硝酸中HNO3的物质的量浓度是_______ mol/L。
(3)NO2和NO的混合气体中,NO2的体积分数是_______ 。
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为_______ L。
(1)该合金中铜与镁的物质的量之比是
(2)该硝酸中HNO3的物质的量浓度是
(3)NO2和NO的混合气体中,NO2的体积分数是
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)有Mg、Al混合粉末10.2 g溶于50 mL 4 mol·L-1的盐酸,若加入2mol·L-1的氢氧化钠溶液,使得沉淀达到最大量,则需加入氢氧化钠的体积为_____ mL。
(2)标准状况下,将足量的Zn投入到一定量的浓硫酸中,完全反应后,收集到336 mL气体,将该气体通入足量氯水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知该气体中SO2的体积分数为________ 。
(3)某化学学习小组在进行知识整理时发现如下规律:有些反应随着溶液由浓变稀,可能导致“量变引起质变”,并据此拟定了如下几个相关题目,请你给出相应答案。
I.实验室制取氯气的化学方程式为MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑(MnO2不能氧化稀盐酸)。用下列两种方法制取氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量的浓盐酸反应。不考虑HCl的挥发,则两种方法生成的氯气的量是方法①
MnCl2+2H2O+Cl2↑(MnO2不能氧化稀盐酸)。用下列两种方法制取氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量的浓盐酸反应。不考虑HCl的挥发,则两种方法生成的氯气的量是方法①____ (填“>”、“<”或“=”)方法②。
II.用100 mL、18 mol·L-1的浓硫酸与足量的铜充分反应后,溶液中硫酸根离子的物质的量____ (填“>”、“<”或“=”)0.9 mol。
(2)标准状况下,将足量的Zn投入到一定量的浓硫酸中,完全反应后,收集到336 mL气体,将该气体通入足量氯水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知该气体中SO2的体积分数为
(3)某化学学习小组在进行知识整理时发现如下规律:有些反应随着溶液由浓变稀,可能导致“量变引起质变”,并据此拟定了如下几个相关题目,请你给出相应答案。
I.实验室制取氯气的化学方程式为MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑(MnO2不能氧化稀盐酸)。用下列两种方法制取氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量的浓盐酸反应。不考虑HCl的挥发,则两种方法生成的氯气的量是方法①
MnCl2+2H2O+Cl2↑(MnO2不能氧化稀盐酸)。用下列两种方法制取氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量的浓盐酸反应。不考虑HCl的挥发,则两种方法生成的氯气的量是方法①II.用100 mL、18 mol·L-1的浓硫酸与足量的铜充分反应后,溶液中硫酸根离子的物质的量
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】有一硫酸和硝酸的混合溶液,取出20mL,加入足量BaCl2溶液,经过滤、洗涤、烘干后得沉淀9.32g;滤液与4mol/L的苛性钠溶液35mL恰好完全中和。试求:
(1)原混合溶液中硫酸和硝酸的物质的量浓度。__________
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)__________
(3)另取10mL原溶液,加入1.92g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)__________
(4)向(3)反应后的溶液中加入多少毫升1mol/L硫酸就能将1.92g铜恰好完全溶解?__________
(1)原混合溶液中硫酸和硝酸的物质的量浓度。
(2)另取10mL原溶液,加入0.96g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)
(3)另取10mL原溶液,加入1.92g铜粉共热,生成一氧化氮的体积为多少?(S.T.P.)
(4)向(3)反应后的溶液中加入多少毫升1mol/L硫酸就能将1.92g铜恰好完全溶解?
您最近半年使用:0次

 与KI反应完全。以淀粉为指示剂,逐滴滴加
与KI反应完全。以淀粉为指示剂,逐滴滴加 的
的 溶液5.00mL,达到滴定终点(反应为
溶液5.00mL,达到滴定终点(反应为 )。
)。

