某同学想通过下图装置实验,探究 SO2 与 Na2O2反应的产物。
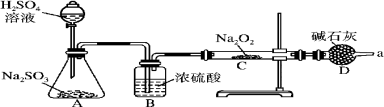
Ⅰ、检验反应中是否有 O2 生成的方法是_______________________________________ ;若有 O2 生成,请写出装置 C 中的化学方程式:________________________ 。
Ⅱ、A 中盛装 H2SO4 溶液的仪器名称是________ ;D 装置除起了防止空气中的水蒸气和二氧化碳进入 C 装置与 Na2O2 反应作用外,还可以________________________________ 。
Ⅲ、(1)C 中固体产物可能有三种情况:①只有 Na2SO3;②只有________ ;③Na2SO3 和 Na2SO4 混合物。
(2)若 Na2O2 反应完全,为确定 C 中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程。限选试剂和仪器:
0.01 mol·L-1 KMnO4酸性溶液 0.1 mol·L-1 Ba(NO3)2 溶液 0.1 mol·L BaCl2
1 mol·L-1 HNO3 溶液 1 mol·L-1 盐酸、试管、胶头滴管。

Ⅰ、检验反应中是否有 O2 生成的方法是
Ⅱ、A 中盛装 H2SO4 溶液的仪器名称是
Ⅲ、(1)C 中固体产物可能有三种情况:①只有 Na2SO3;②只有
(2)若 Na2O2 反应完全,为确定 C 中固体产物的成分,该同学设计如下,请您利用限选试剂和仪器帮助他完成该探究过程。限选试剂和仪器:
0.01 mol·L-1 KMnO4酸性溶液 0.1 mol·L-1 Ba(NO3)2 溶液 0.1 mol·L BaCl2
1 mol·L-1 HNO3 溶液 1 mol·L-1 盐酸、试管、胶头滴管。
| 实验操作 | 预期现象和结论 |
| 步骤一:取少量 C 中固体产物 于试管中,加入适量的蒸馏水、 搅拌溶解,分别取少量于 A、B 试管中 | 固体完全溶解,得到无色透明溶液 |
| 步骤二:取试管 A,向溶液中 加入 | |
| 步骤三:取试管 B,向其中先 加入 荡;再加入 | 产生气泡 ,再加入 另一试剂看到产生白色沉淀, 则固体 C 中还含有 |
更新时间:2017-04-21 21:38:48
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】无机物 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质;上述物质在一定条件下可以发生如下转化。
是单质;上述物质在一定条件下可以发生如下转化。
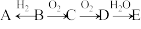
(1)若 为强碱,则A的电子式为
为强碱,则A的电子式为___________ 。
(2)若 为强酸,D在标准状况下是白色固体,则:
为强酸,D在标准状况下是白色固体,则:
① 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式___________ 。
②实验室检验 的酸根离子的方法是
的酸根离子的方法是___________ 。
(3)若 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:
① 为
为___________ 。
②工业上制备C的化学方程式___________ 。
 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质;上述物质在一定条件下可以发生如下转化。
是单质;上述物质在一定条件下可以发生如下转化。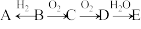
(1)若
 为强碱,则A的电子式为
为强碱,则A的电子式为(2)若
 为强酸,D在标准状况下是白色固体,则:
为强酸,D在标准状况下是白色固体,则:①
 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式②实验室检验
 的酸根离子的方法是
的酸根离子的方法是(3)若
 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:①
 为
为②工业上制备C的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某同学为了验证Fe3+是否能将H2SO3氧化成SO42-,用50 mL 0.1 mol·L-1 FeCl3溶液吸收制取SO2气体的尾气后,进行以下实验:
(1)检验吸收液中的SO42-操作为____________________________________________________ ,证明Fe3+能够把H2SO3氧化成SO42-。
(2)请配平并完成上述反应中的化学方程式:2FeCl3+SO2+________ ===________ +H2SO4+________ ,反应中的氧化产物是________ (写化学式)。
(3)吸收液中除了含有H+、Cl-、SO42-以外,对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:溶液中存在Fe2+;
假设2:溶液中存在Fe3+、Fe2+;
假设3:溶液中存在_________________________________________ 。
②设计方案,进行实验,验证假设。请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1 mol·L-1 KMnO4溶液、0.1 mol·L-1 KSCN溶液、品红稀溶液。
(1)检验吸收液中的SO42-操作为
(2)请配平并完成上述反应中的化学方程式:2FeCl3+SO2+
(3)吸收液中除了含有H+、Cl-、SO42-以外,对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:溶液中存在Fe2+;
假设2:溶液中存在Fe3+、Fe2+;
假设3:溶液中存在
②设计方案,进行实验,验证假设。请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1 mol·L-1 KMnO4溶液、0.1 mol·L-1 KSCN溶液、品红稀溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3 mL,并滴入 | 若出现红色,则假设2成立,1、3不成立;若未出现红色,则假设2不成立,假设1或3成立 |
| 步骤2: | |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸铵是一种无机物,化学式为(NH4)2SO4,白色颗粒,无气味,受热易分解。某化学研究小组拟探究其在400℃时的分解产物。实验装置如图所示(部分夹持装置已略去):
(1)仪器a的名称是_______ 。
(2)先关闭止水夹n,打开止水夹m,400℃加热装置C,装置E中品红溶液褪色,证明分解产物中含有_______ (填化学式),品红溶液褪色说明其具有_______ 。然后打开n,关闭m,装置A中的现象是_______ ,说明分解产物有氨气生成,碱石灰的作用是_______ ,400℃加热装置C至(NH4)2SO4完全分解无残留物,停止加热,进一步研究发现,气体产物中有N2生成。
(3)装置D内稀盐酸吸收的气体是_______ (填化学式)。
(4)检验装置 内溶液中有
内溶液中有 、无
、无 的实验操作和现象是
的实验操作和现象是_______ 。
(5)(NH4)2SO4在400℃分解的化学方程式是_______ 。

(1)仪器a的名称是
(2)先关闭止水夹n,打开止水夹m,400℃加热装置C,装置E中品红溶液褪色,证明分解产物中含有
(3)装置D内稀盐酸吸收的气体是
(4)检验装置
 内溶液中有
内溶液中有 、无
、无 的实验操作和现象是
的实验操作和现象是(5)(NH4)2SO4在400℃分解的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室常用Na2O2与H2O反应快速制取少量O2。用如图所示装置制取O2并进行Na在O2中燃烧的实验。请回答下列问题:
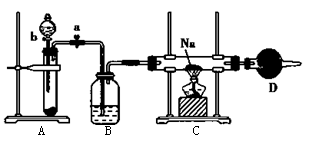
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中的液体不断往下滴,直至全部流入试管。试判断装置是否漏气__________ (填“漏气"“不漏气”或“无法确定”),说明理由:_____________________ 。
(2)写出A装置中所发生反应的化学方程式_______________________________ 。
(3)C装置中观察到的现象是__________ 。
(4)D装置中盛放的试剂是__________ ,其作用是__________ 。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中的液体不断往下滴,直至全部流入试管。试判断装置是否漏气
(2)写出A装置中所发生反应的化学方程式
(3)C装置中观察到的现象是
(4)D装置中盛放的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Na2O2是重要的化工原料,具有多种用途。
(1)Na2O2具有氧化性,可以将SO2氧化为硫酸钠,写出该反应的化学方程式:________ 。该反应中Na2O2的作用为________ (填写字母编号)。
a.还原剂 b.氧化剂 c.既是氧化剂又是还原剂
(2)室温下,某同学进行CO2与Na2O2反应的探究实验。
I.首先按照右图装置制备纯净的CO2气体。
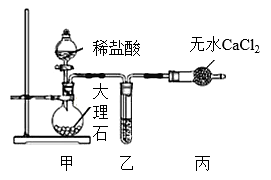
①装置甲中反应的离子方程式为:___________________ 。
②装置乙中加入的是饱和NaHCO3溶液,目的是:___________________ 。
Ⅱ.按照下面的装置图进行实验(夹持装置略)
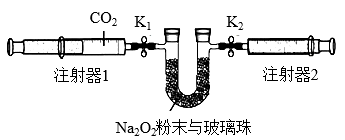
①先组装仪器,___________________ 。然后再用注射器1抽取100 mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠(玻璃珠不参与反应)
②打开止水夹K1、K2,向右缓缓推动注射器1的活塞,可观察到的现象是:___________________ 。
③实验过程中,U形管中反应的化学方程式为:___________________ 。
(3)将一定量的Na2O2固体投入到含有下列离子的溶液中: 、
、 、
、 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有________ (不考虑溶液体积的变化)(填离子符号)。
(1)Na2O2具有氧化性,可以将SO2氧化为硫酸钠,写出该反应的化学方程式:
a.还原剂 b.氧化剂 c.既是氧化剂又是还原剂
(2)室温下,某同学进行CO2与Na2O2反应的探究实验。
I.首先按照右图装置制备纯净的CO2气体。

①装置甲中反应的离子方程式为:
②装置乙中加入的是饱和NaHCO3溶液,目的是:
Ⅱ.按照下面的装置图进行实验(夹持装置略)

①先组装仪器,
②打开止水夹K1、K2,向右缓缓推动注射器1的活塞,可观察到的现象是:
③实验过程中,U形管中反应的化学方程式为:
(3)将一定量的Na2O2固体投入到含有下列离子的溶液中:
 、
、 、
、 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验小组研究SO2与Na2O2的反应。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有_______ 性,SO2与Na2O2反应生成Na2SO4。
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是_______ 。
②B中的试剂为_______ ,其主要作用是_______ 。
③实验证明假设_______ 正确。
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?_______ (填“合理”或“不合理”)。请简要说明理由:_______ 。
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的_______ (只写一条)有关。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是
②B中的试剂为
③实验证明假设
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的
您最近一年使用:0次



