在恒温恒容容器中.可逆反应2NO(g)+O2(g) 2NO2(g)△H<0,不能说明已达到平衡状态的是
2NO2(g)△H<0,不能说明已达到平衡状态的是
 2NO2(g)△H<0,不能说明已达到平衡状态的是
2NO2(g)△H<0,不能说明已达到平衡状态的是| A.O2的消耗速率和NO2的生成速率之比为l:2 |
| B.反应容器中压强不随时间变化而变化 |
| C.混合气体颜色深浅保持不变 |
| D.混合气体平均分子量保持不变 |
更新时间:2017-05-10 16:26:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以下情况中,可以证明可逆反应达到平衡状态的有个
Ⅰ.
①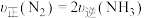
②1个N≡N键断裂的同时,有6个N—H键断裂
Ⅱ.
③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.
⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.
⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时,CO2的体积分数不再改变
Ⅴ.
⑨
⑩恒容绝热时,压强不再改变
⑪恒容绝热时,温度不再改变
Ⅰ.

①
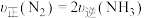
②1个N≡N键断裂的同时,有6个N—H键断裂
Ⅱ.

③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.

⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.

⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时,CO2的体积分数不再改变
Ⅴ.

⑨

⑩恒容绝热时,压强不再改变
⑪恒容绝热时,温度不再改变
| A.6 | B.7 | C.8 | D.9 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,2mol NO和1mol O2混合得到的气体中含有的分子数小于2NA |
B.1L 0.5mol·L-1 NH4Al(SO4)2溶液中所含 和Al3+的数目之和为NA 和Al3+的数目之和为NA |
| C.反应KIO3+6HI=3I2+KI+3H2O中,1mol KIO3完全反应时,转移的电子数为6NA |
| D.在氢氧碱性燃料电池中,当正极上有1mol气体参与反应时,转移的电子数为2NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s) △H>0,下列叙述正确的是( )
Z(g)+W(s) △H>0,下列叙述正确的是( )
 Z(g)+W(s) △H>0,下列叙述正确的是( )
Z(g)+W(s) △H>0,下列叙述正确的是( )A.该反应平衡常数的表达式为K= |
| B.平衡后加入X,上述反应的△H增大 |
| C.升高温度,平衡逆向移动 |
| D.当容器中气体压强不变时,反应达到平衡 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向2L真空密闭容器中加入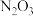 固体,发生反应
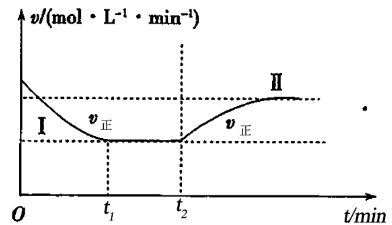
固体,发生反应 ,反应过程如图,下列说法正确的是
,反应过程如图,下列说法正确的是
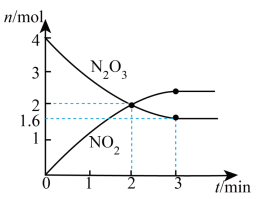
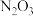 固体,发生反应
固体,发生反应 ,反应过程如图,下列说法正确的是
,反应过程如图,下列说法正确的是
A.0~2min用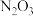 表示的平均反应速率为1mol/min 表示的平均反应速率为1mol/min |
| B.NO的体积分数不再变化,说明反应达到平衡状态 |
C.第3min时反应达到平衡状态,往体系中添加一定量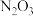 ,平衡正向移动 ,平衡正向移动 |
D.第4min时,保持温度和容积不变,向容器中充入 ,混合气体颜色不变 ,混合气体颜色不变 |
您最近半年使用:0次

 CO2(g)+H2(g)能说明该反应达到平衡状态的是
CO2(g)+H2(g)能说明该反应达到平衡状态的是

