向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得 到深蓝色透明溶液。下列对此现象说法正确的是
| A.反应前后c(Cu2+)不变 |
| B.[Cu (NH3)4]SO4是离子化合物,易溶于水和乙醇 |
| C.[Cu(NH3)4]2+中Cu2+提供空轨道 |
| D.用硝酸铜代替硫酸铜实验,不能观察到同样的现象 |
更新时间:2017-05-17 08:30:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】向硫酸铜溶液中依次加入氨水和乙醇,关于此实验下列现象预测和分析错误的是
| 选项 | 现象预测 | 分析 |
| A | CuSO4溶液呈天蓝色 | 溶液中含有[Cu(H2O)]2+ |
| B | 加入少量氨水时产生白色沉淀 | 氨水呈碱性,可与Cu2+形成难溶的Cu(OH)2 |
| C | 继续加入过量氨水,沉淀溶解,得到深蓝色透明溶液 | NH3中N配位能力较强,与Cu2+形成[Cu(NH3)4]2+,促进Cu(OH)2溶解,平衡向溶解方向移动 |
| D | 继续加入乙醇并用玻璃棒摩擦试管壁,析出深蓝色晶体 | 乙醇极性较小,析出的深蓝色晶体是[Cu(NH3)4]SO4•H2O |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
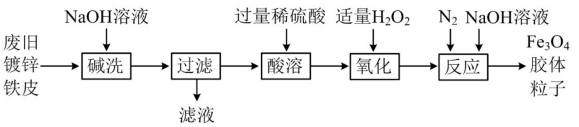
【推荐2】钢铁工业是我国国民经济的基础产业,研究钢铁的防腐有着重要的意义。某课题组进行如下实验:
下列说法正确的是
| 实验 | 装置 | 5min时现象 | 25min时现象 |
| Ⅰ |  | 铁钉表面及周边未见明显变化 | 铁钉周边出现少量红色和蓝色区域,有少量红棕色铁锈生成 |
| Ⅱ | 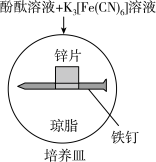 | 铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化 | 铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化 |
A.实验Ⅱ中正极的电极反应式为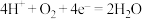 |
| B.实验Ⅱ中5min时出现红色区域,说明铁钉腐蚀速率比Ⅰ快 |
C.由 的阴离子配位数可推出其空间构型为正六边形 的阴离子配位数可推出其空间构型为正六边形 |
| D.若将Ⅱ中Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】类石墨相氮化碳(g—C3N4)作为一种新型光催化材料,在光解水产氢等领域具有广阔的应用前景,研究表明,非金属掺杂(O、S等)能提高其光催化活性。g—C3N4,具有和石墨相似的层状结构,其中一种二维平面结构如图所示。下列关于g—C3N4,的说法错误的是
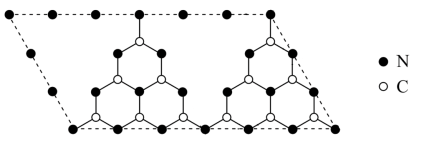

| A.基态C原子的成对电子数与未成对电子数之比为2:1 |
| B.N、O、S的第一电离能(I1)大小为I1(N)>I1(O)>I1(S) |
| C.g—C3N4晶体中存在的微粒间作用力有非极性键、π键和范德华力 |
| D.g—C3N4中,C原子的杂化轨道类型为sp2杂化,N原子的配位数为2和3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
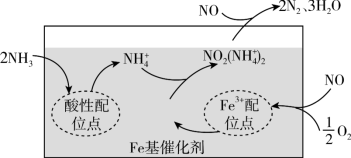
【推荐2】有氧条件下,在 基催化剂表面,
基催化剂表面, 还原
还原 的反应机理如图所示。该反应能够有效脱除烟气中的
的反应机理如图所示。该反应能够有效脱除烟气中的 ,保护环境。下列说法不正确的是
,保护环境。下列说法不正确的是
 基催化剂表面,
基催化剂表面, 还原
还原 的反应机理如图所示。该反应能够有效脱除烟气中的
的反应机理如图所示。该反应能够有效脱除烟气中的 ,保护环境。下列说法不正确的是
,保护环境。下列说法不正确的是
A.在酸性配位点上, 与 与 通过配位键形成 通过配位键形成 |
B.增大压强有利于 与 与 吸附在 吸附在 配位点上形成 配位点上形成 |
C.在反应过程中, 基催化剂不能提高 基催化剂不能提高 的平衡转化率 的平衡转化率 |
D.该反应的总方程式为 |
您最近半年使用:0次


 和
和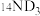 的混合物中含有的电子数为NA
的混合物中含有的电子数为NA 中为
中为 杂化的原子数为NA
杂化的原子数为NA 中σ键的数目为16NA
中σ键的数目为16NA

