下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)⑤、⑥、⑦的原子半径由大到小的顺序为_________________ (填元素符号)。它们的最高价氧化物对应水化物的碱性从强到弱的顺序为______________ (填最高价氧化物对应水化物的化学式)。
(2)②、⑧、⑨的最高价含氧酸的酸性由强到弱的顺序是__________________ (填最高价含氧酸的化学式)。
(3)①、④、⑤三种元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:__________________ 。
(4)由表中①、④两种元素的原子可按1∶1组成的一种常见液态化合物。此液态化合物的电子式为:__________________ 。请写出此液态化合物在MnO2催化作用下分解的化学方程式____________
(5)⑧是极好的半导体材料,而且能与③在高温的条件下生成一种优良的新型陶瓷材料,请写出这个反应的化学方程式:__________________ 。
| 周期\族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)⑤、⑥、⑦的原子半径由大到小的顺序为
(2)②、⑧、⑨的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤三种元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中①、④两种元素的原子可按1∶1组成的一种常见液态化合物。此液态化合物的电子式为:
(5)⑧是极好的半导体材料,而且能与③在高温的条件下生成一种优良的新型陶瓷材料,请写出这个反应的化学方程式:
更新时间:2017-05-20 07:03:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:

(1)请写出上述元素c原子基态核外电子排布式_______________ ; d+基态核外电子排布式_______________________________ 。
(2)请写出一个能比较f、h非金属性强弱的反应的化学方程式___________________ 。
(3)请比较f、h、i 三种元素的第一电离能由大到小的顺序________ (写元素符号);b、e、j三种元素的电负性由大到小的顺序________ (写元素符号)。i2-与b+两种微粒半径大小: i2-___ b+ (填>、=或<)。
(4)请写出e 元素最高价氧化物对应的水化物与a、b、i三种元素形成的化合物反应 的离子方程式___________________________________________ 。

(1)请写出上述元素c原子基态核外电子排布式
(2)请写出一个能比较f、h非金属性强弱的反应的化学方程式
(3)请比较f、h、i 三种元素的第一电离能由大到小的顺序
(4)请写出e 元素最高价氧化物对应的水化物与a、b、i三种元素形成的化合物反应 的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Na2S 常用作皮革脱毛剂,工业上用反应 Na2SO4 +2C Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。
完成下列填空:
(1)硫元素在周期表中的位置为______________ 。上述反应中涉及的各元素中原子半径最小的是
__________ (填元素符号)。写出硫化钠的电子式:___________ 。
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。_____________
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。________________________________
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为______________ mol/(L·h) 。
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。______________________________
 Na2S+2CO2↑ 进行制取。
Na2S+2CO2↑ 进行制取。完成下列填空:
(1)硫元素在周期表中的位置为
(2)用上述反应中涉及的元素,写出一个含有非极性键的化合物的化学式。
(3)写出一个能比较 S 和 O 非金属性强弱的化学事实。
(4)在 2L 的容器内发生上述反应,2 小时内共生成 78 g 硫化钠,则这段时间内用二氧化碳表示的平均反应速率为
(5)将硫化钠溶液滴入氯化铝溶液中,产生白色沉淀,同时有臭鸡蛋气味的气体生成,用平衡移动原理解
释上述现象。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题。
(1)在第三周期元素中,化学性质最不活泼的是_______ ,可用于制半导体材料的元素是_______ ,最高价氧化物的水化物碱性最强的是_______ ,酸性最强的是_______ ,具有两性的是_______ (以上均用化学式填空)。
(2)在C、N、O、F中,原子半径最大的是_______ 。
(3)第32号元素在元素周期表中的位置为_______ 。
(4)由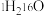 与
与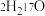 所代表的物质中,共有
所代表的物质中,共有_______ 种元素,_______ 种原子, 、
、 的关系是
的关系是_______ 。
(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:_______ 。
(1)在第三周期元素中,化学性质最不活泼的是
(2)在C、N、O、F中,原子半径最大的是
(3)第32号元素在元素周期表中的位置为
(4)由
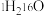 与
与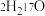 所代表的物质中,共有
所代表的物质中,共有 、
、 的关系是
的关系是(5)写出钠、铝最高价氧化物的水化物之间反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在1~18号元素中,稀有气体元素除外(请用元素符号或化学式表示):
(1)原子半径最大的元素是________ ;
(2)单质氧化性性最强的元素是_________ ;
(3)最高价氧化物对应的水化物酸性最强的是___ ;
(4)最高正价与负价的绝对值之差为6的元素是__________ ;
(5)常温下既能溶于强酸,又能溶于强碱的氧化物是__________ ;
(6)最外层电子数是内层电子数的一半的元素________ 、___________ 。
(1)原子半径最大的元素是
(2)单质氧化性性最强的元素是
(3)最高价氧化物对应的水化物酸性最强的是
(4)最高正价与负价的绝对值之差为6的元素是
(5)常温下既能溶于强酸,又能溶于强碱的氧化物是
(6)最外层电子数是内层电子数的一半的元素
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据相关知识,回答下列问题。
(1)NaOH被大量用于制皂、造纸和纺织品生产。
①Na元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
②NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
③Na的最高价氧化物的化学式为_______ 。
(2)我国科学家成功合成了含 的五氮阴离子盐,这是全氮含能材料科研领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料科研领域中里程碑式的突破。
①N在元素周期表中的位置是_______ 。
② 中,N原子之间的相互作用是
中,N原子之间的相互作用是_______ (填“离子键”或“共价键”)。
③非金属性O强于N,用原子结构解释原因:_______ ,得电子能O大于N。
④砷(As)与氮位于同一主族,下列推断正确的是_______ (填序号)。
a.砷元素的最低负化合价作为-3价
b.热稳定性:
c.砷的最高价氧化物对应的水化物属于酸
(1)NaOH被大量用于制皂、造纸和纺织品生产。
①Na元素位于第IA族H元素下方,Na的原子半径比H的
②NaOH所含的两种非金属元素中,非金属性较强的是
③Na的最高价氧化物的化学式为
(2)我国科学家成功合成了含
 的五氮阴离子盐,这是全氮含能材料科研领域中里程碑式的突破。
的五氮阴离子盐,这是全氮含能材料科研领域中里程碑式的突破。①N在元素周期表中的位置是
②
 中,N原子之间的相互作用是
中,N原子之间的相互作用是③非金属性O强于N,用原子结构解释原因:
④砷(As)与氮位于同一主族,下列推断正确的是
a.砷元素的最低负化合价作为-3价
b.热稳定性:

c.砷的最高价氧化物对应的水化物属于酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】制冷剂是一种易被压缩、液化的气体,液化后在管内循环,蒸发时吸收大量的热量,使环境温度骤然降低,达到制冷的目的。人们曾采用乙醚、NH3、CH3Cl等作制冷制,但它们不是有毒就是易燃,于是科学家根据元素性质的递变规律来研究、开发新的制冷剂。请你根据已有知识,判断某些元素化合物的易燃性、毒性的变化趋势并回答有关问题:
(1)氢化物的易燃性:SiH4>PH3>H2S>HCl,则__________ >H2O>HF(填物质的化学式)。
(2)化合物的毒性:PH3>NH3,CCl4>CF4,则H2S_____ H2O,CS2_____ CO2(选填“>”、“=”或“<”)。
根据上述规律,科学家们开始把注意力集中在含F、Cl的化合物上:
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点为-128 ℃,新的制冷剂的沸点范围应介于二者之间,经过较长时间的反复实验,发现了制冷剂CF2Cl2(氟利昂),其他类似的制冷剂可以是_____________ 或______________ 。
(4)由(3)选择的制冷剂造成的当今某一环境问题是________________________ 。但是求助于周期表中元素及其化合物的_________ (填写下列选项的编号)变化趋势开发制冷剂的科学思维方法是值得借鉴的。
①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色
A.①②③ B.②④⑤ C.②③④ D.①②④⑤
(1)氢化物的易燃性:SiH4>PH3>H2S>HCl,则
(2)化合物的毒性:PH3>NH3,CCl4>CF4,则H2S
根据上述规律,科学家们开始把注意力集中在含F、Cl的化合物上:
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点为-128 ℃,新的制冷剂的沸点范围应介于二者之间,经过较长时间的反复实验,发现了制冷剂CF2Cl2(氟利昂),其他类似的制冷剂可以是
(4)由(3)选择的制冷剂造成的当今某一环境问题是
①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色
A.①②③ B.②④⑤ C.②③④ D.①②④⑤
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为纪念 Dmitri Mendeleev(德米特里·门德列夫)发明的元素周期表诞生150周年。联合国大会室布2019年是“国际化学元素周期表年。以下是元素周期表的一部分
回答下列问题:
(1)在上表中用实线画出元素周期表的上边界_______ 。
(2)元素X原子核外有_______ 种能量不同的电子,元素Y原子最外层电子的轨道表示式为_______ ;26号元素Z的最外层有2个电子,其原结构示意可以表示为_______ 。
(3)比较元素的金属性:X_______ Y(填“>”或“<),从原子结构的角度说明理由:_______ 。
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是_______ 。
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是_______ 。
(5)氮(N)元素的气态氢化物的电子式为_______ ,假设NH 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第_______ 族,其“单质”在常温常压下_______ (填“能”或“不能”)导电。
| X | Y | ||||||||||||||||
| Z | |||||||||||||||||
(1)在上表中用实线画出元素周期表的上边界
(2)元素X原子核外有
(3)比较元素的金属性:X
(4)下列曲线分别表示元素的某种性质(y)与核电荷数(Z)的关系:

①若“y表示元素周期表中第一列元素单质熔点,则对应曲线的编号是
②若“y”表示同一短周期元素的原子半径,则对应曲线的编号是
(5)氮(N)元素的气态氢化物的电子式为
 是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
是主族“元素”NH4的阳离子,则主族“元素”NH4在元素周期表中应处于第
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】焦亚硫酸钠(Na2S2O5)是常用的脱氧剂,其制备方法是向Na2CO3溶液中通入SO2,生成NaHSO3和CO2,一定条件下NaHSO3转化为Na2S2O5。
完成下列填空:
(1)碳原子的原子结构示意图是____________ 。氧原子核外能量不同的电子有_____ 种。CO2的电子式是_________________ 。
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。______________________
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为_______________ 。
证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________ 。
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是_____ ;若反应中转移了0.04 mol的电子,有____ g Na2S2O5参加反应。
完成下列填空:
(1)碳原子的原子结构示意图是
(2)从原子结构的角度,解释氧元素的非金属性比硫元素强的原因。
(3)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其化学方程式为
证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是
(4)Na2S2O5作脱氧剂时的反应原理为Na2S2O5+O2+H2O→Na2SO4+H2SO4,该反应中,氧化产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】卤素单质及其化合物是重要的化工原料,用途广泛。
(1)下列关于卤素及其相关物质的说法不正确的是___________。
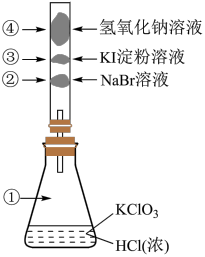
(2)已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是___________ 。
(3)下列关于含卤素物质的实验,说法正确的是___________。
(4)取等浓度的NaBr、NaI的混合溶液,加入一定量氯水后溶液中溶质的情况可能是___________。
(5)将22g NaCl和NaBr的混合粉末溶于水,配成100mL溶液,向溶液中通入足量的Cl2后,将溶液蒸干,得到干燥固体的质量为17.55g,求:
①参加反应中的Cl2在标准状况下的体积为___________ 。
②原混合物中NaCl的物质的量的百分含量为___________ 。(用小数表示,精确到0.01)
(1)下列关于卤素及其相关物质的说法不正确的是___________。
| A.卤素就是氯、溴、碘 | B.氯、溴、碘单质颜色逐渐加深 |
| C.HCl、HBr、HI还原性逐渐增强 | D.卤化银都易见光分解 |
(2)已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是

| ① | ② | ③ | ④ | |
| A | 黄绿色 | 橙色 | 蓝色 | 白色 |
| B | 无色 | 橙色 | 紫色 | 白色 |
| C | 黄绿色 | 橙色 | 蓝色 | 无色 |
| D | 黄绿色 | 无色 | 紫色 | 白色 |
(3)下列关于含卤素物质的实验,说法正确的是___________。
| A.氢气在氯气中燃烧,有苍白色烟雾生成 |
| B.溴水中加入苯振荡,静置后液体分两层,下层为红棕色 |
| C.碘化钾中加入溴水,溶液变黄,说明碘被置换出来 |
| D.卤水都有颜色,都呈酸性 |
(4)取等浓度的NaBr、NaI的混合溶液,加入一定量氯水后溶液中溶质的情况可能是___________。
| A.NaBr、NaI、NaCl | B.NaBr、NaI、NaCl、Br2 |
| C.NaI、NaCl、Br2 | D.NaBr、NaCl、I2 |
(5)将22g NaCl和NaBr的混合粉末溶于水,配成100mL溶液,向溶液中通入足量的Cl2后,将溶液蒸干,得到干燥固体的质量为17.55g,求:
①参加反应中的Cl2在标准状况下的体积为
②原混合物中NaCl的物质的量的百分含量为
您最近一年使用:0次



