A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C为_________ 。(填写相应的元素符号)E的电子式为 ____________ 。
(2)写出A、B的化合物与E反应的化学方程式:_____________ 。
(3)A、B两元素形成化合物属_____________ (“离子”或“共价”)化合物。
(4)写出D元素的最高价氧化物的水化物和A反应的化学方程式:______ 。
(1)C为
(2)写出A、B的化合物与E反应的化学方程式:
(3)A、B两元素形成化合物属
(4)写出D元素的最高价氧化物的水化物和A反应的化学方程式:
更新时间:2017-06-14 20:10:10
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】如图①﹣⑩分别代表有关反应中的一种物质,请填写以下空白.
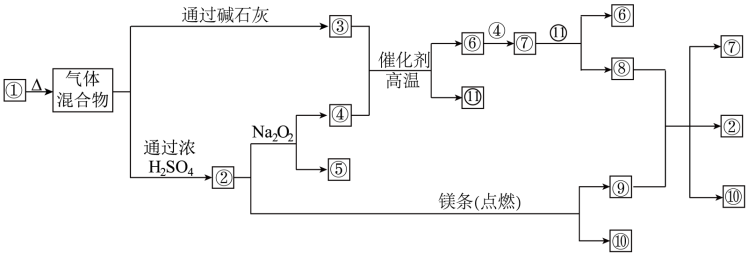
(1)已知①中阴阳离子个数比为1:1,则①的化学式是___ ,②的电子式为___ ;
(2)图中涉及的氧化还原反应共有____ 个
(3)③与④反应的化学方程式为:________ 。
(4)⑧与⑨反应的化学方程式为:_________ 。
(5)一定条件下,将2amL④和⑦的混合气体用排水法收集,得amL气体,则原混合气体中④和⑦的体积比为____ 。

(1)已知①中阴阳离子个数比为1:1,则①的化学式是
(2)图中涉及的氧化还原反应共有
(3)③与④反应的化学方程式为:
(4)⑧与⑨反应的化学方程式为:
(5)一定条件下,将2amL④和⑦的混合气体用排水法收集,得amL气体,则原混合气体中④和⑦的体积比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D为短周期元素,A的M电子层有1个电子,B的最外层电子数为内层电子数的2倍,C的最高化合价为最低化合价绝对值的3倍,C与D同周期,D的原子半径小于C。
(1)B位于元素周期表第____ 周期第____ 族。
(2)C2-离子的结构示意图为____ 。A+、C2-、D-中离子半径最小的是____ 。(用具体离子符号表示)
(3)BC2与二氧化碳的结构相似,其结构式为____ 。A2C的电子式为____ 。
(4)A、D元素最高价氧化物对应水化物相互反应的化学方程式为____ 。
(1)B位于元素周期表第
(2)C2-离子的结构示意图为
(3)BC2与二氧化碳的结构相似,其结构式为
(4)A、D元素最高价氧化物对应水化物相互反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】有关物质的转化关系如下图所示(部分条件已略去)。在通常状况下,B是黑色的金属氧化物的固体,C、D、E、F、H、I均为气体,C的水溶液显碱性,D、E、F是单质,且D、F是空气的主要成分,I为红棕色,H易与D化合生成I;G为紫红色的金属单质;反应①(反应条件为“催化剂、加热”)是工业上制备K的反应原理之一。

(1)B的化学式为________ 。
(2)F的电子式为________ 。
(3)写出反应①的化学方程式:____________________________ 。
(4)写出反应②的离子方程式:____________________________ 。

(1)B的化学式为
(2)F的电子式为
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】实验室可用浓硫酸与铜在加热条件下制备 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:
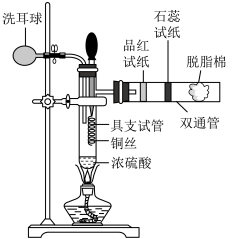
已知:①浓硫酸的沸点约为338℃。
② 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。
③ 显黄绿色。
显黄绿色。
(1)制备 的化学方程式为
的化学方程式为_______ 。
(2)脱脂棉应蘸有_______ (填化学式)溶液。
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液颜色为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为_______ ,该沉淀的生成体现了浓硫酸的_______ (填标号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了 ,设计实验证明该猜想:
,设计实验证明该猜想:_______ 。
③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:_______ 。
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:
①实验Ⅱ应加入_______ HCl溶液。
②上述实验表明, 与酸的反应受到
与酸的反应受到 浓度、
浓度、_______ 、_______ 等因素的影响。
③产生实验Ⅲ现象的原因是_______ 。
④设计实验证明铜丝表面附着的黑色物质是否含有
_______ 。
 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:
已知:①浓硫酸的沸点约为338℃。
②
 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。③
 显黄绿色。
显黄绿色。(1)制备
 的化学方程式为
的化学方程式为(2)脱脂棉应蘸有
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液颜色为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为
A.酸性 B.氧化性 C.吸水性 D.脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了
 ,设计实验证明该猜想:
,设计实验证明该猜想:③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为
 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:| 实验组别 | 实验 | 现象 |
| Ⅰ | 取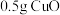 黑色粉末加入 黑色粉末加入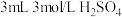 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 溶液显淡蓝色,放置1天后,蓝色变深,仍有大量黑色粉末未溶解 |
| Ⅱ | 取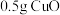 黑色粉末加入_______HCl(过量)溶液中,充分振荡 黑色粉末加入_______HCl(过量)溶液中,充分振荡 | 快速溶解,溶液显黄绿色 |
| Ⅲ | 取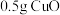 黑色粉末加入 黑色粉末加入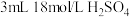 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 黑色粉末不溶解,溶液不变色 |
| Ⅳ | 将实验Ⅲ的溶液加热至沸腾 | 黑色粉末部分溶解,仍有较多黑色固体,溶液显淡蓝色 |
②上述实验表明,
 与酸的反应受到
与酸的反应受到 浓度、
浓度、③产生实验Ⅲ现象的原因是
④设计实验证明铜丝表面附着的黑色物质是否含有

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】硫酸铜可应用于电镀、颜料、医药、农药等方面。下图是探究铜与浓硫酸反应生成硫酸铜的实验装置图:

完成下列填空:
(1)写出烧瓶中发生反应的化学方程式_________ 。写出图中虚线框内装置的作用__________ 、_________ 。
(2)实验结束后,烧瓶中有白色固体生成。写出检验烧瓶中此白色固体是CuSO4的简便的方法__________ 。
(3)实验中,若反应条件控制不当,则会有少量黑色难溶物CuS、Cu2S固体生成。取此黑色固体样品ag,隔绝空气加热,发生2CuS Cu2S+S,充分反应后得到bgCu2S,则CuS的质量分数ω=
Cu2S+S,充分反应后得到bgCu2S,则CuS的质量分数ω=_________ (用含a、b的代数式表示)。加热温度过高,会有部分Cu2S分解生成Cu,则ω________ (选填“偏大”“偏小”或“不变”)。

完成下列填空:
(1)写出烧瓶中发生反应的化学方程式
(2)实验结束后,烧瓶中有白色固体生成。写出检验烧瓶中此白色固体是CuSO4的简便的方法
(3)实验中,若反应条件控制不当,则会有少量黑色难溶物CuS、Cu2S固体生成。取此黑色固体样品ag,隔绝空气加热,发生2CuS
 Cu2S+S,充分反应后得到bgCu2S,则CuS的质量分数ω=
Cu2S+S,充分反应后得到bgCu2S,则CuS的质量分数ω=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】硫脲[ ]是一种白色且具有光泽的晶体,熔点:176~178℃,温度过高时分解,易潮解,易溶于水,微溶于乙醚,常用于制造药物、染料、树脂、压塑粉等。实验室可通过硫氢化钙[
]是一种白色且具有光泽的晶体,熔点:176~178℃,温度过高时分解,易潮解,易溶于水,微溶于乙醚,常用于制造药物、染料、树脂、压塑粉等。实验室可通过硫氢化钙[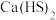 ]和氰氨化钙(
]和氰氨化钙( )制备硫脲,按要求回答问题。
)制备硫脲,按要求回答问题。
(1)制备硫氢化钙悬浊液,装置如图甲所示。
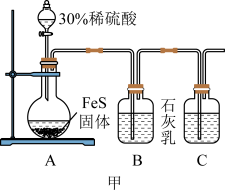
①装置A的作用为_______ 。
②为加快反应速率,可适当增加硫酸浓度,但硫酸浓度不能过大,原因是_______ 。
③装置B中发生反应的离子方程式为_______ 。
(2)备硫脲。将制得的硫氢化钙悬浊液转移到加热容器中,再加入氰氨化钙,在(80±5)℃下反应3h,制备硫脲粗品,制备装置如图乙所示。
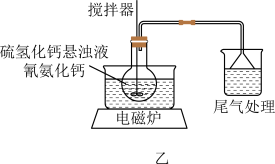
①温度控制在(80±5)℃的加热方式为_______ 。
②制备硫脲的化学方程式为_______ (只有两种生成物)。
③已知氰氨化钙遇水生成一种无色、具有强烈刺激性气味的气体,请设计简单实验证明处理的尾气的主要成分:_______ 。
(3)分离提纯硫脲。将反应所得的悬浊液减压过滤,再将滤液蒸发浓缩、趁热过滤、冷却结晶,离心脱水干燥得到硫脲晶体。
①采用离心脱水干燥而不用加热干燥的原因是_______ 。
②制备 时所用原料为13.2gFeS,最终制得硫脲1.74g,硫脲的产率为
时所用原料为13.2gFeS,最终制得硫脲1.74g,硫脲的产率为_______ (保留3位有效数字)。
 ]是一种白色且具有光泽的晶体,熔点:176~178℃,温度过高时分解,易潮解,易溶于水,微溶于乙醚,常用于制造药物、染料、树脂、压塑粉等。实验室可通过硫氢化钙[
]是一种白色且具有光泽的晶体,熔点:176~178℃,温度过高时分解,易潮解,易溶于水,微溶于乙醚,常用于制造药物、染料、树脂、压塑粉等。实验室可通过硫氢化钙[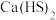 ]和氰氨化钙(
]和氰氨化钙( )制备硫脲,按要求回答问题。
)制备硫脲,按要求回答问题。(1)制备硫氢化钙悬浊液,装置如图甲所示。

①装置A的作用为
②为加快反应速率,可适当增加硫酸浓度,但硫酸浓度不能过大,原因是
③装置B中发生反应的离子方程式为
(2)备硫脲。将制得的硫氢化钙悬浊液转移到加热容器中,再加入氰氨化钙,在(80±5)℃下反应3h,制备硫脲粗品,制备装置如图乙所示。

①温度控制在(80±5)℃的加热方式为
②制备硫脲的化学方程式为
③已知氰氨化钙遇水生成一种无色、具有强烈刺激性气味的气体,请设计简单实验证明处理的尾气的主要成分:
(3)分离提纯硫脲。将反应所得的悬浊液减压过滤,再将滤液蒸发浓缩、趁热过滤、冷却结晶,离心脱水干燥得到硫脲晶体。
①采用离心脱水干燥而不用加热干燥的原因是
②制备
 时所用原料为13.2gFeS,最终制得硫脲1.74g,硫脲的产率为
时所用原料为13.2gFeS,最终制得硫脲1.74g,硫脲的产率为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、W为原子序数依次增大的前四周期元素,其中基态X原子有3个未成对电子,基态Y原子中s电子数与p电子数相等,且轨道中有未成对电子,Z与X同族,W元素位于元素周期表中第四周期12纵列,请回答下列问题:
(1)Z、W的元素符号分别为_______ 、_______ 。
(2)基态Y原子未成对电子有_______ 个。
(3)W单质具有良好的延展性,从成键理论看,原因是_______ 。
(4)X、Z分别与氢形成的最简单化合物中,沸点较高的是_______ (填化学式)。
(5)X、Y的简单氢化物分子中,键角H-Y-H小于H-X-H,原因是_______ 。
(6)WY晶体中部分Y原子被X原子替代后可以改善半导体的性能,W-X键中离子键成分的百分数小于W-Y键,原因是_______ 。
(1)Z、W的元素符号分别为
(2)基态Y原子未成对电子有
(3)W单质具有良好的延展性,从成键理论看,原因是
(4)X、Z分别与氢形成的最简单化合物中,沸点较高的是
(5)X、Y的简单氢化物分子中,键角H-Y-H小于H-X-H,原因是
(6)WY晶体中部分Y原子被X原子替代后可以改善半导体的性能,W-X键中离子键成分的百分数小于W-Y键,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】W、X、Y、Z是原子序数依次增大的四种短周期元素。W的气态氢化物能使紫色石蕊溶液变蓝,W和X两种元素的最高价氧化物的水化物均能与Y的氢氧化物发生反应,W、X、Y、Z的最外层电子数之和为16。
(1)W单质的电子式是____________ 。
(2)请用化学用语解释W的气态氢化物能使紫色石蕊溶液变蓝的原因:________________ 。
(3)已知As元素的原子序数为33,与W在同一主族,As在元素周期表中的位置是_______________ 。
(4)W的最高价氧化物的水化物与Y的氢氧化物发生反应的离子方程式是___________________ 。
(5)X与Z的单质之间发生反应的化学方程式是________________ 。
(6)已知Q与Z是位于相邻周期的同主族元素。某温度下,两种元素的气态单质与H2发生化合反应生成气态氢化物的平衡常数分别为KQ= 5.6×107,KZ = 9.7×1012。Q的元素符号是__________ ,理由是____________ 。
(1)W单质的电子式是
(2)请用化学用语解释W的气态氢化物能使紫色石蕊溶液变蓝的原因:
(3)已知As元素的原子序数为33,与W在同一主族,As在元素周期表中的位置是
(4)W的最高价氧化物的水化物与Y的氢氧化物发生反应的离子方程式是
(5)X与Z的单质之间发生反应的化学方程式是
(6)已知Q与Z是位于相邻周期的同主族元素。某温度下,两种元素的气态单质与H2发生化合反应生成气态氢化物的平衡常数分别为KQ= 5.6×107,KZ = 9.7×1012。Q的元素符号是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】已知A、B、C、D都是短周期元素,它们的原子半径大小顺序为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E是第4周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。试回答下列(1)~(4)问题(用元素符号或化学式表示)
(1)基态E2+的核外价电子排布式为___________ 。
(2)基态D原子的最高能级的轨道表示式为___________ 。
(3)M分子中B原子轨道的杂化类型为___________ 。
(4)基态C原子核外电子云有___________ 种不同的伸展方向,共有___________ 种不同能级组的电子。
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1,若该反应中形成的π键有9mol,则有___________ molN-H键断裂。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在___________ (填标号)
a.离子键b.共价键c.配位键d.范德华力
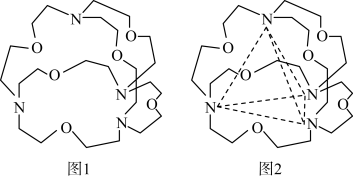
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。
a.CF4 b.CH4 c.NH d.H2O
d.H2O
(1)基态E2+的核外价电子排布式为
(2)基态D原子的最高能级的轨道表示式为
(3)M分子中B原子轨道的杂化类型为
(4)基态C原子核外电子云有
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1,若该反应中形成的π键有9mol,则有
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键b.共价键c.配位键d.范德华力
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
a.CF4 b.CH4 c.NH
 d.H2O
d.H2O
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】甲是一种含结晶水的盐,由A、B、C、D、E五种原子序数依次增大的短周期元素组成。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。B元素原子核内质子数比C的少1,C、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。
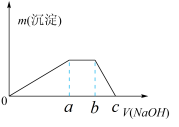
(1)D的元素符号是___________ E在周期表中的位置是___________ 。
(2)B、C、E的简单气态氢化物的沸点高低顺序为___________ (用化学式表示,下同);相同条件下,等物质的量浓度的B和E的最高价氧化物对应的水化物的水溶液,pH较小的是___________ 。
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为 ,则甲晶体的化学式为
,则甲晶体的化学式为___________ 。
(4)实验③中根据图象得V(Oa):V(ab):V(bc)=___________ 。
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式___________ 。
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。

(1)D的元素符号是
(2)B、C、E的简单气态氢化物的沸点高低顺序为
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为
 ,则甲晶体的化学式为
,则甲晶体的化学式为(4)实验③中根据图象得V(Oa):V(ab):V(bc)=
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D、E是五种短周期元素,它们的原子序数依次增大。其中A与C、B与E分别同主族。B、E两元素原子核内质子数之和是A、C之和的2倍。C、D、E 三种元素对应的最高价氧化物的水化物间两两皆能反应。
请回答:
(1)元素B的名称________ ,E在周期表中的位置为__________________ .
(2)写出B、C两元素所形成的原子个数比为1:1的化合物的电子式______ ,该化合物中存在的化学键有__________________ (选离子键、极性键或非极性键)。
(3)C、D两元素对应的最高价氧化物的水化物发生反应的离子方程式为_____________________
(4)下列选项中,可以验证B、E两元素非金属性强弱的是_______ (填序号)。
①比较两种元素常见单质的熔点
②比较两种元素的单质与氢气化合的难易程度
③比较两种元素对应氢化物的水溶液的酸性
请回答:
(1)元素B的名称
(2)写出B、C两元素所形成的原子个数比为1:1的化合物的电子式
(3)C、D两元素对应的最高价氧化物的水化物发生反应的离子方程式为
(4)下列选项中,可以验证B、E两元素非金属性强弱的是
①比较两种元素常见单质的熔点
②比较两种元素的单质与氢气化合的难易程度
③比较两种元素对应氢化物的水溶液的酸性
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】X、Y、Z、Q、M、R、T、W是原子序数依次增大的前四周期元素其中X元素的原子核外只有一个电子;X与Y原子序数之和等于Z的原子序数;Z元素的气态氢化物极易溶于水,可用作制冷剂;Q基态原子核外s能级电子总数与p能级电子总数相等;M基态原子核外有6个原子轨道排有电子,且只有1个未成对电子;R最高价氧化物的水化物是一种强酸;T为s区元素且基态原子各能层没有未成对电子;W最外层只有1个电子,其内层各能级所有轨道电子均成对。
(1)Y的基态原子最高能层符号为___________ 。
(2)Z基态原子有___________ 种不同运动状态的电子。
(3)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是___________ (用分子式表示)。
(4)Y、T能组成化合物TY2,写出其电子式___________ 。
(5)W在元素周期表中的位置为___________ ,其基态原子价层电子排布图为___________ 。
(6)下列说法不正确的是___________ 。
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
(1)Y的基态原子最高能层符号为
(2)Z基态原子有
(3)Y、Z、Q与分别X形成的10电子化合物,键角由大到小的顺序是
(4)Y、T能组成化合物TY2,写出其电子式
(5)W在元素周期表中的位置为
(6)下列说法不正确的是
A.X、Y、Z都能与Q形成原子个数之比为1:1的化合物
B.Y、Z、Q的第一电离能依次逐渐增大
C.简单离子半径大小:R>T>M
D.W的焰色试验与原子核外电子跃迁吸收能量有关
E.M同周期元素氧化物的晶体类型按离子晶体、共价晶体、分子晶体的顺序过渡
您最近一年使用:0次



