如图是实验室制备气体和验证气体性质的装置图,若利用该装置实现碳和浓硫酸的反应,并进行如下验证:

(1)实验步骤: 连接仪器、____ 、加药品后,然后滴入浓硫酸,加热。
(2)C与浓硫酸反应的化学方程式是____ 。
(3)若要证明产物中的两种气体,装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则B、D装置中品红溶液的作用分别是____ ,____ 。证明气体中有CO2的现象是____ 。
(4)若证明SO2具有氧化性,同时证明碳的非金属性比硅强,B、C、D中分别装有Na2S溶液、足量酸性KMnO4溶液、品红溶液。则:B中的现象为____ ;E中应加入____ 溶液(填化学式),现象为____ ,反应的离子方程式为____ 。

(1)实验步骤: 连接仪器、
(2)C与浓硫酸反应的化学方程式是
(3)若要证明产物中的两种气体,装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则B、D装置中品红溶液的作用分别是
(4)若证明SO2具有氧化性,同时证明碳的非金属性比硅强,B、C、D中分别装有Na2S溶液、足量酸性KMnO4溶液、品红溶液。则:B中的现象为
更新时间:2017-06-17 19:50:26
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
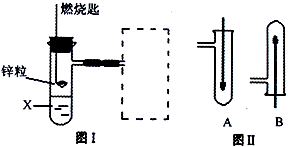
【推荐1】(1)图Ⅰ是实验室用H2还原CuO实验的简易装置,其中的铜质燃烧匙可以在试管中上下移动,虚线框中需从图Ⅱ中选取装置。图Ⅱ中的细铜丝一端被弯成螺旋状,实验时,先在酒精灯火焰上加热,变黑后再迅速伸入制得的H2中。
①在图Ⅰ中,X溶液应选用______ 。
A.稀硫酸 B.浓硫酸 C.NaCl溶液
②在图Ⅰ虚线框中,应选用图Ⅱ中的_______ (填A或B)装置。
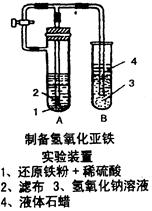
(2)某学生设计了一个制取氢氧化亚铁的实验方案,实验装置见上右图,请分析实验过程:
①在B试管中加入NaOH溶液后加热煮沸l-2分钟并立即加入2mL液体石蜡,上述操作中加热煮沸的目的是:_____________________________ 。
②在具支试管A中加入稀H2SO4溶液和略微过量的铁粉,分析为什么铁粉要过量_____________ 。
③连接好导管,同时打开活栓,当铁粉与稀硫酸反应平稳时,关闭活栓,这时看到A试管中_________ (填现象),B试管中_________ (填现象)。
④如果B中产生的氢氧化亚铁遇到空气,出现的现象是_______________ ,发生变化的化学方程式为_____________ 。
(3)现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。
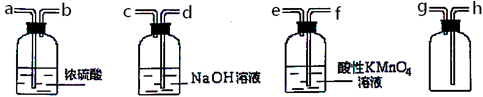
①要达到实验目的,按气流从左到右,各接口连接顺序正确的是_______ 。
A.dcabh B.feabh C.feabg
②本实验除去SO2的原理是利用SO2的________ 性质(填序号)。
A.氧化性 B.漂白性 C.还原性 D.酸性
③SO2与酸性高锰酸钾反应的离子方程式是__________________ 。
①在图Ⅰ中,X溶液应选用
A.稀硫酸 B.浓硫酸 C.NaCl溶液
②在图Ⅰ虚线框中,应选用图Ⅱ中的


(2)某学生设计了一个制取氢氧化亚铁的实验方案,实验装置见上右图,请分析实验过程:
①在B试管中加入NaOH溶液后加热煮沸l-2分钟并立即加入2mL液体石蜡,上述操作中加热煮沸的目的是:
②在具支试管A中加入稀H2SO4溶液和略微过量的铁粉,分析为什么铁粉要过量
③连接好导管,同时打开活栓,当铁粉与稀硫酸反应平稳时,关闭活栓,这时看到A试管中
④如果B中产生的氢氧化亚铁遇到空气,出现的现象是
(3)现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。

①要达到实验目的,按气流从左到右,各接口连接顺序正确的是
A.dcabh B.feabh C.feabg
②本实验除去SO2的原理是利用SO2的
A.氧化性 B.漂白性 C.还原性 D.酸性
③SO2与酸性高锰酸钾反应的离子方程式是
您最近一年使用:0次
【推荐2】将硫铁矿(主要成分为FeS2,含有少量的碳)焙烧所得尾气主要含SO2、CO2。为了检验尾气的主要成分并验证尾气的部分性质,设计了以下实验。实验用到的装置和药品如图所示:(实验装置可重复使用)

请回答下列问题:
(1)为完成实验目的,请把装置按气流方向进行连接(用小写字母填写)_________ 。
(2)装置D的作用是_________ 。
(3)酸性高锰酸钾溶液的作用有二:其一,验证SO2有还原性;其二,_________ 。
(4)装置E中被氧化的元素是_________ 。
(5)在该实验中,SO2通入FeCl3溶液中反应的离子方程式为_________ 。取反应后的该溶液于一洁净的试管中,滴加少量KSCN溶液,溶液不变红,说明溶液中_______ (填“含有”或“不含有”)Fe3+;再继续滴加少量氯水,溶液也不变红,请分析产生这种现象的原因______ 。

请回答下列问题:
(1)为完成实验目的,请把装置按气流方向进行连接(用小写字母填写)
(2)装置D的作用是
(3)酸性高锰酸钾溶液的作用有二:其一,验证SO2有还原性;其二,
(4)装置E中被氧化的元素是
(5)在该实验中,SO2通入FeCl3溶液中反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】某研究小组利用海水提取粗盐后得到的苦卤(含Mg2+、Ca2+、Br-等离子的溶液)提取Br2并制备含镁化合物。部分工艺流程设计如下:
回答下列问题:
(1)步骤I中用硫酸酸化可抑制氯气与水的反应,原因是____ (结合离子方程式回答)。
(2)工业上常用Na2CO3法或SO2法实现含Br2混合气到液溴的转化,流程如下:
Na2CO3法:
SO2法:
① Na2CO3法中步骤Ⅲ的反应有气体生成,离子方程式为______ 。步骤V中蒸馏时蒸气出口温度通常控制在65-75℃,若温度过低,溴蒸出不充分;若温度过高,则会导致液溴中混有较多的____________ 。
② SO2法对比Na2CO3法的缺点是__________ (答出一条即可)。
(3)提溴后所得含Mg2+、Ca2+的溶液可设计如下流程制备碱式碳酸镁[Mg5(OH)2(CO3)4·4H2O]和无水氯化镁:
① 步骤Ⅷ的化学方程式为_________ 。
② 若步骤X中生成的CO与CO2物质的量之比为3:1,写出反应的化学方程式__________ 。
③25℃,步骤Ⅵ生成Mg(OH)2沉淀后,若溶液中残留的Mg2+浓度为l.8×10-6mol/L 。则溶液的pH为________ ;此pH下,欲使Mg(OH)2沉淀中不含Ca(OH)2,则溶液中c(Ca2+)不能大于____ (已知:25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Ca(OH)2]=5.5×10-6)

回答下列问题:
(1)步骤I中用硫酸酸化可抑制氯气与水的反应,原因是
(2)工业上常用Na2CO3法或SO2法实现含Br2混合气到液溴的转化,流程如下:
Na2CO3法:

SO2法:
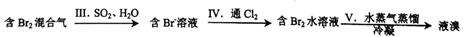
① Na2CO3法中步骤Ⅲ的反应有气体生成,离子方程式为
② SO2法对比Na2CO3法的缺点是
(3)提溴后所得含Mg2+、Ca2+的溶液可设计如下流程制备碱式碳酸镁[Mg5(OH)2(CO3)4·4H2O]和无水氯化镁:

① 步骤Ⅷ的化学方程式为
② 若步骤X中生成的CO与CO2物质的量之比为3:1,写出反应的化学方程式
③25℃,步骤Ⅵ生成Mg(OH)2沉淀后,若溶液中残留的Mg2+浓度为l.8×10-6mol/L 。则溶液的pH为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】实验题
实验室制取乙烯是用乙醇跟浓硫酸反应,常因温度过高而发生副反应生成炭黑、二氧化硫、二氧化碳和水蒸气。请用如图编号为①~⑥的实验装置,设计一个实验,以验证上述反应后的混合气体中含有二氧化硫、二氧化碳和水蒸气。

(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)(6)→( )→(3)→( )→( )→( )____
(2)装置⑤中的固体药品为____ ,用以验证的产物是____ 。
(3)装置④中的溶液是____ ,用以验证的产物是____ 。
(4)装置①中的品红溶液的作用_____ 。
(5)装置②中溴水的作用是____ 。写出②中可能发生的2个化学方程式____ 、____ 。
实验室制取乙烯是用乙醇跟浓硫酸反应,常因温度过高而发生副反应生成炭黑、二氧化硫、二氧化碳和水蒸气。请用如图编号为①~⑥的实验装置,设计一个实验,以验证上述反应后的混合气体中含有二氧化硫、二氧化碳和水蒸气。

(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)(6)→( )→(3)→( )→( )→( )
(2)装置⑤中的固体药品为
(3)装置④中的溶液是
(4)装置①中的品红溶液的作用
(5)装置②中溴水的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】实验室用浓硫酸和焦炭反应生成的产物中含有CO2、SO2、H2O。请回答下列问题:
(1)写出反应的化学方程式______________ ;
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2、SO2、H2O(g),按气流的方向,各装置的连接顺序是:______ 。(填序号)

(3)实验时若观察到:①中溶液褪色,B瓶中深水颜色逐渐变浅,C瓶中溶液不褪色, 则A 瓶的作用是______ ,B瓶的作用是______ ,C瓶的作用是_______ 。
(4)装置②中所加的试剂名称是_______ ,它可以验证的气体是_____ ,简述确定装置②在整套装置中的位置的理由是___________ 。
(5)装置③中所盛溶液的名称是______ ,它可以用来验证的气体是________ 。
(1)写出反应的化学方程式
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2、SO2、H2O(g),按气流的方向,各装置的连接顺序是:

(3)实验时若观察到:①中溶液褪色,B瓶中深水颜色逐渐变浅,C瓶中溶液不褪色, 则A 瓶的作用是
(4)装置②中所加的试剂名称是
(5)装置③中所盛溶液的名称是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为_____________________
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置中导管口的编号):
_________ 接__________ ,________ 接__________ ,___________ 接_______________ 。
(1)上述反应的化学方程式为
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
| 编号 | ① | ② | ③ | ④ |
| 装置 |  |  |  |  |
您最近一年使用:0次



