实验室里用图所示装置制取并收集纯净的氯气.回答下列问题:

①写出烧瓶中发生反应的化学方程式:_________________________________ .
②C处盛有饱和食盐水,其作用是_________________ .
③D处盛放的试剂是_________ (填名称),其作用是_____________ .
④F处盛有__________ (填名称),发生反应的离子方程式为_______________ .

①写出烧瓶中发生反应的化学方程式:
②C处盛有饱和食盐水,其作用是
③D处盛放的试剂是
④F处盛有
更新时间:2017-06-23 02:32:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
“碱浸”中NaOH的两个作用分别是_______ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式_______ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
“碱浸”中NaOH的两个作用分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国某电镀厂的电镀废水沉泥中含有大量的有价金属(Cu、Zn、Ni、Fe、Ag等)。某科研团队利用电镀废水沉泥回收七水硫酸锌(ZnSO4·7H2O)的工艺流程如下:

已知:“除铁”时若pH过高,会产生氢氧化铁胶状沉淀,其具有较强的吸附性。回答下列问题:
(1)“浸出”步骤中,适当增大H2SO4浓度的原因是___________ 。
(2)“除铁”步骤中发生反应的离子方程式为___________ 。调节pH对不同金属沉出率的影响如图所示:

沉铁时最合理的pH约为___________ (填序号)。
A.2.8 B. 3.2 C. 3.4 D.3.6
(3)根据流程图可知Zn、Cu、Ni的金属性强弱顺序为___________ 。
(4)“浸出”的浸渣中含有Ag2S,经一系列处理得Ag(NH3)2Cl,用肼(N2H4)还原Ag(NH3)2Cl得到单质银(Ag),还原过程中氧化剂与还原剂的物质的量之比为4:1,则N2H4的氧化产物为___________ 。
(5)已知肼蒸汽可以与NO2反应:2N2H4(g)+2NO2(g) 3N2(g)+4H2O(g),在温度T下,容积固定的密闭容器中充入3molN2H4和3molNO2,起始压强为Po,一段时间后,反应达到平衡,此时压强p=1.5Po,反应开始时,NO2的分压是
3N2(g)+4H2O(g),在温度T下,容积固定的密闭容器中充入3molN2H4和3molNO2,起始压强为Po,一段时间后,反应达到平衡,此时压强p=1.5Po,反应开始时,NO2的分压是___________ (用含po的代数式表示),N2H4的平衡分压是___________ (用含p的代数式表示),平衡时N2H4的转化率是___________ %。(保留一位小数)

已知:“除铁”时若pH过高,会产生氢氧化铁胶状沉淀,其具有较强的吸附性。回答下列问题:
(1)“浸出”步骤中,适当增大H2SO4浓度的原因是
(2)“除铁”步骤中发生反应的离子方程式为

沉铁时最合理的pH约为
A.2.8 B. 3.2 C. 3.4 D.3.6
(3)根据流程图可知Zn、Cu、Ni的金属性强弱顺序为
(4)“浸出”的浸渣中含有Ag2S,经一系列处理得Ag(NH3)2Cl,用肼(N2H4)还原Ag(NH3)2Cl得到单质银(Ag),还原过程中氧化剂与还原剂的物质的量之比为4:1,则N2H4的氧化产物为
(5)已知肼蒸汽可以与NO2反应:2N2H4(g)+2NO2(g)
 3N2(g)+4H2O(g),在温度T下,容积固定的密闭容器中充入3molN2H4和3molNO2,起始压强为Po,一段时间后,反应达到平衡,此时压强p=1.5Po,反应开始时,NO2的分压是
3N2(g)+4H2O(g),在温度T下,容积固定的密闭容器中充入3molN2H4和3molNO2,起始压强为Po,一段时间后,反应达到平衡,此时压强p=1.5Po,反应开始时,NO2的分压是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是“铁链状”图案,图中相连的两物质可归属于同一类别,相交部分A、B、C、D为其相应的分类依据代号。

(1)①写出相邻两种物质之间能发生反应的化学方程式______________________________
②写出除去NaCl溶液中杂质FeCl3的化学方程式__________________________ 。
(2)请简述选用图中物质制备Fe(OH)3胶体的实验操作_________________________ 。
(3)以下框图中化合物A是上述链状图中的一种物质,是生活中常见的一种调味品,如下图是该物质在化工生产中的一系列反应;其中化合物F俗称烧碱,单质C也是上述链状图中的一种物质。
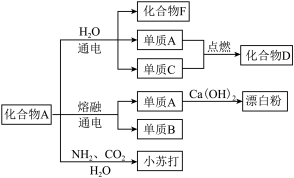
①写出单质B与H2O反应的离子方程式______________________________ 。
②单质A与Ca(OH)2反应制取漂白粉的化学方程式为________________________ 。

(1)①写出相邻两种物质之间能发生反应的化学方程式
②写出除去NaCl溶液中杂质FeCl3的化学方程式
(2)请简述选用图中物质制备Fe(OH)3胶体的实验操作
(3)以下框图中化合物A是上述链状图中的一种物质,是生活中常见的一种调味品,如下图是该物质在化工生产中的一系列反应;其中化合物F俗称烧碱,单质C也是上述链状图中的一种物质。

①写出单质B与H2O反应的离子方程式
②单质A与Ca(OH)2反应制取漂白粉的化学方程式为
您最近一年使用:0次



