以石油化工的一种产品A(乙烯)为主要原料合成一种具有果香味的物质E的生产流程如下:

(1)步骤①的化学方程式_______ ,反应类型_______ 。步骤②的化学方程式_______ ,反应类型_______ 。
(2)某同学欲用上图装置制备物质E,回答以下问题:
①试管A发生反应的化学方程式_______ 。
②试管B中的试剂是_______ ;分离出乙酸乙酯的实验操作是_______ (填操作名称),用到的主要玻璃仪器为_______ 。
③插入右边试管的导管接有一个球状物,其作用为_______ 。
(3)为了制备重要的有机原料——氯乙烷(CH3-CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备,原理是:
CH3-CH3+Cl2 CH3-CH2Cl+HCl。
CH3-CH2Cl+HCl。
乙同学:选乙烯和适量氯化氢在一定条件下制备,原理是:CH2=CH2+HCl → CH3-CH2Cl。
你认为上述两位同学的方案中,合理的是_______ ,简述你的理由:_______ 。

(1)步骤①的化学方程式
(2)某同学欲用上图装置制备物质E,回答以下问题:
①试管A发生反应的化学方程式
②试管B中的试剂是
③插入右边试管的导管接有一个球状物,其作用为
(3)为了制备重要的有机原料——氯乙烷(CH3-CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备,原理是:
CH3-CH3+Cl2
 CH3-CH2Cl+HCl。
CH3-CH2Cl+HCl。乙同学:选乙烯和适量氯化氢在一定条件下制备,原理是:CH2=CH2+HCl → CH3-CH2Cl。
你认为上述两位同学的方案中,合理的是
更新时间:2017-07-12 19:21:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】苯佐卡因(对氨基苯甲酸乙酯)常用于创面、溃疡面及痔疮的镇痛。在实验室用对氨基苯甲酸( )与乙醇反应合成苯佐卡因,已知:
)与乙醇反应合成苯佐卡因,已知:
 +CH3CH2OH
+CH3CH2OH
 +H2O
+H2O
有关数据和实验装置图如图:

产品合成:在250mL圆底烧瓶中加入8.2g对氨基苯甲酸(约0.06mol)和80mL无水乙醇(约1.4mol),振荡溶解,将烧瓶置于冰水浴并加入10mL浓硫酸,然后将反应混合物在80℃热水浴中加热回流1h,并不断振荡。
分离提纯:冷却后将反应液转移到400mL烧杯中,分批加入10%的Na2CO3溶液直至pH=9,转移至分液漏斗中,用乙醚(密度为0.714g·cm-3)分两次萃取,并向醚层加入无水硫酸镁,蒸馏,冷却结晶,最终得到产物3.3g。
①仪器A的名称为___ 。
②在合成反应进行之前圆底烧瓶中还应加入适量的__ 。
③将该烧瓶置于冰水浴中的目的是__ 。
④分液漏斗使用之前必须进行的操作是__ ,乙醚位于__ (填“上层”或“下层”);分离提纯操作加入无水硫酸镁的作用是__ 。
⑤合成反应中加入远过量的乙醇的目的是__ ;分离提纯过程中加入10%Na2CO3溶液的作用是___ 。
⑥本实验中苯佐卡因的产率为___ (保留3位有效数字)。该反应产率较低的原因是__ (填标号)。
a.浓硫酸具有强氧化性和脱水性,导致副反应多
b.催化剂加入量不足
c.产品难溶于水,易溶于乙醇、乙醚
d.酯化反应是可逆反应
 )与乙醇反应合成苯佐卡因,已知:
)与乙醇反应合成苯佐卡因,已知: +CH3CH2OH
+CH3CH2OH
 +H2O
+H2O有关数据和实验装置图如图:

| 相对分 子质量 | 密度/ (g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 | |
| 乙醇 | 46 | 0.789 | -114.3 | 78.5 | 与水以任意比互溶 |
| 对氨基苯甲酸 | 137 | 1.374 | 188 | 339.9 | 微溶于水,易溶于乙醇 |
| 对氨基苯甲酸乙酯 | 165 | 1.17 | 90 | 172 | 难溶于水,易溶于醇、醚类 |
分离提纯:冷却后将反应液转移到400mL烧杯中,分批加入10%的Na2CO3溶液直至pH=9,转移至分液漏斗中,用乙醚(密度为0.714g·cm-3)分两次萃取,并向醚层加入无水硫酸镁,蒸馏,冷却结晶,最终得到产物3.3g。
①仪器A的名称为
②在合成反应进行之前圆底烧瓶中还应加入适量的
③将该烧瓶置于冰水浴中的目的是
④分液漏斗使用之前必须进行的操作是
⑤合成反应中加入远过量的乙醇的目的是
⑥本实验中苯佐卡因的产率为
a.浓硫酸具有强氧化性和脱水性,导致副反应多
b.催化剂加入量不足
c.产品难溶于水,易溶于乙醇、乙醚
d.酯化反应是可逆反应
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某同学用如图所示的实验装置制取少量乙酸乙酯,实验结束后,试管甲中上层为透明的、不溶于水的油状液体。
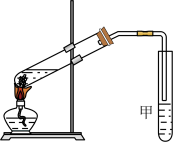
(1)实验开始时,试管甲中的导管不伸入液面下的原因是______ ;当观察到试管甲中______ 时,认为反应基本完成。
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图。
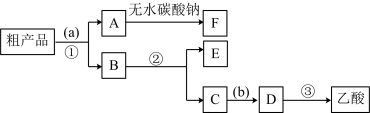
试剂b是______ ;分离方法①是______ ;分离方法③是______ 。

(1)实验开始时,试管甲中的导管不伸入液面下的原因是
(2)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图。

试剂b是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】已知如表数据:
某同学进行乙酸乙酯的制备实验。
(1)写出该反应的方程式_______ 。
(2)安装好仪器后,在大试管中配制好体积比为3:2的乙醇和乙酸,加热至沸腾,很久也没有果香味液体生成,原因是_______ 。
(3)根据表中数据分析 ,为什么乙醇需要过量些,其原因是_______ 。
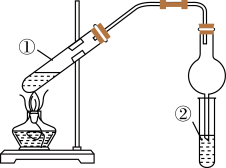
(4)该同学设计了下列实验装置。装置中的干燥管具有哪些作用?_______ 。试管②中能否用NaOH溶液来除去乙酸乙酯中的杂质_______ ?请结合相关方程式进行理由阐述_______ 。经多次实验发现,用该装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为_______ 、_______ 。
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | —— | 338 | 1.84 |
(1)写出该反应的方程式
(2)安装好仪器后,在大试管中配制好体积比为3:2的乙醇和乙酸,加热至沸腾,很久也没有果香味液体生成,原因是
(3)
(4)该同学设计了下列实验装置。装置中的干燥管具有哪些作用?

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】氨甲环酸(G),别名止血环酸,是一种已被广泛使用半个世纪的止血药,它的一种合成路线如下(部分反应条件和试剂略):
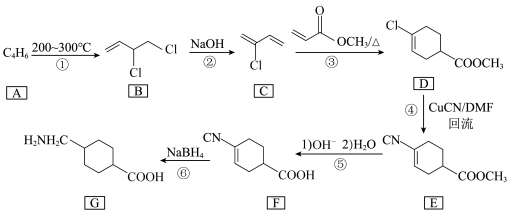
回答下列问题:
(1)A的结构简式是___________ 。
(2)C的化学名称是___________ 。
(3)②的反应类型是___________ 。
(4)E中不含N原子的官能团名称为___________ 。
(5)氨甲环酸(G)的分子式为___________ 。
(6)写出满足以下条件的所有E的同分异构体的结构简式:______________________ 。
a含苯环 b.与硝化甘油具有相同官能团 c.核磁共振氢谱有三组峰
(7)写出以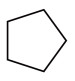 和
和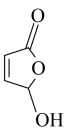 为原料,制备医药中间体
为原料,制备医药中间体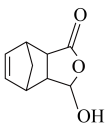 的合成路线:
的合成路线:_______________________________________________________ (无机试剂任选)。

回答下列问题:
(1)A的结构简式是
(2)C的化学名称是
(3)②的反应类型是
(4)E中不含N原子的官能团名称为
(5)氨甲环酸(G)的分子式为
(6)写出满足以下条件的所有E的同分异构体的结构简式:
a含苯环 b.与硝化甘油具有相同官能团 c.核磁共振氢谱有三组峰
(7)写出以
 和
和 为原料,制备医药中间体
为原料,制备医药中间体 的合成路线:
的合成路线:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A(C3H6)是基本有机化工原料,由A制备聚合物C和 合成路线如图所示(部分条件略去)。
合成路线如图所示(部分条件略去)。

已知: ,R-C
,R-C N
N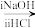 RCOOH
RCOOH
(1)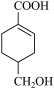 发生缩聚形成的高聚物的结构简式为
发生缩聚形成的高聚物的结构简式为____ ;D→E的反应类型为____ 。
(2)E→F的化学方程式为____ 。
(3)B的同分异构体中,与B具有相同官能团且能发生银镜反应,其中核磁共振氢谱上显示3组峰,且峰面积之比为6:1:1的是____ (写出结构简式)。
(4)等物质的量的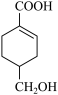 分别与足量NaOH、NaHCO3反应, 消耗NaOH、NaHCO3的物质的量之比为
分别与足量NaOH、NaHCO3反应, 消耗NaOH、NaHCO3的物质的量之比为____ ;检验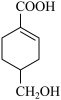 的碳碳双键的方法是
的碳碳双键的方法是____ (写出对应试剂及现象)。
 合成路线如图所示(部分条件略去)。
合成路线如图所示(部分条件略去)。
已知:
 ,R-C
,R-C N
N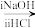 RCOOH
RCOOH(1)
 发生缩聚形成的高聚物的结构简式为
发生缩聚形成的高聚物的结构简式为(2)E→F的化学方程式为
(3)B的同分异构体中,与B具有相同官能团且能发生银镜反应,其中核磁共振氢谱上显示3组峰,且峰面积之比为6:1:1的是
(4)等物质的量的
 分别与足量NaOH、NaHCO3反应, 消耗NaOH、NaHCO3的物质的量之比为
分别与足量NaOH、NaHCO3反应, 消耗NaOH、NaHCO3的物质的量之比为 的碳碳双键的方法是
的碳碳双键的方法是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
真题
解题方法
【推荐3】常用作风信子等香精的定香剂D以及可用作安全玻璃夹层的高分子化合物PVB的合成路线如下:
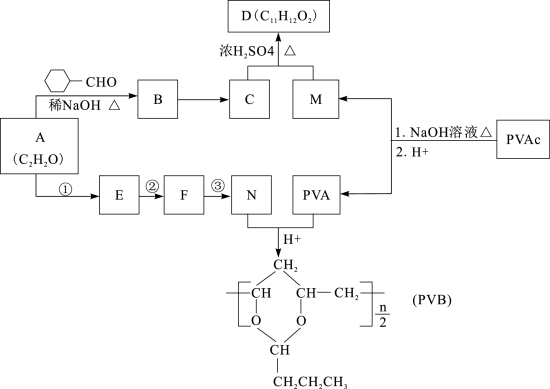
已知:

(1)A的核磁共振氢谱有两种峰,A的名称是___________
(2)A与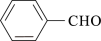 合成B的化学方程式是
合成B的化学方程式是_________
(3)C为反式结构,由B还原得到。C的结构的是__________
(4)E能使Br2的CCl4溶液褪色,N由A经反应1~3合成。
a. ①的化学试剂和条件是_______ 。
b. ②的反应类型是_______ 。
c. ③的化学方程式是_______ 。
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是_______ 。
(6)碱性条件下,PVAc完全水解的化学方程式是_______ 。

已知:

(1)A的核磁共振氢谱有两种峰,A的名称是
(2)A与
 合成B的化学方程式是
合成B的化学方程式是(3)C为反式结构,由B还原得到。C的结构的是
(4)E能使Br2的CCl4溶液褪色,N由A经反应1~3合成。
a. ①的化学试剂和条件是
b. ②的反应类型是
c. ③的化学方程式是
(5)PVAc由一种单体经加聚反应得到,该单体的结构简式是
(6)碱性条件下,PVAc完全水解的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
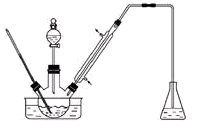

已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4•nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1) 实验装置中冷凝管的主要作用是_____ ,锥形瓶中应为_______ (填化学式)溶液。
(2) 步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)______ 。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3) 步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的______ (填化学式)。
(4) 步骤3中加入无水MgSO4固体的作用是___________________________________ 。
(5) 步骤4中采用减压蒸馏,是为了防止____________________________________ 。


已知:(1)间溴苯甲醛温度过高时易被氧化。
(2)溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点见下表:
| 物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
| 沸点/℃ | 58.8 | 179 | 83.5 | 229 |
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4•nH2O晶体。
步骤4:减压蒸馏有机层,收集相应馏分。
(1) 实验装置中冷凝管的主要作用是
(2) 步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3) 步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的
(4) 步骤3中加入无水MgSO4固体的作用是
(5) 步骤4中采用减压蒸馏,是为了防止
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知:

(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是_______ 。②试管C置于冰水浴中的目的是_______ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_______ 层(填上或下),分液后用_______ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图装置蒸馏,收集产品时,控制的温度应在83℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是_______ 。

a.蒸馏时从70℃开始收集产品
b.制备粗品时环己醇随产品一起蒸出
c.环己醇实际用量多了
(3)以下区分环己烯精品和粗品的方法,合理的是_______ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
已知:


| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图装置蒸馏,收集产品时,控制的温度应在83℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是

a.蒸馏时从70℃开始收集产品
b.制备粗品时环己醇随产品一起蒸出
c.环己醇实际用量多了
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
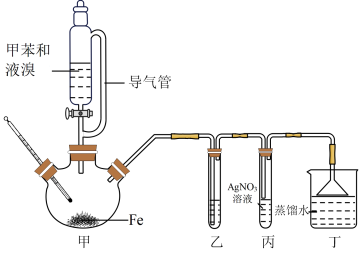
【推荐3】对溴甲苯(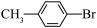 )是一种有机合成原料,广泛应用于医药合成。实验室中为了制得对溴甲苯并证明甲苯和溴反应的反应类型,装置如图所示。
)是一种有机合成原料,广泛应用于医药合成。实验室中为了制得对溴甲苯并证明甲苯和溴反应的反应类型,装置如图所示。
已知:
回答下列问题:
(1)仪器甲的名称是___________ 。
(2)装置乙中需盛放的试剂名称为___________ ,目的是___________ 。
(3)生成对溴甲苯的化学方程式为___________ 。
(4)甲苯和溴在光照下发生反应的化学方程式为___________ 。
(5)取装置甲中反应后的混合物,经过下列操作可获得纯净的对溴甲苯。
步骤1:水洗,分液;
步骤2:用NaOH稀溶液洗涤,除去___________ (填化学式),分液;
步骤3:水洗,分液;
步骤4:加入无水CaCl2粉末干燥,过滤;
步骤5:通过___________ (填操作名称),分离对溴甲苯和甲苯。
(6)关于该实验,下列说法正确的是___________ (填字母)。
a.可以用溴水代替液溴
b.装置丙中的导管可以插入溶液中
c.装置丙中有淡黄色沉淀生成时,说明该反应为取代反应
 )是一种有机合成原料,广泛应用于医药合成。实验室中为了制得对溴甲苯并证明甲苯和溴反应的反应类型,装置如图所示。
)是一种有机合成原料,广泛应用于医药合成。实验室中为了制得对溴甲苯并证明甲苯和溴反应的反应类型,装置如图所示。
已知:
| 甲苯 | 溴 | 对溴甲苯 | |
| 沸点/℃ | 110 | 59 | 184 |
| 水溶性 | 难溶 | 微溶 | 难溶 |
(1)仪器甲的名称是
(2)装置乙中需盛放的试剂名称为
(3)生成对溴甲苯的化学方程式为
(4)甲苯和溴在光照下发生反应的化学方程式为
(5)取装置甲中反应后的混合物,经过下列操作可获得纯净的对溴甲苯。
步骤1:水洗,分液;
步骤2:用NaOH稀溶液洗涤,除去
步骤3:水洗,分液;
步骤4:加入无水CaCl2粉末干燥,过滤;
步骤5:通过
(6)关于该实验,下列说法正确的是
a.可以用溴水代替液溴
b.装置丙中的导管可以插入溶液中
c.装置丙中有淡黄色沉淀生成时,说明该反应为取代反应
您最近一年使用:0次



