如图表示常见元素单质及化合物相应转化关系,部分反应的产物没有全部列出。
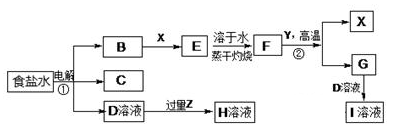
已知:B是黄绿色气体、有毒性,C是所有气体中密度最小的一种,D是一种强碱;X、Y是日常生活中应用最为广泛的两种金属材料,F是一种红棕色的固体氧化物,常可以用作制备红色油漆和涂料;Z为气态氧化物。
请回答下列问题:
(1)气体B和X反应的化学方程式___________ ;
(2)反应②属于四种基本反应类型中的_______ 反应。
(3)有学生认为B与X反应的产物E不一定是纯净物。他认为产物中可能还有______ (填化学式),为验证其猜想该同学设计了相关实验,你认为他需要选择的试剂为____ 。
A.酸性高锰酸钾溶液 B.NaOH溶液 C.KSCN溶液 D.稀硫酸
(4)若Z能导致温室效应,则反应③的离子反应方程式为_______________ 。
(5)若Z是酸雨形成的罪魁祸首,目前应用最广泛的工业处理含Z废气的方法是在一定条件下与生石灰作用而使其固定,产物可作建筑材料,反应的化学方程式为______________ 。

已知:B是黄绿色气体、有毒性,C是所有气体中密度最小的一种,D是一种强碱;X、Y是日常生活中应用最为广泛的两种金属材料,F是一种红棕色的固体氧化物,常可以用作制备红色油漆和涂料;Z为气态氧化物。
请回答下列问题:
(1)气体B和X反应的化学方程式
(2)反应②属于四种基本反应类型中的
(3)有学生认为B与X反应的产物E不一定是纯净物。他认为产物中可能还有
A.酸性高锰酸钾溶液 B.NaOH溶液 C.KSCN溶液 D.稀硫酸
(4)若Z能导致温室效应,则反应③的离子反应方程式为
(5)若Z是酸雨形成的罪魁祸首,目前应用最广泛的工业处理含Z废气的方法是在一定条件下与生石灰作用而使其固定,产物可作建筑材料,反应的化学方程式为
更新时间:2017-08-18 10:46:26
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】合理利用废旧铅蓄电池可缓解铅资源短缺,同时减少污染。
I.一种从废旧铅蓄电池的铅膏中回收铅的流程如图(部分产物已略去)。

已知:①溶度积(25℃):Ksp(PbSO4)=2.25×10-8,Ksp(PbCO3)=7.2×10-14;
②PbSiF6和H2SiF6均为能溶于水的强电解质。
请回答下列问题:
(1)过程i中,物质a表现______ (填“氧化”或“还原”)性。
(2)过程ii需要加入(NH4)2CO3溶液,从化学平衡的角度解释其作用原理______ ;饱和PbSO4溶液中c(Pb2+)=______ mol/L。
(3)过程iii发生反应的离子方程式为______ 。
II.工业上用PbSiF6和H2SiF6混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、Fe、Zn)的提纯,装置示意图如图。
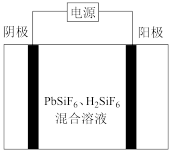
(4)①阴极材料为______ (填“粗铅”或“纯铅”)。
②电解时产生的阳极泥的主要成分为______ (用元素符号表示)。
(5)为了保证析出铅的光滑度和致密性,电解工作一段时间后需要补充Pb2+以保持溶液中Pb2+浓度的稳定,同时需要调控好溶液中H2SiF6的浓度。
①电解工作一段时间后电解液中会混入______ (用离子符号表示)而影响Pb2+的浓度。
②H2SiF6的浓度过高时也会造成铅产率减小,原因可能是______ (用电极反应式表示)。
I.一种从废旧铅蓄电池的铅膏中回收铅的流程如图(部分产物已略去)。

已知:①溶度积(25℃):Ksp(PbSO4)=2.25×10-8,Ksp(PbCO3)=7.2×10-14;
②PbSiF6和H2SiF6均为能溶于水的强电解质。
请回答下列问题:
(1)过程i中,物质a表现
(2)过程ii需要加入(NH4)2CO3溶液,从化学平衡的角度解释其作用原理
(3)过程iii发生反应的离子方程式为
II.工业上用PbSiF6和H2SiF6混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、Fe、Zn)的提纯,装置示意图如图。

(4)①阴极材料为
②电解时产生的阳极泥的主要成分为
(5)为了保证析出铅的光滑度和致密性,电解工作一段时间后需要补充Pb2+以保持溶液中Pb2+浓度的稳定,同时需要调控好溶液中H2SiF6的浓度。
①电解工作一段时间后电解液中会混入
②H2SiF6的浓度过高时也会造成铅产率减小,原因可能是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液无色、澄清,对该溶液初步分析后发现其中可能含有SO 、Na+、CO
、Na+、CO 、OH-、K+、Cl-中的若干种,然后又做了如下实验:
、OH-、K+、Cl-中的若干种,然后又做了如下实验:
①用紫色石蕊溶液测定溶液的酸碱性,结果紫色石蕊溶液显蓝色;
②取2mL溶液,加入BaCl2溶液和稀盐酸,生成了白色沉淀,没有产生气泡;
③将②中所得的混合物充分静置后,取上层澄清的液体,加入AgNO3溶液和稀硫酸,生成了白色沉淀。
(1)由上述实验可知:溶液中一定存在的离子是_____ (填离子符号,下同);一定不存在的离子是_____ ,原因是_____ (用离子方程式表示)。
(2)在上述实验操作中,有错误的步骤是_____ (填序号),原因是_____ 。
(3)改正实验操作后,仍生成白色沉淀,则接下来可以用_____ (用本章学过的方法)方法验证溶液中剩余未检验的离子。
 、Na+、CO
、Na+、CO 、OH-、K+、Cl-中的若干种,然后又做了如下实验:
、OH-、K+、Cl-中的若干种,然后又做了如下实验:①用紫色石蕊溶液测定溶液的酸碱性,结果紫色石蕊溶液显蓝色;
②取2mL溶液,加入BaCl2溶液和稀盐酸,生成了白色沉淀,没有产生气泡;
③将②中所得的混合物充分静置后,取上层澄清的液体,加入AgNO3溶液和稀硫酸,生成了白色沉淀。
(1)由上述实验可知:溶液中一定存在的离子是
(2)在上述实验操作中,有错误的步骤是
(3)改正实验操作后,仍生成白色沉淀,则接下来可以用
您最近一年使用:0次
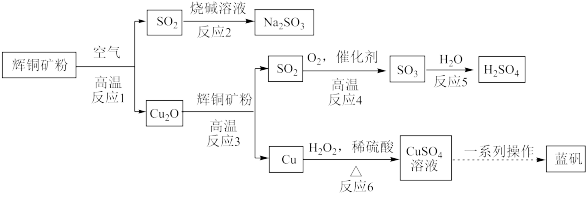
【推荐3】胆矾(或蓝矾)在日常生活中有广泛应用,如配制农药波尔多液、作游泳池的消毒剂。某小组以辉铜矿粉(主要成分是Cu2S)为原料制备胆矾及副产品的简易流程如下:
请回答下列问题:
(1)胆矾的化学式为_______ 。
(2)反应1中被氧化的元素有_______ (填元素符号);80 gSO3与足量水反应生成_______ mol H2SO4。
(3)反应3的化学方程式为_______ 。
(4)反应6的离子方程式为_______ 。
(5)Na2SO3在空气中易变质生成_______ (填化学式)。
(6)已知蓝矾的溶解度随温度变化如图所示。

从CuSO4溶液中提取蓝矾,采用“一系列操作”包括蒸发浓缩、_______ 、过滤、洗涤、低温干燥。

请回答下列问题:
(1)胆矾的化学式为
(2)反应1中被氧化的元素有
(3)反应3的化学方程式为
(4)反应6的离子方程式为
(5)Na2SO3在空气中易变质生成
(6)已知蓝矾的溶解度随温度变化如图所示。

从CuSO4溶液中提取蓝矾,采用“一系列操作”包括蒸发浓缩、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
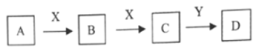
【推荐1】下列物质的转化中,A、X是常见单质,Y在常温下为无色液体,B、C、D均为中学化学中常见的化合物,它们之间的转化关系如图所示(部分产物和反应条件已略去)。
回答下列问题:
(1)若B为能导致酸雨的气体,则D的化学式可能是_______ 。
(2)若C为淡黄色固体,D为强碱溶液,则C→D的离子方程式为_______ 。
(3)若A为淡黄色固体,D为强酸,则D的浓溶液与铜反应生成气体B的化学方程式为_______ 。
(4)若A为黄绿色气体,X为常见金属,则X与B溶液反应的离子方程式为_______ 。

回答下列问题:
(1)若B为能导致酸雨的气体,则D的化学式可能是
(2)若C为淡黄色固体,D为强碱溶液,则C→D的离子方程式为
(3)若A为淡黄色固体,D为强酸,则D的浓溶液与铜反应生成气体B的化学方程式为
(4)若A为黄绿色气体,X为常见金属,则X与B溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图中每一个方格表示有关的一种反应物或生成物(部分的产物已省略);X加热产生等物质的量的A、B、C三种物质,常温下A、C为无色气体,B是一种生活中常见的液体;X与NaOH溶液在加热作用下产生一种能遇浓盐酸产生白烟的气体C;X与HCl反应产生一种无色无味的气体A,它能使澄清石灰变浑浊。请填下列空白:

(1)物质X是_______ (填写化学式)
(2)X中阳离子的检验方法是_______ 。
(3)反应①的化学方程式_______ 。
(4)F→G的化学方程式_______ 。
(5)G→E的离子方程式_______ 。
(6)将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为_______ mol

(1)物质X是
(2)X中阳离子的检验方法是
(3)反应①的化学方程式
(4)F→G的化学方程式
(5)G→E的离子方程式
(6)将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出,金属铝可跟氢氧化钠溶液反应,反应原理如下: )。
)。
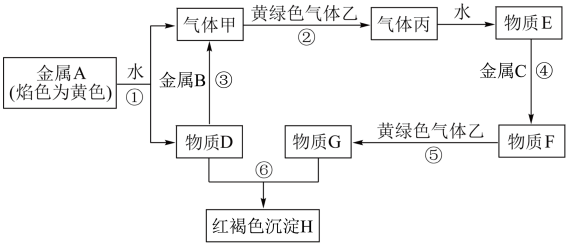
请根据以上信息回答下列问题:
(1)写出下列物质的化学式A___________ ;B___________ ;C___________ ;乙___________ 。
(2)写出下列反应的化学方程式:反应①___________ ;反应②___________ 。
(3)写出下列反应的离子方程式:反应④___________ ;反应⑥___________ 。
 )。
)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式A
(2)写出下列反应的化学方程式:反应①
(3)写出下列反应的离子方程式:反应④
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
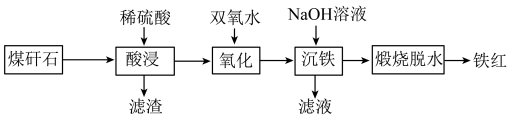
【推荐1】由煤矸石(主要成分为SiO2及铁铝的氧化物,还含有少量CaO)制备铁红的工艺流程如图。___________ (任写两条)。
(2)滤渣的主要成分是___________ 。
(3)“氧化”过程中发生反应的离子方程式为___________ 。
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和___________ 。
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
(2)滤渣的主要成分是
(3)“氧化”过程中发生反应的离子方程式为
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
A.铁红的化学式为 | B.铁红是具有磁性的晶体 |
| C.铁红属于碱性氧化物 | D.铁红常用作油漆、涂料的红色颜料 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铜是一种重要的战略物资,以黄铜矿(主要成分是CuFeS2)为主要原料生产铜、铁红、单质硫时,原料的综合利用率较高,其主要流程如图所示(已知Na[CuCl2]的电离方程式为:Na[CuCl2]=Na++[CuCl2]-):
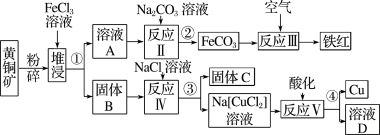
(1)操作①、②、③、④的目的相同,在实验中这种操作的名称是____________ 。铁红的重要用途:_______________ (写其中一种)。
(2)流程中粉碎的目的是______________________________________ 。
(3)固体B中含有两种产物,一种是单质C,另一种是原子个数比为1:1 的一种金属的低价态盐,写出堆浸时反应的化学方程式:______________________________________ 。
(4)反应V的离子方程式:______________________________________ 。
(5)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如下图所示的装置进行电解精炼, e电极上的电极反应式为____________________________________ 。

若当电路中有2mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为(假设杂质只有铁且精炼时铜与铁的放电比例与混合物的物质的量之比相同,计算时用%表示保留一位小数)_______________ 。

(1)操作①、②、③、④的目的相同,在实验中这种操作的名称是
(2)流程中粉碎的目的是
(3)固体B中含有两种产物,一种是单质C,另一种是原子个数比为1:1 的一种金属的低价态盐,写出堆浸时反应的化学方程式:
(4)反应V的离子方程式:
(5)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如下图所示的装置进行电解精炼, e电极上的电极反应式为

若当电路中有2mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为(假设杂质只有铁且精炼时铜与铁的放电比例与混合物的物质的量之比相同,计算时用%表示保留一位小数)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示:

已知:最高价含铬酸根在酸性介质中以 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
回答下列问题:
(1)若铬钒渣中铬的含氧酸盐为NaCrO2,则“煅烧”过程中NaCrO2发生反应的化学方程式为___________ 。若在实验室中进行煅烧铬钒渣,___________ (填“能”或“不能”)用陶瓷坩埚,理由是___________ 。
(2)Fe2O3是___________ (填“酸性”、“碱性”或“两性”)氧化物,写出它在日常生活中的一种用途:___________ 。
(3)“沉淀”步骤中生成H2SiO3反应的离子方程式为___________ 。
(4)“还原”步骤中氧化剂与还原剂的物质的量之比为___________ 。
(5)若取10kg含Cr元素质量分数为13%的铬钒渣进行上述流程,Cr元素在整个流程中损失率为5%,则可制得Cr(OH)3固体的质量为___________ (保留3位有效数字)kg。

已知:最高价含铬酸根在酸性介质中以
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。回答下列问题:
(1)若铬钒渣中铬的含氧酸盐为NaCrO2,则“煅烧”过程中NaCrO2发生反应的化学方程式为
(2)Fe2O3是
(3)“沉淀”步骤中生成H2SiO3反应的离子方程式为
(4)“还原”步骤中氧化剂与还原剂的物质的量之比为
(5)若取10kg含Cr元素质量分数为13%的铬钒渣进行上述流程,Cr元素在整个流程中损失率为5%,则可制得Cr(OH)3固体的质量为
您最近一年使用:0次



