下列有关说法或操作中,正确的有( )
①标准状况下,1 mol溴单质的体积约为22.4 L ②用托盘天平称量50.56 g KCl固体 ③用酒精从饱和碘水中萃取碘
④让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路” ⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法
①标准状况下,1 mol溴单质的体积约为22.4 L ②用托盘天平称量50.56 g KCl固体 ③用酒精从饱和碘水中萃取碘
④让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路” ⑤从含有少量氯化钠的硝酸钾溶液中提取硝酸钾可用结晶的方法
| A.1个 | B.2个 |
| C.3个 | D.4个 |
更新时间:2017-09-07 07:17:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】利用表中提供的仪器和药品,能达到相应实验目的的是
| 选项 | 仪器 | 药品 | 实验目的 |
| A | 烧杯、玻璃棒、胶头滴管 | FeCl3溶液、NaOH溶液 | 制Fe(OH)3胶体 |
| B | 圆底烧瓶、导气管、烧杯、铁架台 | 干燥的二氧化碳气体、蒸馏水 | 模拟喷泉实验 |
| C | 托盘天平(带砝码)、胶头滴管、烧杯、玻璃棒 | 98%浓硫酸、蒸馏水 | 配制一定物质的量浓度的稀硫酸 |
| D | 酒精灯、玻璃棒、蒸发皿、三脚架 | NaCl溶液 | 蒸发溶液得到晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对反应速率的影响 | 将装有NO2的密闭烧瓶浸泡在冰水中 |
| B | 提纯混有氯化氢和水蒸气的氯气 | 将氯气依次通过浓硫酸和饱和食盐水 |
| C | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和FeCl3溶液中 |
| D | 比较乙醇和水中氢的活泼性 | 分别将少量钠投入盛有无水乙醇和水的烧杯中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加 德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LCCl4中含有C-Cl键的数目为1.5NA |
| B.7.8g苯中含碳碳单键的数目为0.3NA |
| C.1L0.1mol·L−1硫酸钠溶液中含有的氧原子数为0.4NA |
| D.常温下,14g乙烯和丙烯混合气体中的氢原子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA表示阿伏加德罗常数的值,下列判断正确的是
A. 参加反应转移电子数一定为2NA 参加反应转移电子数一定为2NA |
B.标准状况下,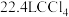 中含有的原子数目为2NA 中含有的原子数目为2NA |
C.常温常压下, 中含有质子数为3NA 中含有质子数为3NA |
D.在常温常压下,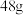 氧气和臭氧的混合气体含氧原子数是3NA 氧气和臭氧的混合气体含氧原子数是3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.7.8g Na2O2 与足量的水反应产生氧气,转移的电子数为0.2NA |
| B.标准状况下,2.24 L CH3OH中含有的H原子数为0.4NA |
C. 溶液中含有的 Na+数为0.1NA 溶液中含有的 Na+数为0.1NA |
| D.3.2g N2H4 中含有的极性共价键数为0.4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】分离或提纯下列物质,所选用的试剂或方法不正确 的是
A.除去 溶液中的少量 溶液中的少量 :选用适量的 :选用适量的 溶液 溶液 |
| B.除去氯气中混有少量氯化氢:将气体通过饱和氯化钠溶液洗气 |
| C.除去二氧化硅中的碳酸钙:加入足量盐酸后过滤 |
| D.除去氯化亚铁溶液中的氯化铁:加入足量铜粉后再过滤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】电石渣的主要成分为 ,含少量的
,含少量的 、
、 和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有
和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有 。
。
 ,含少量的
,含少量的 、
、 和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有
和C等杂质。从中回收制备高纯碳酸钙的工艺流程如下。已知:浸出液的金属阳离子只有 。
。
| A.本流程中可以循环使用的物质是氨气和氯化铵 |
| B.系列操作为洗涤和干燥 |
C.已知: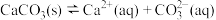 ,则 ,则 属于弱电解质 属于弱电解质 |
D.滤渣1的成分为 、 、 和C 和C |
您最近一年使用:0次



