轻质氧化镁是新型功能复合材料的重要添加剂,可由菱镁矿(含MgCO3、CaCO3、Fe2O3、Al2O3、SiO2)为原料制备,其制备流程如下:
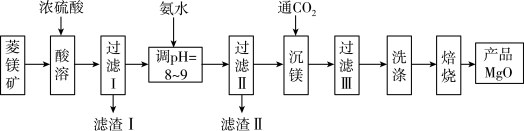
(1)酸溶时,为了提高酸溶速率可采用的措施有______ ;提高矿物的浸取率可采取的措施有______ 。(各答一条即可)
(2)浓硫酸与Al2O3反应的化学方程式为___________ ;滤渣I的主要成分为______ 和______ (填化学式)。
(3)用氨水调节溶液pH =8~9的目的是______ ,若氨水加的量较多使pH >9,则最终氧化镁的产量会______ (填“增大”“不变”或“减小”)。
(4)沉镁时发生反应的离子方程式为________________ 。
(5)流程中“焙烧”操作若在实验室中进行,样品应放在______ 中加热(填仪器名称),当______ 时,说明固体样品已分解完全。

(1)酸溶时,为了提高酸溶速率可采用的措施有
(2)浓硫酸与Al2O3反应的化学方程式为
(3)用氨水调节溶液pH =8~9的目的是
(4)沉镁时发生反应的离子方程式为
(5)流程中“焙烧”操作若在实验室中进行,样品应放在
更新时间:2017-09-10 22:06:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域。一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如下:
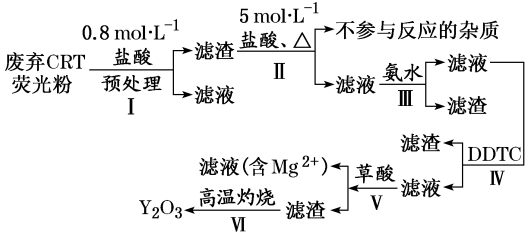
已知:废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)
试回答步骤I中进行原料预处理的目的为_______ 。

已知:废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)
| 成分含量/% | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
试回答步骤I中进行原料预处理的目的为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式是NaAl(OH)2CO3。关于该物质的说法正确的是( )
II.铝是现今人类生产生活中使用广泛性仅次于铁的重要金属。工业上常以“钒土矿”为原料来冶炼金属铝。已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质)。为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
①取矿样10.0 g加入过量稀盐酸溶解(假定其他未知成分的杂质都不溶于盐酸,也不和盐酸反应),过滤弃去不溶残渣。
②将滤液稀释并在250 mL容量瓶中定容后,取25.0 mL逐滴滴加2.5 mol·L-1的NaOH溶液,得到如图所示的变化关系。请根据有关数据回答下列问题:
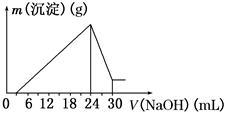
(1)写出滴加NaOH溶液0~3 mL时发生反应的离子方程式:________________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为______ ,其物质的量为____________ 。
(3)该钒土矿样中Al2O3的质量分数为________ 。
(4)用10.0 t“钒土矿”样提纯所得的Al2O3(提纯过程的损耗忽略不计)进行电解,理论上在_____ 极(填“阴”,“阳”)最多可制得金属铝________ t。
| A.该物质属于两性氢氧化物 |
| B.该物质是Al(OH)3和Na2CO3的混合物 |
| C.1 mol NaAl(OH)2CO3最多可消耗4 mol H+ |
| D.该药剂不适合于胃溃疡患者服用 |
II.铝是现今人类生产生活中使用广泛性仅次于铁的重要金属。工业上常以“钒土矿”为原料来冶炼金属铝。已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质)。为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
①取矿样10.0 g加入过量稀盐酸溶解(假定其他未知成分的杂质都不溶于盐酸,也不和盐酸反应),过滤弃去不溶残渣。
②将滤液稀释并在250 mL容量瓶中定容后,取25.0 mL逐滴滴加2.5 mol·L-1的NaOH溶液,得到如图所示的变化关系。请根据有关数据回答下列问题:

(1)写出滴加NaOH溶液0~3 mL时发生反应的离子方程式:
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该钒土矿样中Al2O3的质量分数为
(4)用10.0 t“钒土矿”样提纯所得的Al2O3(提纯过程的损耗忽略不计)进行电解,理论上在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失.
(1)写出该反应的离子方程式_________________ ,其中钠熔成闪亮小球的原因是__________
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式_____________
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式_________ ;继续将沉淀过滤、洗涤、干燥、灼烧,此时得到的固体为_________ (填化学式)。
(1)写出该反应的离子方程式
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.根据下表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填入对应“答案”的空格中。
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是_____________ 。
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有_______________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3_______ NaHCO3(填“>”或“<”)。
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为__________ L(标准状况)。
| 实验操作 | 答案 | 实验现象 |
| (1)让一束光线通过Fe(OH)3胶体 | A.呈蓝色 B.生成白色胶状沉淀 C.呈现光亮“通路” D.产生红褐色沉淀 | |
| (2)向盛有FeCl3溶液的试管中加入NaOH溶液 | ||
| (3)向Al2(SO4)3溶液中滴加氨水 | ||
| (4)向土豆片上滴加碘水 |
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
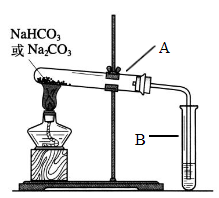
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热煮沸饱和FeCl3溶液;
丙同学向25mL沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是__ ;若丙同学实验中不停止加热,会看到__ 。
(2)证明有Fe(OH)3胶体生成的实验操作及现象是__ 。
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明__ 。
②向其中加入稀硫酸,产生的现象是___ 。
甲同学向1mol·L-1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热煮沸饱和FeCl3溶液;
丙同学向25mL沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的实验操作及现象是
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明
②向其中加入稀硫酸,产生的现象是
您最近一年使用:0次

 2AlN+_______;
2AlN+_______;

