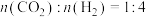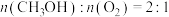有关碰撞理论,下列说法中正确的是
| A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应. |
| B.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 |
| C.催化剂不影响反应活化能,从而只影响反应速率而不影响化学平衡 |
| D.升温能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
更新时间:2017-10-11 22:15:56
|
【知识点】 影响化学反应速率的外因
相似题推荐
单选题
|
适中
(0.65)
【推荐1】M溶液受热会发生分解反应。体积均为2L的4组溶液(忽略反应前后体积的变化),M的物质的量随时间的变化如下表,则下列说法不正确的是
| 0min | 10min | 20min | 30min | 40min | 50min | 60min | ||
| ① | 10℃ | 1.1 | 0.90 | 0.80 | 0.73 | 0.68 | 0.65 | 0.65 |
| ② | 10℃ | a | 0.70 | 0.65 | 0.65 | 0.65 | 0.65 | 0.65 |
| ③ | 25℃ | 1.0 | 0.70 | 0.50 | 0.35 | 0.25 | 0.20 | 0.20 |
| ④ | 30℃ | 2.0 | 1.4 | 0.90 | 0.50 | 0.20 | 0.13 | 0.13 |
| A.在10-20min内,实验①中M的平均分解速率为0.005mol/(L·min) |
| B.a>1.1,且说明浓度越大反应速率越快 |
| C.对比实验①和④,不能说明M的平均反应速率随温度升高而增大 |
| D.不考虑其它影响因素,仅由③可知,反应物浓度越大反应速率越快 |
您最近一年使用:0次
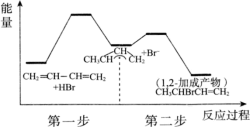
【推荐2】1,3-丁二烯(CH2=CH—CH=CH2)与HBr发生1,2-加成反应分两步进行:第一步H+讲攻1,3-T二烯生成碳正离子(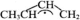 );第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
);第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
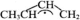 );第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
);第二步Br-进攻碳正离子完成1,2-加成反应,反应过程中的能量变化如下图所示。下列说法正确的是
| A.两步均为吸热反应 |
| B.该总反应为放热反应 |
| C.第一步反应速率大于第二步反应速率 |
| D.加入催化剂可以改变该反应的反应热 |
您最近一年使用:0次

 人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
人工合成淀粉,使淀粉生产方式从农耕种植转变为工业制造成为可能,其部分转化过程如下:
 水解可制得
水解可制得 。
。