随原子序数的递增,八种短周期元素(用字母x表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同)________________ ;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:__________ 。
(4)已知1mol e 的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:__________________ 。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同)
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)已知1mol e 的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:
更新时间:2017-10-23 14:26:13
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮元素可以形成多种化合物。肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。已知肼可用作火箭燃料,燃烧时发生的反应为N2O4(g)+2N2H4(g)=3N2(g)+4H2O(g) △H=-1040kJ•mol-1。回答下列问题:
(1)该反应的能量变化与如图所示能量变化不相符的是______ (填标号)。
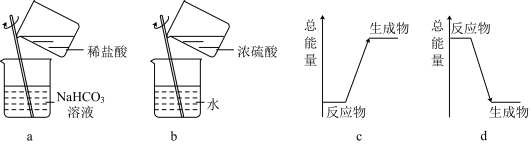
(2)该反应每放出520kJ热量,同时有_____ molσ键形成,有_____ molN-H键断裂。
(3)N2H4的电子式可表示为______ ,该分子中N原子的杂化方式为______ 。
(4)叠氮化合物在化学工业上有重要的应用。N 被称为叠氮离子,1个N
被称为叠氮离子,1个N 中含有
中含有_____ 个电子;请写出与N 具有等电子数的物质的化学式:
具有等电子数的物质的化学式:_____ (写一种)。
(1)该反应的能量变化与如图所示能量变化不相符的是

(2)该反应每放出520kJ热量,同时有
(3)N2H4的电子式可表示为
(4)叠氮化合物在化学工业上有重要的应用。N
 被称为叠氮离子,1个N
被称为叠氮离子,1个N 中含有
中含有 具有等电子数的物质的化学式:
具有等电子数的物质的化学式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂。它是一种白色固体,微溶于冷水,化学性质与过氧化钠类似。某实验小组在碱性环境中利用CaCl2与H2O2反应制取CaO2•8H2O,装置如图所示。

回答下列问题:
(1)CaO2的电子式为_______ 。
(2)实验室制备NH3的化学方程式为_______ 。
(3)仪器B的主要作用除导气外,还具有的作用是_______ 。
(4)已知该反应是放热反应,采用冰水浴的优点是_______ (任写一条)。
(5)实验时,在三颈烧瓶中析出CaO2•8H2O晶体,总反应的离子方程式为_______ ;反应结束后,分离提纯CaO2•8H2O的过程中,洗涤的操作为_______ 。
(6)若CaCl2原料中含有Fe3+杂质,Fe3+催化分解H2O2,会使H2O2的利用率明显降低。反应的机理为:
①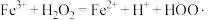
② (已配平)
(已配平)
③
④
根据上述机理推导步骤②中的化学方程式为_______ 。

回答下列问题:
(1)CaO2的电子式为
(2)实验室制备NH3的化学方程式为
(3)仪器B的主要作用除导气外,还具有的作用是
(4)已知该反应是放热反应,采用冰水浴的优点是
(5)实验时,在三颈烧瓶中析出CaO2•8H2O晶体,总反应的离子方程式为
(6)若CaCl2原料中含有Fe3+杂质,Fe3+催化分解H2O2,会使H2O2的利用率明显降低。反应的机理为:
①
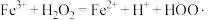
②
 (已配平)
(已配平)③

④

根据上述机理推导步骤②中的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是中学化学中常见物质的转化关系。E为红棕色气体,单质G可被磁铁吸引, 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
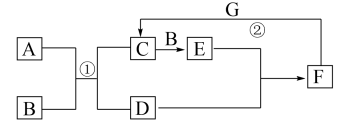
回答下列问题:
(1)D的电子式为_____ ,C的化学式是_____ 。
(2)实验室中常将F的浓溶液保存在_____ 色细口瓶中并置于阴凉处。用化学方程式解释原因______ 。
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为_____ 。
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式______ 。
 和
和 的浓溶液靠近会出现白烟。
的浓溶液靠近会出现白烟。
回答下列问题:
(1)D的电子式为
(2)实验室中常将F的浓溶液保存在
(3)过量G发生反应②后,向溶液中加入足量氢氧化钠溶液,现象为
(4)为防止E污染环境,可用CH4与其反应生成无污染气体和水,写出该反应的化学方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】综合利用CO2、CO对构建低碳社会有重要意义。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
①10min后达到平衡时CO的浓度为_______ ;
②10min内用H2表示的平均反应速率为_______ ;
③若要加快CH3OH的生成速率,可采取的措施有_______ 填一种合理的措施)
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2 CH2=CH2+4H2O
CH2=CH2+4H2O
①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,写出该反应的热化学方程式_______ 。
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。

下列有关说法不正确的是_______ (填序号)。
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为_______ 。(保留两位有效数字)
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为_______ 。
(1)利用H2 和CO在一定条件下发生如下反应:CO(g)+2H2(g)
 CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。
CH3OH(g)(放热反应)。对此反应进行如下研究:在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。①10min后达到平衡时CO的浓度为
②10min内用H2表示的平均反应速率为
③若要加快CH3OH的生成速率,可采取的措施有
(2)利用H2 和CO2在一定条件下可以合成乙烯:6H2+2CO2
 CH2=CH2+4H2O
CH2=CH2+4H2O①已知:4.4gCO2与H2完全转化为CH2=CH2和水(气态)共放出6.39kJ的热量,写出该反应的热化学方程式
②不同温度对CO2的转化率及催化剂的催化效率的影响如图甲所示。

下列有关说法不正确的是
A.不同条件下反应,N点的速率最大
B.温度在约250℃时,催化剂的催化效率最高
C.相同条件下,乙烯的产量M点比N高
③若在密闭容器中充入体积比为 3∶1的 H2和CO2,则图甲中M点时,产物CH2=CH2的体积分数为
(3)利用一种钾盐水溶液作电解质,CO2电催化还原为乙烯,如图乙所示。在阴极上产生乙烯的电极反应方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y.已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
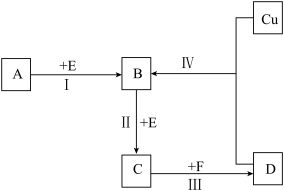
(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为_____________________ 。
②反应Ⅰ的化学方程式为_________________ 。
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式_______________________________________ 。
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol ,则:
,则:
①反应Ⅳ的溶液加热蒸干所得的晶体属于_______ 晶体(填“离子”、“分子”、“原子”).
②反应I的化学方程式为__________________________ 。
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式___________________________________ 。

(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为
②反应Ⅰ的化学方程式为
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol
 ,则:
,则:①反应Ⅳ的溶液加热蒸干所得的晶体属于
②反应I的化学方程式为
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】455°C下,向某2L密闭容器中通入1mol HI发生反应2HI(g)  H2(g)+I2(g), ∆H >0, 反应在2min时达到平衡,已知该温度下,反应H2(g)+I2(g)
H2(g)+I2(g), ∆H >0, 反应在2min时达到平衡,已知该温度下,反应H2(g)+I2(g)  2HI(g)的平衡常数为49。
2HI(g)的平衡常数为49。
(1)该温度下反应2HI(g) H2(g)+I2(g)的平衡常数为
H2(g)+I2(g)的平衡常数为______
(2)0-2min 中内以HI表示的反应速率为______ (用3位小数表示)
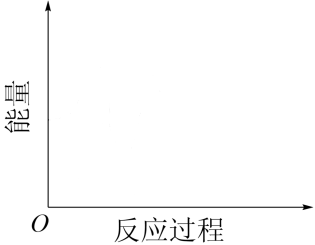
(3)反应实际分为两步:反应①2HI→H2+2I·,反应②2I·→I2。已知反应①吸热,反应②放热,且总反应速率由反应①决定,请在图中画出反应的反应进程一能量图______ 。
(4)下列关于该反应的说法中不正确的是
(5)25°C时,1molHI 完全分解为H2和I2时,放出26.5kJ热量,写出该温度下分解HI分解反应的热化学方程式_______ 。
 H2(g)+I2(g), ∆H >0, 反应在2min时达到平衡,已知该温度下,反应H2(g)+I2(g)
H2(g)+I2(g), ∆H >0, 反应在2min时达到平衡,已知该温度下,反应H2(g)+I2(g)  2HI(g)的平衡常数为49。
2HI(g)的平衡常数为49。(1)该温度下反应2HI(g)
 H2(g)+I2(g)的平衡常数为
H2(g)+I2(g)的平衡常数为(2)0-2min 中内以HI表示的反应速率为
(3)反应实际分为两步:反应①2HI→H2+2I·,反应②2I·→I2。已知反应①吸热,反应②放热,且总反应速率由反应①决定,请在图中画出反应的反应进程一能量图

(4)下列关于该反应的说法中不正确的是
| A.升高温度,活化分子百分数增加,反应速率增大 |
| B.活化分子的碰撞都是有效碰撞 |
| C.使用合适的催化剂,可以增大反应速率和HI的平衡转化率 |
| D.恒温恒容下达平衡后,再充入少量HI,达新平衡后,HI的总转化率不变 |
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1∶2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素Y的单质的电子式为________ 。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为______________ 。
(3)元素W非金属性比R弱,用原子结构的知识解释原因:___________________ 。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:_____________________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为__________ 。
(1)元素Y的单质的电子式为
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(3)元素W非金属性比R弱,用原子结构的知识解释原因:
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1∶3,则该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表给出了五种元素的相关信息,其中X、Y、Z、W为短周期元素。
根据上述信息填空:
(1)Y元素的原子含有___________ 个能层,其中第二能层中的能级包括___________ ;画出W元素原子的结构示意图:___________ ;M元素是___________ (填元素符号)。
(2)Z与X形成的某种化合物能和Z与Y形成的另一种无色化合物(这两种化合物分子中Z与另一元素原子的个数比均为1:2)一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:___________ 。
| 元素 | 相关信息 |
| X | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| Y | 工业上通过分离液态空气获得它的一种单质,含它的另一种单质的浓度相对较高的平流层是保护地球地表环境的重要屏障 |
| W | 植物生长所需的主要元素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| Z | 室温下其单质为粉末状固体,加热易熔化。该单质在氧气中燃烧发出明亮的蓝紫色火焰 |
| M | 它是人体不可缺少的微量元素,含该元素的合金是工业生产中不可缺少的金属材料,常用于建造桥梁楼房等 |
(1)Y元素的原子含有
(2)Z与X形成的某种化合物能和Z与Y形成的另一种无色化合物(这两种化合物分子中Z与另一元素原子的个数比均为1:2)一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素名称: A____________ B ____________ C ____________ D ____________ 。
(2)写出AB2的电子式为___________ 。
(3)用电子式表示化合物C2D的形成过程___________________________________ 。
(1)元素名称: A
(2)写出AB2的电子式为
(3)用电子式表示化合物C2D的形成过程
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,字母a-i代表相应元素,回答下列问题:

(1)b、g元素分别为:_______ 、_______ (填元素符号),元素h在周期表中的位置是_______ 。
(2)元素e、f、h、i形成的简单离子中,半径最小的是_______ (填离子符号)。
(3)由元素a与e的单质化合,形成的产物是工业上常用的还原剂,其电子式为_______ 。
(4)常温下,元素e的最高价氧化物对应的水化物与元素g的最高价氧化物反应的离子方程式为_______ 。
(5)元素i的单质通入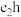 溶液中,产生浅黄色沉淀,该反应的离子方程式为
溶液中,产生浅黄色沉淀,该反应的离子方程式为_______ ,该实验说明i的非金属性强于h,从原子结构的角度解释其原因_______ 。
(6)a可以分别与c、d形成电子数为18的X和Y分子,X是一种良好的火箭燃料,Y是一种绿色氧化剂,二者常温下均为液态,X和Y反应生成c的单质的化学反应方程式为_______ 。

(1)b、g元素分别为:
(2)元素e、f、h、i形成的简单离子中,半径最小的是
(3)由元素a与e的单质化合,形成的产物是工业上常用的还原剂,其电子式为
(4)常温下,元素e的最高价氧化物对应的水化物与元素g的最高价氧化物反应的离子方程式为
(5)元素i的单质通入
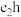 溶液中,产生浅黄色沉淀,该反应的离子方程式为
溶液中,产生浅黄色沉淀,该反应的离子方程式为(6)a可以分别与c、d形成电子数为18的X和Y分子,X是一种良好的火箭燃料,Y是一种绿色氧化剂,二者常温下均为液态,X和Y反应生成c的单质的化学反应方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表列出了①~⑨九种元素在周期表中的位置。
回答下列问题:
(1)①~⑨九种元素中,化学性质最不活泼的是_______ (填元素符号)。
(2)元素②的原子结构示意图是_______ 。
(3)元素②和③中原子半径较大的是_______ (填元素符号)。
(4)元素③和④中气态氢化物稳定性较强的是_______ (填化学式)
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是_______ (填化学式)。
(6)元素⑦的单质与⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(7)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是_______ (填化学式),X和Y反应的离子方程式为_______ 。
(8)元素④和⑥形成的化合物中既含有离子键又含有非极性键,该化合物的电子式为_______ ,元素①和③组成的10电子化合物,该分子构型为_______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①~⑨九种元素中,化学性质最不活泼的是
(2)元素②的原子结构示意图是
(3)元素②和③中原子半径较大的是
(4)元素③和④中气态氢化物稳定性较强的是
(5)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是
(6)元素⑦的单质与⑥的最高价氧化物对应的水化物反应的离子方程式为
(7)元素⑥和⑦的最高价氧化物对应的水化物分别为X和Y,其中碱性较强的是
(8)元素④和⑥形成的化合物中既含有离子键又含有非极性键,该化合物的电子式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表的建立是化学发展史上的重要里程碑之一,部分元素在元素周期表中的位置如图:
(1)a、b、d、f、h五种元素原子的最外层电子数之和为_______ 。
(2)能比较得出h、j非金属性强弱的离子反应方程式为_______ (用化学符号表示,下同)。
(3)b、c、f、g四种元素简单离子中,半径最大的是_______ ,半径最小的是_______ 。
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式_______ 。
(5)比较e、g、h最高价含氧酸酸性强弱:_______ >_______ >_______ (写出具体物质化学式)。
| 族 周期 | ⅠA | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | f | ||||||
| 3 | b | c | d | e | g | h | |
| 4 | i | Ca | j |
(2)能比较得出h、j非金属性强弱的离子反应方程式为
(3)b、c、f、g四种元素简单离子中,半径最大的是
(4)写出d的最高价氧化物和b的最高价氧化物的水化物在水溶液中发生的离子反应方程式
(5)比较e、g、h最高价含氧酸酸性强弱:
您最近半年使用:0次



