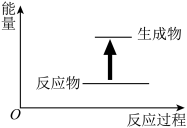
下列说法或表示方法正确的是
| A.反应物的总能量低于生成物的总能量时,该反应一定不能发生 |
| B.化学反应中的能量变化都是以热量的形式体现 |
| C.任何化学反应都伴随着能量的变化 |
| D.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq) == CH3COONa(aq) + H2O(l) △H =-57.4kJ·mol-1 |
更新时间:2017-10-21 17:35:00
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知: 。相关共价键的键能如下表:
。相关共价键的键能如下表:
则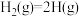 的
的 为
为
 。相关共价键的键能如下表:
。相关共价键的键能如下表:| 共价键 | 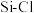 |  |  |
键能/ |  | 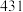 | 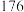 |
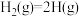 的
的 为
为A.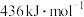 | B. |
C.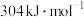 | D.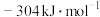 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】肼 是一种应用广泛的化工原料,可用作火箭发动机的燃料,已知
是一种应用广泛的化工原料,可用作火箭发动机的燃料,已知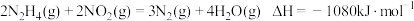 。下列说法正确的是
。下列说法正确的是
 是一种应用广泛的化工原料,可用作火箭发动机的燃料,已知
是一种应用广泛的化工原料,可用作火箭发动机的燃料,已知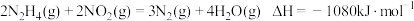 。下列说法正确的是
。下列说法正确的是A.该反应逆反应的活化能 一定大于 一定大于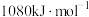 |
B.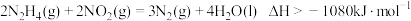 |
| C.该反应反应物的总键能大于生成物的总键能 |
| D.该反应反应物的总能量小于生成物的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】已知下列反应的热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036 kJ⋅mol-1
4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH2=+94 kJ⋅mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484kJ⋅mol-1
则H2S热分解反应的2H2S(g)=2H2(g)+S2(g)的ΔH4为
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036 kJ⋅mol-1
4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH2=+94 kJ⋅mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484kJ⋅mol-1
则H2S热分解反应的2H2S(g)=2H2(g)+S2(g)的ΔH4为
| A.-314kJ/mol | B.+170kJ/mol | C.-170kJ/mol | D.+314kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】全球首座第四代核电站——华能石岛湾高温气冷堆核电站商业示范工程圆满完成168小时连续运行考验,正式投入商业运行。下列说法正确的是
| A.利用核能发电时,转化率可达到100% |
| B.以石墨为慢化剂,石墨属于混合型晶体 |
C.以气体氦为冷却剂,气体氦液化的过程中, |
D.慢中子与核燃料铀发生有效反应,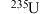 与 与 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知反应X+Y=M+N为放热反应,下列有关说法中正确的是
| A.X的能量一定低于M | B.X和Y的总能量一定高于M和N的总能量 |
| C.Y的能量一定低于N | D.该反应一定不需要加热就能发生 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列属于吸热反应的是
| A.甲烷燃烧 | B.生石灰与水反应 |
| C.石灰石高温分解 | D.锌粒与稀硫酸反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知25℃、101kPa时,2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol,请结合水的聚集状态变化时的焓变示意图分析,下列说法错误的是
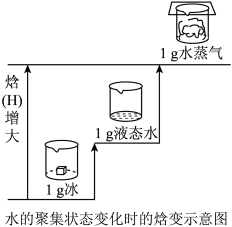

| A.冰融化为水时,需要吸收热量 |
| B.1g冰变为1g水蒸气后化学键数目不变 |
| C.H2的燃烧热△H=-241.8kJ/mol |
| D.△H的单位中“mol-1”指每摩尔反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】如图所示,有关化学反应和能量变化的说法正确的是
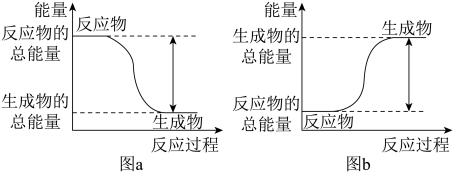

A.图a可以表示 和 和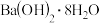 反应的能量变化 反应的能量变化 |
| B.图a中生成物比反应物稳定 |
| C.图b可以表示甲烷燃烧反应的能量变化 |
| D.图b表示的反应一定需要加热才能发生 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列过程中的焓变大于零的是
| A.铝与盐酸反应 | B.食物腐烂 | C.石灰石高温分解 | D.酸碱中和 |
您最近一年使用:0次