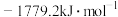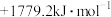已知下列反应的热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036 kJ⋅mol-1
4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH2=+94 kJ⋅mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484kJ⋅mol-1
则H2S热分解反应的2H2S(g)=2H2(g)+S2(g)的ΔH4为
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036 kJ⋅mol-1
4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH2=+94 kJ⋅mol-1
2H2(g)+O2(g)=2H2O(g) ΔH3=-484kJ⋅mol-1
则H2S热分解反应的2H2S(g)=2H2(g)+S2(g)的ΔH4为
| A.-314kJ/mol | B.+170kJ/mol | C.-170kJ/mol | D.+314kJ/mol |
21-22高二下·内蒙古赤峰·期末 查看更多[4]
内蒙古赤峰市2021-2022学年高二下学期期末考试化学试题(已下线)化学反应的热效应——课时2 焓变的计算河南省濮阳市南乐县第一高级中学2022-2023学年高二上学期第一次月考化学试题(已下线)专题02 盖斯定律、反应热的计算【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
更新时间:2022-07-10 17:02:32
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】通过以下反应均可获取H2。下列有关说法正确的是
①焦炭与水反应制氢:C(s)+ H2O(g) = CO(g)+ H2(g) ΔH1 = 131.3 kJ·mol–1
②太阳光催化分解水制氢:2H2O(l) = 2H2(g)+ O2(g) ΔH2 = 571.6 kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) = CO(g)+3H2(g) ΔH3 = 206.1 kJ·mol–1
①焦炭与水反应制氢:C(s)+ H2O(g) = CO(g)+ H2(g) ΔH1 = 131.3 kJ·mol–1
②太阳光催化分解水制氢:2H2O(l) = 2H2(g)+ O2(g) ΔH2 = 571.6 kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g) = CO(g)+3H2(g) ΔH3 = 206.1 kJ·mol–1
| A.反应①为放热反应 |
| B.反应②中电能转化为化学能 |
| C.若反应③使用催化剂,ΔH3不变 |
| D.反应2H2(g) + O2(g) = 2H2O(g)的ΔH = -571.6 kJ·mol–1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】CH4联合H2O(g)和CO2制取H2时,发生的主要反应如下:
①CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206kJ•mol-1;
CO(g)+3H2(g) △H1=+206kJ•mol-1;
②CH4(g)+CO2(g) 2CO(g)+2H2(g) △H2=+247kJ•mol-1。
2CO(g)+2H2(g) △H2=+247kJ•mol-1。
将CH4、H2O(g)和CO2按一定比例通入填充有催化剂的恒容反应器,反应相同时间内(反应均未达到化学平衡状态)测得 随温度的变化如图所示。
随温度的变化如图所示。
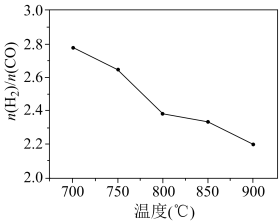
下列说法错误的是
①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+206kJ•mol-1;
CO(g)+3H2(g) △H1=+206kJ•mol-1;②CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H2=+247kJ•mol-1。
2CO(g)+2H2(g) △H2=+247kJ•mol-1。将CH4、H2O(g)和CO2按一定比例通入填充有催化剂的恒容反应器,反应相同时间内(反应均未达到化学平衡状态)测得
 随温度的变化如图所示。
随温度的变化如图所示。
下列说法错误的是
| A.随着温度的升高,温度对反应②速率的影响大于对反应①速率的影响 |
B.由①②可知,CO(g)+H2O(g) CO2(g)+H2(g) △H=-41kJ•mol-1 CO2(g)+H2(g) △H=-41kJ•mol-1 |
| C.其他条件不变时升高温度,反应①的正反应速率增大、逆反应速率减小 |
D.其他条件不变时,增大原料中H2O(g)的浓度可以提高产物中 的值 的值 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】有三个热化学方程式:①2H2(g)+O2(g)=2H2O(g) ΔH1;②2H2(g)+O2(g)=2H2O(l)ΔH2;③H2(g)+ O2(g)=H2O(g) ΔH3;其中ΔH1、ΔH2、ΔH3的大小关系为
O2(g)=H2O(g) ΔH3;其中ΔH1、ΔH2、ΔH3的大小关系为
 O2(g)=H2O(g) ΔH3;其中ΔH1、ΔH2、ΔH3的大小关系为
O2(g)=H2O(g) ΔH3;其中ΔH1、ΔH2、ΔH3的大小关系为| A.ΔH1=ΔH2=ΔH3 | B.2ΔH3=ΔH1>ΔH2 |
| C.ΔH3>ΔH2>ΔH1 | D.ΔH2>ΔH1>ΔH3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】实验室用4mol SO2与2molO2在一定条件下进行下列反应:2SO2(g)+O2(g) 2SO3(g); △H=-197kJ·mol-1,当放出 315.2kJ热量时,SO2转化率为
2SO3(g); △H=-197kJ·mol-1,当放出 315.2kJ热量时,SO2转化率为
 2SO3(g); △H=-197kJ·mol-1,当放出 315.2kJ热量时,SO2转化率为
2SO3(g); △H=-197kJ·mol-1,当放出 315.2kJ热量时,SO2转化率为| A.40% | B.50% | C.80% | D.90% |
您最近一年使用:0次

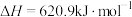 。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是(
。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是(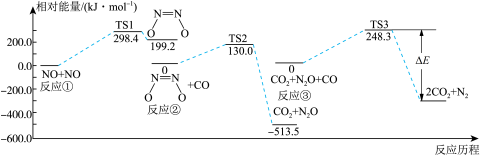


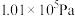 时,
时,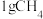 燃烧生成
燃烧生成 与液态
与液态 放出
放出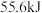 的热量,则生成
的热量,则生成 时的反应热为
时的反应热为