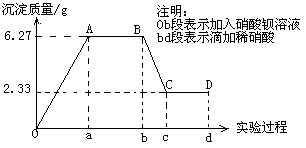
下列是某研究性学习小组对某无色水样成分的检测过程,已知该水样中只可能含有K+ 、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子,该小组同学取了100ml水样进行实验:向水样中先滴加硝酸钡溶液,再滴加1mol·L-1硝酸,实验过程中沉淀质量与所加试剂量的关系变化如下图所示:
(1)观察知该水样中一定不含有的阳离子是________ 。
(2)水样中一定含有的阴离子是________ 其相应的物质的量比为________ 。
(3)试根据实验结果推测K+是否存在_______ (填“是”或“否”)若存在,其物质的量浓度的范围是______ mol·L-1(若不存在,则不必回答)。
(4)设计简单实验验证原水样中可能存在的离子_______________________________________________ (写出实验步骤、现象和结论)。
(1)观察知该水样中一定不含有的阳离子是
(2)水样中一定含有的阴离子是
(3)试根据实验结果推测K+是否存在
(4)设计简单实验验证原水样中可能存在的离子
17-18高三上·山西忻州·阶段练习 查看更多[2]
更新时间:2017-10-21 22:20:39
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某强酸性透明溶液中可能含有 、
、 、
、 、
、 、
、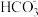 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:
①取该溶液 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到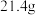 固体。
固体。
②向上述滤液中加入足量的 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。
已知:含 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。
(1)该溶液中一定含有___________ ;可能含有___________ ,可以用定性分析操作___________ 来进行检验。若含有,现象是:___________ 。
(2)计算:该 溶液中,若
溶液中,若 ,则
,则
___________ 。
(3)已知 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式___________ ;当某溶液 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有___________ 。
a. b.
b.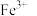 c.
c. d.
d. e.
e.
 、
、 、
、 、
、 、
、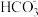 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:①取该溶液
 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到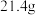 固体。
固体。②向上述滤液中加入足量的
 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。已知:含
 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。(1)该溶液中一定含有
(2)计算:该
 溶液中,若
溶液中,若 ,则
,则
(3)已知
 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有a.
 b.
b.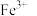 c.
c. d.
d. e.
e.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】Ⅰ.某溶液中可能含有Na+、Ca2+、NO 、CO
、CO 、SO
、SO 、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行如下实验:
、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行如下实验:
①加入稀盐酸后,生成无色无味的气体,将气体通入澄清石灰水,变浑浊。
②加入足量的BaCl2溶液,产生白色沉淀,过滤,在沉淀中加入足量的盐酸,沉淀不能完全溶解。
③取②中滤液,加入硝酸酸化后,再加入过量的AgNO3溶液,析出白色沉淀。
(1)由实验可知一定存在的离子是_______ ,一定不存在的离子是_______ ,可能存在的离子是_______ 。
Ⅱ.炼金废水中含有配离子[Au(CN)2]+,其电离出的CN-有毒,在酸性水溶液中,CN-与H+结合生成易挥发的HCN,其毒性更强。回答下列问题:
(2)HCN的电离方程式为_______ 。
(3)HCN的结构式为(所有元素均达8电子或2电子稳定结构)_______ 。
(4)处理炼金废水常在碱性条件下,用NaClO将CN-氧化为CO 和N2,其反应的离子方程式为
和N2,其反应的离子方程式为_______ 。
(5)实际处理该废水时不在酸性条件下进行的主要原因是_______ 。
 、CO
、CO 、SO
、SO 、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行如下实验:
、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行如下实验:①加入稀盐酸后,生成无色无味的气体,将气体通入澄清石灰水,变浑浊。
②加入足量的BaCl2溶液,产生白色沉淀,过滤,在沉淀中加入足量的盐酸,沉淀不能完全溶解。
③取②中滤液,加入硝酸酸化后,再加入过量的AgNO3溶液,析出白色沉淀。
(1)由实验可知一定存在的离子是
Ⅱ.炼金废水中含有配离子[Au(CN)2]+,其电离出的CN-有毒,在酸性水溶液中,CN-与H+结合生成易挥发的HCN,其毒性更强。回答下列问题:
(2)HCN的电离方程式为
(3)HCN的结构式为(所有元素均达8电子或2电子稳定结构)
(4)处理炼金废水常在碱性条件下,用NaClO将CN-氧化为CO
 和N2,其反应的离子方程式为
和N2,其反应的离子方程式为(5)实际处理该废水时不在酸性条件下进行的主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】对一份稀溶液做初步分析后发现,溶液无色、澄清,其中可能含有 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
①用pH试纸检测溶液的酸碱性,结果pH试纸显红色。
②取2mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
(1)溶液中一定存在的离子是________ ,一定不存在的离子是________ 。
(2)上述实验操作中,有错误的操作是________ (填写序号)。改正该错误的方法是(要做较详细的说明)________ 。
(3)到目前为止,仍不能肯定溶液中是否存在的离子是_______ ,若想确定是否含有其中的金属阳离子,应该采用什么方法________ (写出方法即可)。
 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。①用pH试纸检测溶液的酸碱性,结果pH试纸显红色。
②取2mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
(1)溶液中一定存在的离子是
(2)上述实验操作中,有错误的操作是
(3)到目前为止,仍不能肯定溶液中是否存在的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】氧化还原反应在物质制备、能量转化方面有重要的应用。
(1)反应I2+2Na2S2O3=Na2S4O6+2NaI常用于测定溶液中I2的含量。反应的氧化剂是________ ,每生成1 mol Na2S4O6,反应转移电子为________ mol。
(2)ClO2是一种新型净水剂,一种制取ClO2的反应如下:KClO3+HCl(浓)-KCl+Cl2↑+ClO2↑+H2O(未配平)写出配平后的化学方程式:________ 。
(3)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,高铁酸钠可与水反应生成Fe(OH)3胶体、氢氧化钠和氧气,写出相应的离子方程式______________ 。
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、 、
、 、Cl﹣中的几种,现进行如下实验:
、Cl﹣中的几种,现进行如下实验:
①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有__________ ,肯定没有_________ ,可能有_________ (填离子符号)。
(1)反应I2+2Na2S2O3=Na2S4O6+2NaI常用于测定溶液中I2的含量。反应的氧化剂是
(2)ClO2是一种新型净水剂,一种制取ClO2的反应如下:KClO3+HCl(浓)-KCl+Cl2↑+ClO2↑+H2O(未配平)写出配平后的化学方程式:
(3)高铁酸钠(Na2FeO4)可作为高效、多功能水处理剂,高铁酸钠可与水反应生成Fe(OH)3胶体、氢氧化钠和氧气,写出相应的离子方程式
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、
 、
、 、Cl﹣中的几种,现进行如下实验:
、Cl﹣中的几种,现进行如下实验:①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的量是联系宏观和微观的桥梁,请回答下列问题
I.某无色混合物水溶液,可能含有以下离子中的若干种:K+、 、Mg2+、Cu2+、Cl-、
、Mg2+、Cu2+、Cl-、 、
、 ,现各取100 mL 溶液三份进行如下实验:
,现各取100 mL 溶液三份进行如下实验:
①向第一份加入AgNO3溶液,有白色沉淀产生;
②向第二份加入足量NaOH溶液后加热,收集到气体 0.896 L(标准状况)
③向第三份加入足量BaCl2溶液,得到沉淀6.63克,经足量盐酸洗涤后,剩余4.66克。
(1)肯定存在的离子有_______ ,肯定不存在的离子有_______ ;
(2)可能存在的离子是_______ ,判断该离子存在与否的方法是_______ ;
(3)肯定存在的阳离子在原溶液中的物质的量浓度_______ 。
II.将NaOH、Na2CO3的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入2 mol·L-1的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示。

(4)AB段发生反应的离子方程式为_______ 。
(5)当加入35 mL盐酸时,产生CO2的体积(标准状况)为_______ mL。
(6)原混合溶液中NaOH与Na2CO3的物质的量之比为_______ 。
I.某无色混合物水溶液,可能含有以下离子中的若干种:K+、
 、Mg2+、Cu2+、Cl-、
、Mg2+、Cu2+、Cl-、 、
、 ,现各取100 mL 溶液三份进行如下实验:
,现各取100 mL 溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生;
②向第二份加入足量NaOH溶液后加热,收集到气体 0.896 L(标准状况)
③向第三份加入足量BaCl2溶液,得到沉淀6.63克,经足量盐酸洗涤后,剩余4.66克。
(1)肯定存在的离子有
(2)可能存在的离子是
(3)肯定存在的阳离子在原溶液中的物质的量浓度
II.将NaOH、Na2CO3的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入2 mol·L-1的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示。

(4)AB段发生反应的离子方程式为
(5)当加入35 mL盐酸时,产生CO2的体积(标准状况)为
(6)原混合溶液中NaOH与Na2CO3的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】I.写出下列反应的离子方程式:
(1)氢氧化钡溶液和稀硫酸反应:_______
(2)往碳酸氢钙溶液中加入过量氢氧化钠溶液:_______
II.由几种离子组成的混合物中可能含有下列离子中的若干种:K+、Na+、NH 、Mg2+、Cu2+、CO
、Mg2+、Cu2+、CO 、SO
、SO 、将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
、将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
请回答下列问题:
(3)实验1说明存在的离子是_______ (填离子符号,下同),一定不存在的离子是_______ 。
(4)由实验2可知,100mL溶液中c(NH )=
)=_______ mol•L-1。
(5)由实验3可知,100mL溶液中 n(SO )=
)=_______ mol。
(6)溶液中c(Na+)的范围是_______ (用不等式表达)
(1)氢氧化钡溶液和稀硫酸反应:
(2)往碳酸氢钙溶液中加入过量氢氧化钠溶液:
II.由几种离子组成的混合物中可能含有下列离子中的若干种:K+、Na+、NH
 、Mg2+、Cu2+、CO
、Mg2+、Cu2+、CO 、SO
、SO 、将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
、将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:| 序号 | 实验内容 | 实验结果 |
| 1 | 加入盐酸 | 有气泡产生 |
| 2 | 加入足量浓 NaOH 溶液并加热 | 收集到标准状况下的气体 1.12L |
| 3 | 加入足量 BaCl2 溶液,对所得沉淀进行洗涤、干燥、称量; | 第一次称量读数为 6.27g; 再向沉淀中加入足量盐酸,过滤、洗涤、干燥、称量。第二次称量读数为 2.33g |
(3)实验1说明存在的离子是
(4)由实验2可知,100mL溶液中c(NH
 )=
)=(5)由实验3可知,100mL溶液中 n(SO
 )=
)=(6)溶液中c(Na+)的范围是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出物质的化学式:A______ X______ 。
(2) B溶于水后的电离方程式为______________________ 。
鉴别B中阴离子的实验操作方法是_____________________ 。
(3)写出 A溶液与B溶液反应的离子方程式:
________________________________________________________________________ 。
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为________ 。(列出算式即可)
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出物质的化学式:A
(2) B溶于水后的电离方程式为
鉴别B中阴离子的实验操作方法是
(3)写出 A溶液与B溶液反应的离子方程式:
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某溶液无色、澄清,对该溶液初步分析后发现其中可能含有SO 、Na+、CO
、Na+、CO 、OH-、K+、Cl-中的若干种,然后又做了如下实验:
、OH-、K+、Cl-中的若干种,然后又做了如下实验:
①用紫色石蕊溶液测定溶液的酸碱性,结果紫色石蕊溶液显蓝色;
②取2mL溶液,加入BaCl2溶液和稀盐酸,生成了白色沉淀,没有产生气泡;
③将②中所得的混合物充分静置后,取上层澄清的液体,加入AgNO3溶液和稀硫酸,生成了白色沉淀。
(1)由上述实验可知:溶液中一定存在的离子是_____ (填离子符号,下同);一定不存在的离子是_____ ,原因是_____ (用离子方程式表示)。
(2)在上述实验操作中,有错误的步骤是_____ (填序号),原因是_____ 。
(3)改正实验操作后,仍生成白色沉淀,则接下来可以用_____ (用本章学过的方法)方法验证溶液中剩余未检验的离子。
 、Na+、CO
、Na+、CO 、OH-、K+、Cl-中的若干种,然后又做了如下实验:
、OH-、K+、Cl-中的若干种,然后又做了如下实验:①用紫色石蕊溶液测定溶液的酸碱性,结果紫色石蕊溶液显蓝色;
②取2mL溶液,加入BaCl2溶液和稀盐酸,生成了白色沉淀,没有产生气泡;
③将②中所得的混合物充分静置后,取上层澄清的液体,加入AgNO3溶液和稀硫酸,生成了白色沉淀。
(1)由上述实验可知:溶液中一定存在的离子是
(2)在上述实验操作中,有错误的步骤是
(3)改正实验操作后,仍生成白色沉淀,则接下来可以用
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某强酸性溶液X中可能含有Fe2+、Fe3+、Al3+、Ba2+、 、
、 、
、 、
、 、
、 中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
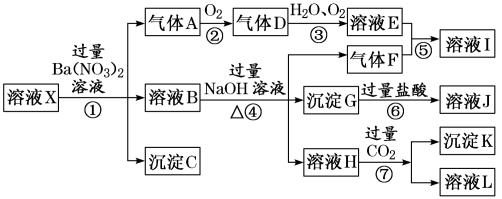
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有___________ 。
(2)溶液X中关于硝酸根离子的判断,正确的是___________ (填编号,下同)。
a.一定含有 b.一定不含有 c.可能含有
(3)转化①的离子方程式为___________ 。转化⑦的离子方程式为___________ 。
(4)在溶液J中通入二氧化硫气体,请写出反应的离子方程式___________ 。
 、
、 、
、 、
、 、
、 中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有
(2)溶液X中关于硝酸根离子的判断,正确的是
a.一定含有 b.一定不含有 c.可能含有
(3)转化①的离子方程式为
(4)在溶液J中通入二氧化硫气体,请写出反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室制备苯甲酸(相对分子质量122)、提纯及纯度测定步骤如下:
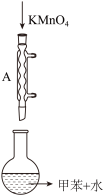
Ⅰ.往圆底烧瓶中加入2.5mL甲苯和140mL水,加热至沸,从仪器A上口(如图)分批加入10.4gKMnO4固体,最后用少量水将粘在仪器A内壁的KMnO4固体冲洗入圆底烧瓶内。
Ⅱ.继续煮沸并间歇性摇动圆底烧瓶,直至甲苯完全反应。
(反应方程式:C6H5CH3+KMnO4→C6H5COOK+MnO2+KOH+H2O)
Ⅲ.趁热过滤反应混合物,用少量热水洗涤滤渣,合并滤液和洗涤液,将滤液放在冷水浴中冷却,用浓硫酸酸化,使溶液从强碱性至强酸性,苯甲酸全部析出为止。
Ⅳ.过滤可得粗产品约2g。
Ⅴ.用重结晶法提纯。
Ⅵ.用碱滴定法测纯度,取0.1000g样品,溶于乙醇中,加入10mL水和2滴酚酞,用0.02mol/LNaOH溶液滴定。
回答下列问题。
(1)步骤Ⅰ中仪器A的名称是______ ,主要的作用是______ 。
(2)步骤Ⅱ加热前需要向圆底烧瓶中加入沸石,目的是______ ,反应基本完成的现象为______ 。
(3)步骤Ⅲ“趁热过滤反应混合物,用少量热水洗涤滤渣”中使用热水的目的是______ 。
(4)步骤Ⅴ中的合理步骤为a→______→______→______→______。______ (步骤不重复)
a.加入约100mL水(75℃)配制成热的浓溶液
b.加半匙活性炭
c.用少量沸水淋洗烧杯和漏斗中的固体,合并滤液
d.搅拌下将溶液煮沸3~5min,趁热过滤
e.冷却结晶,过滤、洗涤、晾干得苯甲酸纯品
(5)步骤Ⅵ中测得苯甲酸纯度大于100%的可能原因是_______ ,因此将步骤Ⅵ改为中和酸滴定法:称取0.1000g样品,溶于15mL浓度为0.1mol/LNaOH溶液中,加入2滴酚酞作指示剂,用0.1000mol/L盐酸调至红色消失,加入20mL乙醚,10滴溴酚蓝作指示剂,摇匀,用0.1000mol/L盐酸滴定,边滴边将水层和乙醚层充分摇匀使生成的苯甲酸及时被乙醚溶解,水层显淡绿色时为滴定终点,四次滴定平行数据如表,则苯甲酸的纯度为______ 。

Ⅰ.往圆底烧瓶中加入2.5mL甲苯和140mL水,加热至沸,从仪器A上口(如图)分批加入10.4gKMnO4固体,最后用少量水将粘在仪器A内壁的KMnO4固体冲洗入圆底烧瓶内。
Ⅱ.继续煮沸并间歇性摇动圆底烧瓶,直至甲苯完全反应。
(反应方程式:C6H5CH3+KMnO4→C6H5COOK+MnO2+KOH+H2O)
Ⅲ.趁热过滤反应混合物,用少量热水洗涤滤渣,合并滤液和洗涤液,将滤液放在冷水浴中冷却,用浓硫酸酸化,使溶液从强碱性至强酸性,苯甲酸全部析出为止。
Ⅳ.过滤可得粗产品约2g。
Ⅴ.用重结晶法提纯。
Ⅵ.用碱滴定法测纯度,取0.1000g样品,溶于乙醇中,加入10mL水和2滴酚酞,用0.02mol/LNaOH溶液滴定。
回答下列问题。
(1)步骤Ⅰ中仪器A的名称是
(2)步骤Ⅱ加热前需要向圆底烧瓶中加入沸石,目的是
(3)步骤Ⅲ“趁热过滤反应混合物,用少量热水洗涤滤渣”中使用热水的目的是
(4)步骤Ⅴ中的合理步骤为a→______→______→______→______。
a.加入约100mL水(75℃)配制成热的浓溶液
b.加半匙活性炭
c.用少量沸水淋洗烧杯和漏斗中的固体,合并滤液
d.搅拌下将溶液煮沸3~5min,趁热过滤
e.冷却结晶,过滤、洗涤、晾干得苯甲酸纯品
(5)步骤Ⅵ中测得苯甲酸纯度大于100%的可能原因是
| 序号 | 1 | 2 | 3 | 4 |
| 样品质量/g | 0.1000 | 0.1000 | 0.1000 | 0.1000 |
| 耗酸体积/mL | 8.00 | 8.02 | 7.98 | 8.96 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某工业漂白剂X由五种元素构成,可视为钠盐A与有机物B的加合物。取 该漂白剂X进行如下实验:
该漂白剂X进行如下实验:

固体D为某含氧酸的正盐与其酸式盐的混合物。气体F是纯净物,能使品红溶液褪色。气体C在标况下的密度约为 ,可与气体F反应生成淡黄色固体。气体体积已折算至标准状况。
,可与气体F反应生成淡黄色固体。气体体积已折算至标准状况。
(1)X构成的元素有钠、碳、氢和_______ ,X的化学式是_______ 。
(2)步骤Ⅰ中,气体B与足量新制 浊液反应的化学方程式为
浊液反应的化学方程式为_______ 。
(3)步骤Ⅱ,发生反应的离子方程式为_______ 。
(4)固体X投入滴有淀粉的碘水中,溶液蓝色褪去,可能的原因有_______ 。
(5)将气体F通入足量氨水中,转化为 的P溶液,然后通入一定量空气后,生成含Q的溶液。为确定P的氧化率,请设计简要的实验方案,并指明需要测定的物理量:
的P溶液,然后通入一定量空气后,生成含Q的溶液。为确定P的氧化率,请设计简要的实验方案,并指明需要测定的物理量:_______ 。
 该漂白剂X进行如下实验:
该漂白剂X进行如下实验:
固体D为某含氧酸的正盐与其酸式盐的混合物。气体F是纯净物,能使品红溶液褪色。气体C在标况下的密度约为
 ,可与气体F反应生成淡黄色固体。气体体积已折算至标准状况。
,可与气体F反应生成淡黄色固体。气体体积已折算至标准状况。(1)X构成的元素有钠、碳、氢和
(2)步骤Ⅰ中,气体B与足量新制
 浊液反应的化学方程式为
浊液反应的化学方程式为(3)步骤Ⅱ,发生反应的离子方程式为
(4)固体X投入滴有淀粉的碘水中,溶液蓝色褪去,可能的原因有
(5)将气体F通入足量氨水中,转化为
 的P溶液,然后通入一定量空气后,生成含Q的溶液。为确定P的氧化率,请设计简要的实验方案,并指明需要测定的物理量:
的P溶液,然后通入一定量空气后,生成含Q的溶液。为确定P的氧化率,请设计简要的实验方案,并指明需要测定的物理量:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,它们分别由下表中的离子组成:
为鉴别它们,分别完成以下实验,其结果如下:①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。请根据上述实验结果,填空:
(1)写出下列物质的化学式:A________ ,X________ 。
(2)B溶于水后的电离方程式为________ 。鉴别B中阴离子的实验操作方法是________ 。
(3)写出A溶液与B溶液反应的离子方程式:________ 。
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为________ (列出算式即可)。
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
(1)写出下列物质的化学式:A
(2)B溶于水后的电离方程式为
(3)写出A溶液与B溶液反应的离子方程式:
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为
您最近一年使用:0次



