某强酸性透明溶液中可能含有 、
、 、
、 、
、 、
、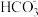 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:
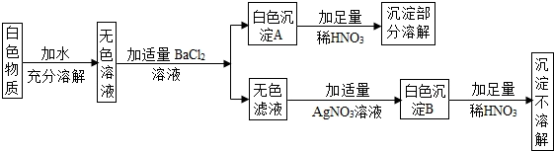
①取该溶液 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到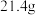 固体。
固体。
②向上述滤液中加入足量的 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。
已知:含 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。
(1)该溶液中一定含有___________ ;可能含有___________ ,可以用定性分析操作___________ 来进行检验。若含有,现象是:___________ 。
(2)计算:该 溶液中,若
溶液中,若 ,则
,则
___________ 。
(3)已知 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式___________ ;当某溶液 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有___________ 。
a. b.
b.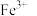 c.
c. d.
d. e.
e.
 、
、 、
、 、
、 、
、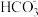 、
、 中的几种。为了确定其组成,现做以下实验:
中的几种。为了确定其组成,现做以下实验:①取该溶液
 ,加入足量的
,加入足量的 溶液,加热,得到标况下
溶液,加热,得到标况下 气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到
气体;同时产生红褐色沉淀,过滤,洗涤,干燥得到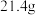 固体。
固体。②向上述滤液中加入足量的
 溶液,产生白色沉淀,过滤,洗涤,干燥得到
溶液,产生白色沉淀,过滤,洗涤,干燥得到 固体。
固体。已知:含
 的盐与强碱混合后,加热可以产生
的盐与强碱混合后,加热可以产生 。
。(1)该溶液中一定含有
(2)计算:该
 溶液中,若
溶液中,若 ,则
,则
(3)已知
 与
与 在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式
在溶液中“相遇”时会产生红褐色沉淀和无色气泡,写出相应的离子方程式 中大量存在
中大量存在 时,
时, 溶液中不可能大量含有
溶液中不可能大量含有a.
 b.
b.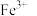 c.
c. d.
d. e.
e.
更新时间:2021-11-21 08:10:40
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某工业废水中存在大量的Na+、Cl-、Cu2+、SO ,欲除去其中的Cu2+、SO
,欲除去其中的Cu2+、SO ,设计工艺流程如图所示:
,设计工艺流程如图所示:_______ ,试剂 b溶液为_______ 。
(2)操作X为_______ ,试剂 a、b_______ (填“能”或“不能”)对调顺序。
(3)如果在工业废水中直接加入氢氧化钡溶液,写出发生反应的离子方程式_______ 。
(4)如何检验废水中的SO 已除尽
已除尽_______ (写出对应的操作及现象)。
 ,欲除去其中的Cu2+、SO
,欲除去其中的Cu2+、SO ,设计工艺流程如图所示:
,设计工艺流程如图所示: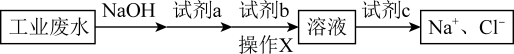
(2)操作X为
(3)如果在工业废水中直接加入氢氧化钡溶液,写出发生反应的离子方程式
(4)如何检验废水中的SO
 已除尽
已除尽
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某固体中含有 、可能含有
、可能含有 、
、 、
、 、
、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验:
中的几种离子,取等质量的两份该固体,进行如下实验:
I.将一份固体溶于水得无色透明溶液,加入足量 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
Ⅱ.将另一份固体与过量NaOH浓溶液混合后充分加热,产生 0.672L(标准状况下)。
0.672L(标准状况下)。
回答下列问题:
(1)该固体中一定没有的离子是______________ ;除 外,一定含有的离子是
外,一定含有的离子是______________ 。
(2)实验Ⅰ中沉淀质量减少的反应的离子方程式__________________________________________ 。
 、可能含有
、可能含有 、
、 、
、 、
、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验:
中的几种离子,取等质量的两份该固体,进行如下实验:I.将一份固体溶于水得无色透明溶液,加入足量
 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。Ⅱ.将另一份固体与过量NaOH浓溶液混合后充分加热,产生
 0.672L(标准状况下)。
0.672L(标准状况下)。回答下列问题:
(1)该固体中一定没有的离子是
 外,一定含有的离子是
外,一定含有的离子是(2)实验Ⅰ中沉淀质量减少的反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】化学小组通过实验探究分析一包KCl固体中的杂质成分并进行分离提纯。
(1)取该固体溶于水得无色溶液,则三位同学的检测结果正确的是___________ (填写代号)
(2)对该KCl固体精制的实验流程如图所示:

①配制100mL 0.1 KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、
KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、___________ 、胶头滴管;称量KOH固体时间过长,所配溶液的浓度___________ (填“偏高”“偏低”或“无影响”)。
②试剂A的化学式为___________ 。
③操作1的名称是___________ 。
④滴加稀盐酸后,大量减少的离子有___________ 。
(3)准确称取134.5g该固体溶于水,加入足量 溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为___________ 。
(1)取该固体溶于水得无色溶液,则三位同学的检测结果正确的是
| 检测同学 | 检测结果 |
| 甲 | KCl、 、 、 |
| 乙 | KCl、 、 、 |
| 丙 | KCl、 、 、 |

①配制100mL 0.1
 KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、
KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、②试剂A的化学式为
③操作1的名称是
④滴加稀盐酸后,大量减少的离子有
(3)准确称取134.5g该固体溶于水,加入足量
 溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】I.将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、SO 、OH-、CO
、OH-、CO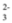 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:
①取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
②取少许溶液滴入 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。
③取少许溶液先滴加稀硝酸再加 溶液,产生白色沉淀。
溶液,产生白色沉淀。
④再取少许原溶液滴入少量 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
(1)根据以上现象判断,原溶液中肯定不存在的离子是___________ ;
(2)写出实验④中发生反应的离子方程式___________ ;
(3)要确定原溶液中是否含有 ,应进行的实验操作(写出操作步骤)是:
,应进行的实验操作(写出操作步骤)是:___________ 。
Ⅱ.利用下图可以从不同角度研究含铁物质的性质及其转化关系。图中甲~己均是含铁元素的中学常见物质。回答下列问题:
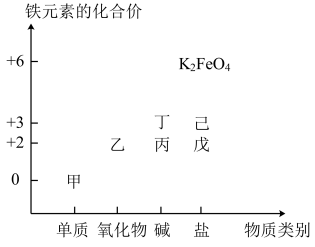
(4) 常用作杀菌消毒剂,从铁元素化合价的角度分析是因其具有
常用作杀菌消毒剂,从铁元素化合价的角度分析是因其具有___________ 性。下列关于甲~己的说法正确的是___________ (填字母)。
a.若戊、己均为盐酸盐,则均可以由甲通过一步反应制得
b.乙属于碱性氧化物,能与任何酸反应
c.丙、丁、戊、己均属于电解质
d.甲、乙、丙、戊均既有氧化性又有还原性
(5)已知甲与稀硝酸反应的化学方程式为:甲+HNO3(稀)→戊+己+NO↑+H2O(未配平)。若产物中戊和己的分子个数比为3∶1,则该反应的化学方程式为(需配平):___________ 。
(6) 可以通过以下反应制得,请配平下列离子方程式:
可以通过以下反应制得,请配平下列离子方程式:___________
___________ ___________
___________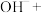 ___________
___________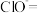 ___________
___________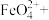 ___________
___________ ___________
___________
 、OH-、CO
、OH-、CO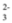 和Cl-,取该溶液进行如下实验:
和Cl-,取该溶液进行如下实验:①取少量溶液滴入紫色石蕊溶液,溶液呈蓝色。
②取少许溶液滴入
 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。③取少许溶液先滴加稀硝酸再加
 溶液,产生白色沉淀。
溶液,产生白色沉淀。④再取少许原溶液滴入少量
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。(1)根据以上现象判断,原溶液中肯定不存在的离子是
(2)写出实验④中发生反应的离子方程式
(3)要确定原溶液中是否含有
 ,应进行的实验操作(写出操作步骤)是:
,应进行的实验操作(写出操作步骤)是:Ⅱ.利用下图可以从不同角度研究含铁物质的性质及其转化关系。图中甲~己均是含铁元素的中学常见物质。回答下列问题:

(4)
 常用作杀菌消毒剂,从铁元素化合价的角度分析是因其具有
常用作杀菌消毒剂,从铁元素化合价的角度分析是因其具有a.若戊、己均为盐酸盐,则均可以由甲通过一步反应制得
b.乙属于碱性氧化物,能与任何酸反应
c.丙、丁、戊、己均属于电解质
d.甲、乙、丙、戊均既有氧化性又有还原性
(5)已知甲与稀硝酸反应的化学方程式为:甲+HNO3(稀)→戊+己+NO↑+H2O(未配平)。若产物中戊和己的分子个数比为3∶1,则该反应的化学方程式为(需配平):
(6)
 可以通过以下反应制得,请配平下列离子方程式:
可以通过以下反应制得,请配平下列离子方程式:___________
 ___________
___________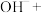 ___________
___________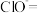 ___________
___________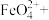 ___________
___________ ___________
___________
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:

(1)A的名称是____________ ;F的化学式是 _____________ 。
(2)B→D反应的化学方程式__________________________________ 。
(3)F在空气中遇水蒸气产生白雾现象,这白雾实际上是___________________ 。

(1)A的名称是
(2)B→D反应的化学方程式
(3)F在空气中遇水蒸气产生白雾现象,这白雾实际上是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】中学化学学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质间的转化关系如图所示(部分产物已略去)
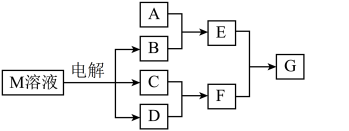
(1)写出用惰性电极电解M溶液的离子方程式:______________________ 。写出F的电子式:__________________________ 。
(2)若A是地売中含量最多的金属元素,将A的氯化物溶液0.2mol/L和氢氧化钠溶液等体积混合,得到的沉淀物中A元素与溶液中A元素的质量相等,则氢氧化钠溶液的物质的量浓度可能为____________ 。
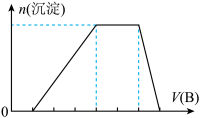
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如图所示,则A与B溶液反应后溶液中的溶质为______ (填化学式)。

(4)若A是一种正盐,A能分别与B、F溶液反应生成无色且具有刺激性气味的气体,则A的化学式为_____________ 。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入KSCN溶液后显红色,则由A转化成E的离子方程式是________________________________ 。
(6)若A是一种溶液,只可能有H+、NH4+、Mg2+、Fe3+、Al3+、SO42—、CO32—中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生如图所示变化,由此可知,该溶液中肯定含有的离子及其浓度之比为____________ 。

(1)写出用惰性电极电解M溶液的离子方程式:
(2)若A是地売中含量最多的金属元素,将A的氯化物溶液0.2mol/L和氢氧化钠溶液等体积混合,得到的沉淀物中A元素与溶液中A元素的质量相等,则氢氧化钠溶液的物质的量浓度可能为
(3)若A是CO2气体,A与B溶液反应后所得的溶液再与盐酸反应,放出气体的物质的量与所加盐酸体积之间的关系如图所示,则A与B溶液反应后溶液中的溶质为

(4)若A是一种正盐,A能分别与B、F溶液反应生成无色且具有刺激性气味的气体,则A的化学式为
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入KSCN溶液后显红色,则由A转化成E的离子方程式是
(6)若A是一种溶液,只可能有H+、NH4+、Mg2+、Fe3+、Al3+、SO42—、CO32—中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生如图所示变化,由此可知,该溶液中肯定含有的离子及其浓度之比为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请填写下列空白。
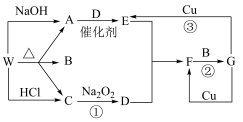
(1)化合物W可能是________ 或__________ (填化学式),C的结构式是________ ,
(2)D的组成元素在周期表中的位置是__________ 。
(3)反应③的离子方程式:________________________ 。
(4)已知在催化剂作用下,E与CO反应生成参与大气生态循环的无毒物质,请写出该反应的化学方程式______________________________________ 。
(5)在反应②中,发生还原反应和氧化反应的物质的质量之比为__________ 。

(1)化合物W可能是
(2)D的组成元素在周期表中的位置是
(3)反应③的离子方程式:
(4)已知在催化剂作用下,E与CO反应生成参与大气生态循环的无毒物质,请写出该反应的化学方程式
(5)在反应②中,发生还原反应和氧化反应的物质的质量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】一种将废水(含Ca2+、Mg2+、CN-及悬浮物)通过净化、杀菌消毒生产自来水的流程示意图如下:
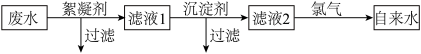
(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是(填标号)______。
(2)绿矾是常用的絮凝剂,它在水中最终生成(填化学式)沉淀____ ,下列物质中也可以作为絮凝剂的有(填标号)______ 。
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO )越大,净水效果越好,原因是
)越大,净水效果越好,原因是___ 。
(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加_后加__ ,理由是_____ 。此时Ca2+、Mg2+离子分别形成______ 、______ (填化学式)而沉淀下来。
(4)向滤液2中通入Cl2的作用有两种:一是利用生成的(填名称)______ 、______ 具有强氧化性能杀死水中的病菌;二是将CN-氧化成CO2和N2,从而消除CN-的毒性,若参加反应的C12与CN-的物质的量之比为5: 2,则该反应的离子方程式是______ 。

(1)絮凝剂除去悬浮物质时发生物理变化和化学变化,下列既发生物理变化又发生化学变化的是(填标号)______。
| A.蒸馏 | B.煤干馏 | C.风化 | D.分馏 |
A.NH4Cl B.食盐 C.明矾 D.CH3COONa
若用FeCl3作絮凝剂,实践中发现废水中的c(HCO
 )越大,净水效果越好,原因是
)越大,净水效果越好,原因是(3)加沉淀剂是为了除去Ca2+、Mg2+,若加入生石灰和纯碱作沉淀剂,试剂添加时先加_后加
(4)向滤液2中通入Cl2的作用有两种:一是利用生成的(填名称)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某工厂利用黄铁矿(FeS2)和电解金属锰后的阳极渣(主要成分MnO2,杂质为Pb、Fe、Cu元素的化合物)为原料制备高性能磁性材料MnCO3的I工艺流程如下:
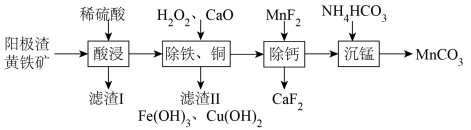
回答下列问题:
(1)FeS2中硫元素化合价为___________ ,滤渣I的成分除了S还有___________ 。
(2)写出任意两种加快酸浸速率的措施___________ 、___________ 。“除铁、铜”过程中加入H2O2的目的是___________ 。
(3)请结合平衡移动原理解释“除钙”时溶液酸度不宜过高,否则溶液中Ca2+沉淀不完全的原因是:___________ 。
(4)“沉锰”时发生反应的离子方程式为:___________ 。“沉锰”时需缓慢向含MnSO4的溶液中滴加NH4HCO3,否则会发生反应MnCO3(s) + 2OH-(aq) Mn(OH)2(s) +
Mn(OH)2(s) + (aq)而生成Mn(OH)2,该反应的平衡常数K=
(aq)而生成Mn(OH)2,该反应的平衡常数K=___________ (保留一位小数,已知: Ksp[Mn(OH)2]=1.9 ×10-13,Ksp(MnCO3)=2.2× 10-11)。

回答下列问题:
(1)FeS2中硫元素化合价为
(2)写出任意两种加快酸浸速率的措施
(3)请结合平衡移动原理解释“除钙”时溶液酸度不宜过高,否则溶液中Ca2+沉淀不完全的原因是:
(4)“沉锰”时发生反应的离子方程式为:
 Mn(OH)2(s) +
Mn(OH)2(s) + (aq)而生成Mn(OH)2,该反应的平衡常数K=
(aq)而生成Mn(OH)2,该反应的平衡常数K=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某实验小组为探究 与
与 反应后的产物,做如下探究实验。
反应后的产物,做如下探究实验。
【查阅资料】
① 为砖红色固体,不溶于水;
为砖红色固体,不溶于水;
②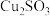 为黄色固体,不溶于水;
为黄色固体,不溶于水;
③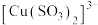 为无色配合离子、
为无色配合离子、 为无色配合离子、
为无色配合离子、 为深蓝色配合离子。
为深蓝色配合离子。
【实验探究】
实验1:①向2mL 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始出现黄色沉淀,但无气体产生。
溶液,开始出现黄色沉淀,但无气体产生。
②继续加入 溶液,最终沉淀消失。经检验,溶液中生成
溶液,最终沉淀消失。经检验,溶液中生成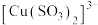 离子。
离子。
实验2:向90℃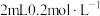 的
的 溶液中滴加
溶液中滴加 的
的 溶液,直接生成砖红色沉淀。
溶液,直接生成砖红色沉淀。
实验3:向2mL 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始阶段有蓝色沉淀出现。
溶液,开始阶段有蓝色沉淀出现。
(1)某同学认为实验1黄色沉淀中有少量 ,该同学认为是
,该同学认为是 、
、 相互促进水解产生的,用离子方程式表示生成
相互促进水解产生的,用离子方程式表示生成 沉淀的过程:
沉淀的过程:_______ 。
(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为_______ 。
(3)经检验,实验2所得溶液中有大量 、
、 生成。该实验中
生成。该实验中 表现
表现_______ 性,写出该实验中反应的离子方程式:_______ 。
(4)某同学设计了如图所示的电化学装置,探究 与
与 的反应。该装置中左侧烧杯中的石墨电极做
的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。

 与
与 反应后的产物,做如下探究实验。
反应后的产物,做如下探究实验。【查阅资料】
①
 为砖红色固体,不溶于水;
为砖红色固体,不溶于水;②
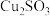 为黄色固体,不溶于水;
为黄色固体,不溶于水;③
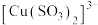 为无色配合离子、
为无色配合离子、 为无色配合离子、
为无色配合离子、 为深蓝色配合离子。
为深蓝色配合离子。【实验探究】
实验1:①向2mL
 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始出现黄色沉淀,但无气体产生。
溶液,开始出现黄色沉淀,但无气体产生。②继续加入
 溶液,最终沉淀消失。经检验,溶液中生成
溶液,最终沉淀消失。经检验,溶液中生成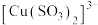 离子。
离子。实验2:向90℃
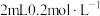 的
的 溶液中滴加
溶液中滴加 的
的 溶液,直接生成砖红色沉淀。
溶液,直接生成砖红色沉淀。实验3:向2mL
 的
的 溶液中滴加
溶液中滴加 的
的 溶液,开始阶段有蓝色沉淀出现。
溶液,开始阶段有蓝色沉淀出现。(1)某同学认为实验1黄色沉淀中有少量
 ,该同学认为是
,该同学认为是 、
、 相互促进水解产生的,用离子方程式表示生成
相互促进水解产生的,用离子方程式表示生成 沉淀的过程:
沉淀的过程:(2)若要进一步检验黄色沉淀中有Cu(OH)2,可采用的具体实验方法为
(3)经检验,实验2所得溶液中有大量
 、
、 生成。该实验中
生成。该实验中 表现
表现(4)某同学设计了如图所示的电化学装置,探究
 与
与 的反应。该装置中左侧烧杯中的石墨电极做
的反应。该装置中左侧烧杯中的石墨电极做
您最近一年使用:0次

 等离子,试推断:
等离子,试推断: