(1)同温同压下,含氧元素质量相同的二氧化硫和三氧化硫的质量比为:__________ ,
(2)25℃时,质量比为8:11的O2和CO2,体积之比为1:2,则这两种气体的压强之比为___________ 。
(3)标准状况下,等体积的氧气和某气体质量比为1:2.5,则该气体的摩尔质量为____________ 。
(4)已知t℃时NaOH的溶解度为S g,该温度下NaOH饱和溶液溶质的物质的量浓度是cmol/L,则此饱和溶液的密度为(用S、c表示)_________________ g/mL。
(5)黑索金广泛用于装填各种军用弹药,它的摩尔质量为222g/mol,一定量的黑索金引爆产生等体积的N2、H2O及CO气体,黑索金的化学式为_______________ 。
(6)在恒温条件下,向2L恒容密闭容器中加入1molN2和3molH2发生反应N2+3H2=2NH3,起始时压强为P0,反应一段时间之后压强为P1,请用P0、P1表示此时N2的转化率__________ ,(转化率为反应掉的某种反应物的量占该种反应物起始量的百分数)
(2)25℃时,质量比为8:11的O2和CO2,体积之比为1:2,则这两种气体的压强之比为
(3)标准状况下,等体积的氧气和某气体质量比为1:2.5,则该气体的摩尔质量为
(4)已知t℃时NaOH的溶解度为S g,该温度下NaOH饱和溶液溶质的物质的量浓度是cmol/L,则此饱和溶液的密度为(用S、c表示)
(5)黑索金广泛用于装填各种军用弹药,它的摩尔质量为222g/mol,一定量的黑索金引爆产生等体积的N2、H2O及CO气体,黑索金的化学式为
(6)在恒温条件下,向2L恒容密闭容器中加入1molN2和3molH2发生反应N2+3H2=2NH3,起始时压强为P0,反应一段时间之后压强为P1,请用P0、P1表示此时N2的转化率
更新时间:2017-10-26 20:01:37
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】在150℃,101 kPa下由CO、H2组成的混合气体共6 g,其相对氢气的密度为7.5,将该气体在充足的氧气中完全燃烧后的产物通过足量的Na2O2粉末,使Na2O2粉末增重的质量为_______ g,燃烧消耗的氧气在标准状况下的体积应是_______ L。
您最近半年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】(1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_________ (填选项序号)。

(2)设NA为阿伏加德罗常数的数值,如果ag某气体中含有的分子数为b,那么cg该气体在标准状况下的体积约是__________ 。
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2+3O2=XO2+2YO2,冷却后(产物均为气态),在标准状况下测得生成物的体积是336mL,密度是2.56g/L。
①反应前O2的体积是________ mL(标准状况),化合物XY2的摩尔质量是________ 。
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为______ 和______ (写元素符号)。

(2)设NA为阿伏加德罗常数的数值,如果ag某气体中含有的分子数为b,那么cg该气体在标准状况下的体积约是
(3)液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2+3O2=XO2+2YO2,冷却后(产物均为气态),在标准状况下测得生成物的体积是336mL,密度是2.56g/L。
①反应前O2的体积是
②若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为
您最近半年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某化工厂以甲烷为主要原料来制取合成甲醇及合成氨的原料,其主要反应为:
 ①(反应中CH4转化率为1)
①(反应中CH4转化率为1)
 ②(反应中CH4转化率为1)
②(反应中CH4转化率为1)
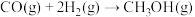 (反应中CO转化率为
(反应中CO转化率为 )
)
合成工艺如下:
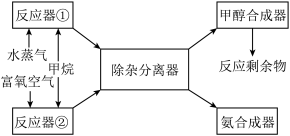
请回答下列问题(所有气体体积均折算为标准状况):
(1)若只用反应器①来直接合成甲醇。当充入反应器①的甲烷和水蒸气的体积分别为672m3和2240m3时,反应剩余物中CO为_____ mol、H2为_______ mol;
(2)若CH4同时和H2O(g)及O2(g)反应,则am3 CH4按上述两式完全反应,产物气体的体积V的范围为________ 。
(3)若充入反应器①的甲烷和水蒸气的体积分别为l体积和3体积,反应剩余物中: V(H2):V(N2):V(CO)=3:1:l。则充入反应器②的富氧空气(只含N2和H2)的体积为_______ ;富氧空气中氧气体积分数为____ 。
(4)若将25%的富氧空气、CH4和H2O(g)混合并充分反应,反应的产物中n(H2):n(N2)=3:1,来合成氨气,则反应中的H2O(g)富氧空气的物质的量之比为_______ 。
 ①(反应中CH4转化率为1)
①(反应中CH4转化率为1) ②(反应中CH4转化率为1)
②(反应中CH4转化率为1)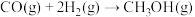 (反应中CO转化率为
(反应中CO转化率为 )
)合成工艺如下:

请回答下列问题(所有气体体积均折算为标准状况):
(1)若只用反应器①来直接合成甲醇。当充入反应器①的甲烷和水蒸气的体积分别为672m3和2240m3时,反应剩余物中CO为
(2)若CH4同时和H2O(g)及O2(g)反应,则am3 CH4按上述两式完全反应,产物气体的体积V的范围为
(3)若充入反应器①的甲烷和水蒸气的体积分别为l体积和3体积,反应剩余物中: V(H2):V(N2):V(CO)=3:1:l。则充入反应器②的富氧空气(只含N2和H2)的体积为
(4)若将25%的富氧空气、CH4和H2O(g)混合并充分反应,反应的产物中n(H2):n(N2)=3:1,来合成氨气,则反应中的H2O(g)富氧空气的物质的量之比为
您最近半年使用:0次
计算题
|
较难
(0.4)
【推荐1】含AlCl313.35g的溶液中加入一定浓度的NaOH溶液100mL后,结果得到沉淀3.9g。
(1)写出可能发生反应的离子方程式:
_______________________________ 、_________________________________
(2)上述NaOH溶液物质的量浓度可能是多少?
______________________ 。
(1)写出可能发生反应的离子方程式:
(2)上述NaOH溶液物质的量浓度可能是多少?
您最近半年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为________ L,NO2的体积为________ L。
(2)待产生的气体全部释放后,向溶液中加入VmLamol/L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸溶液的浓度为__________ mol/L。
(1)NO的体积为
(2)待产生的气体全部释放后,向溶液中加入VmLamol/L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近半年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)1 L Al2(SO4)3和MgSO4的混合溶液中,含Mg2+ 2.4 g,SO 的物质的量浓度为1 mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1 mol·L-1,则Al3+的物质的量浓度是_______ 。
(2)若用质量分数为98%,密度为1.84g·cm-3的浓H2SO4来配制0.5 mol·L−1H2SO4溶液500mL,需要量取浓硫酸_______ mL(结果保留一位小数)。
(3)若将质量分数为a%,物质的量浓度的c1mol/L的稀硫酸蒸发掉一定量的水,使之成为2a%的c2mol/L的稀硫酸,则c1和c2 的关系是_______
A.c1=2c2 B.2c1>c2 C.2c1<c2 D.无法确定
(4)95%的16.52mol/L的酒精溶液,其47.5%的酒精溶液物质的量浓度为_______
A.大于8.26mol/L B.等于8.26mol/L C.小于8.26mol/L D.无法确定
(5)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,碳与氧两种原子的数目之比为_______ 。
(6)过氧化钙是一种安全无毒的物质,称取0.542g过氧化钙样品,先溶于适量的稀盐酸中(发生反应:2CaO2·xH2O +4HCl 2CaCl2+O2↑+(2+x)H2O,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。则样品中CaO2·xH2O的x值为
2CaCl2+O2↑+(2+x)H2O,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。则样品中CaO2·xH2O的x值为_______ 。
(7)在质量分数为28﹪的KOH水溶液中,OH-与H2O分子数之比是_______ 。
 的物质的量浓度为1 mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1 mol·L-1,则Al3+的物质的量浓度是(2)若用质量分数为98%,密度为1.84g·cm-3的浓H2SO4来配制0.5 mol·L−1H2SO4溶液500mL,需要量取浓硫酸
(3)若将质量分数为a%,物质的量浓度的c1mol/L的稀硫酸蒸发掉一定量的水,使之成为2a%的c2mol/L的稀硫酸,则c1和c2 的关系是
A.c1=2c2 B.2c1>c2 C.2c1<c2 D.无法确定
(4)95%的16.52mol/L的酒精溶液,其47.5%的酒精溶液物质的量浓度为
A.大于8.26mol/L B.等于8.26mol/L C.小于8.26mol/L D.无法确定
(5)在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,该混合气体中,碳与氧两种原子的数目之比为
(6)过氧化钙是一种安全无毒的物质,称取0.542g过氧化钙样品,先溶于适量的稀盐酸中(发生反应:2CaO2·xH2O +4HCl
 2CaCl2+O2↑+(2+x)H2O,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。则样品中CaO2·xH2O的x值为
2CaCl2+O2↑+(2+x)H2O,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。则样品中CaO2·xH2O的x值为(7)在质量分数为28﹪的KOH水溶液中,OH-与H2O分子数之比是
您最近半年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】硫酸的摩尔质量是__________ ,98g纯净的硫酸的物质的量是________ ,其中约含有_______ 个硫酸分子,约含有__________ 个氢原子,约含__________ 个氧原子,____ 摩尔氧原子。
您最近半年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】将200mlBaCl2溶液等分为两份,一份中加入100ml物质的量浓度为0.1mol/L的稀硫酸,恰好完全沉淀;另一份中加入足量AgNO3溶液,使其充分沉淀。试计算:
(1)此BaCl2溶液的物质的量浓度是________
(2)上述反应中生成的AgCl沉淀的质量是________
(1)此BaCl2溶液的物质的量浓度是
(2)上述反应中生成的AgCl沉淀的质量是
您最近半年使用:0次
计算题
|
较难
(0.4)
【推荐3】I.在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g。此混合物中CO和CO2的物质的量比是______ ,CO的体积分数是______ ,CO的质量分数是___ ,混合气体中C和O的原子个数比是_____ ,混合气体的平均摩尔质量是_____ 。
II.现有mg某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为________ 个。
(2)该气体若溶于1L水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为__________ mol·L-1。
II.现有mg某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为
(2)该气体若溶于1L水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为
您最近半年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某化工厂以甲烷为主要原料来制取合成甲醇及合成氨的原料,其主要反应为:
 ①(反应中CH4转化率为1)
①(反应中CH4转化率为1)
 ②(反应中CH4转化率为1)
②(反应中CH4转化率为1)
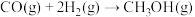 (反应中CO转化率为
(反应中CO转化率为 )
)
合成工艺如下:

请回答下列问题(所有气体体积均折算为标准状况):
(1)若只用反应器①来直接合成甲醇。当充入反应器①的甲烷和水蒸气的体积分别为672m3和2240m3时,反应剩余物中CO为_____ mol、H2为_______ mol;
(2)若CH4同时和H2O(g)及O2(g)反应,则am3 CH4按上述两式完全反应,产物气体的体积V的范围为________ 。
(3)若充入反应器①的甲烷和水蒸气的体积分别为l体积和3体积,反应剩余物中: V(H2):V(N2):V(CO)=3:1:l。则充入反应器②的富氧空气(只含N2和H2)的体积为_______ ;富氧空气中氧气体积分数为____ 。
(4)若将25%的富氧空气、CH4和H2O(g)混合并充分反应,反应的产物中n(H2):n(N2)=3:1,来合成氨气,则反应中的H2O(g)富氧空气的物质的量之比为_______ 。
 ①(反应中CH4转化率为1)
①(反应中CH4转化率为1) ②(反应中CH4转化率为1)
②(反应中CH4转化率为1)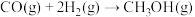 (反应中CO转化率为
(反应中CO转化率为 )
)合成工艺如下:

请回答下列问题(所有气体体积均折算为标准状况):
(1)若只用反应器①来直接合成甲醇。当充入反应器①的甲烷和水蒸气的体积分别为672m3和2240m3时,反应剩余物中CO为
(2)若CH4同时和H2O(g)及O2(g)反应,则am3 CH4按上述两式完全反应,产物气体的体积V的范围为
(3)若充入反应器①的甲烷和水蒸气的体积分别为l体积和3体积,反应剩余物中: V(H2):V(N2):V(CO)=3:1:l。则充入反应器②的富氧空气(只含N2和H2)的体积为
(4)若将25%的富氧空气、CH4和H2O(g)混合并充分反应,反应的产物中n(H2):n(N2)=3:1,来合成氨气,则反应中的H2O(g)富氧空气的物质的量之比为
您最近半年使用:0次
计算题
|
较难
(0.4)
【推荐2】现对三种不同的镁铝合金样品进行编号,做以下实验探究。
(1)取样品①m1g,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到固体的质量仍然为m1g.合金中镁的质量分数为_____ (保留2位小数,下同)。
(2)取样品②m2g,与足量稀硫酸反应,固体完全溶解时得到气体的体积为VL(标准状况)。m2的取值范围是_____ 。
(3)取样品③0.918g与30.00mL、2.00mL盐酸充分反应后,得到672mL气体(标准状况)。剩余合金0.306g(认为合金中镁、铝与酸的反应同时发生)。然后在反应后所得体系中继续加1.00mol/L的NaOH溶液,恰好使所有铝元素均不以沉淀形式存在。则需要加入1.00mol/L的NaOH溶液_____ mL。
(1)取样品①m1g,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到固体的质量仍然为m1g.合金中镁的质量分数为
(2)取样品②m2g,与足量稀硫酸反应,固体完全溶解时得到气体的体积为VL(标准状况)。m2的取值范围是
(3)取样品③0.918g与30.00mL、2.00mL盐酸充分反应后,得到672mL气体(标准状况)。剩余合金0.306g(认为合金中镁、铝与酸的反应同时发生)。然后在反应后所得体系中继续加1.00mol/L的NaOH溶液,恰好使所有铝元素均不以沉淀形式存在。则需要加入1.00mol/L的NaOH溶液
您最近半年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定某碳酸钠样品中Na2CO3的质量分数,某探究性学习小组设计以下两种方案。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:
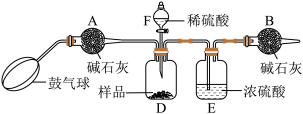
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是_______ ;操作⑥中,鼓入空气的作用是_______ ;
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式_______ 。
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是_______ 。
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。
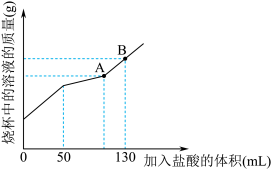
(4)加入50mL盐酸时,写出反应的离子反应方程式_______ 。
(5)在这个样品中,含碳酸钠的质量分数为_______ 。
(6)A点时,溶液溶质是_______ ,所得溶质质量分数为_______ 。(忽略体积的微小变化,结果保留小数点后两位)。
Ⅰ.取样品bg,设计如下实验方案,操作步骤如下:

①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(a1g)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(a2g)。
⑧计算
(1)操作③中,鼓入空气的作用是
(2)根据题干所给的数据列出样品中Na2CO3的质量分数表达式
(3)经实验发现最终所得的 Na2CO3的质量分数超过100%,其可能的原因是
Ⅱ.现有碳酸钠和氯化钠的混合物样品25g,将其放入干净的烧杯中,加入一定量的水,使其完全溶解得到200mL溶液。向所得溶液中慢慢加入4mol•L-1的盐酸,烧杯中溶液的质量与加入盐酸的体积关系曲线如图所示。请回答下列问题。

(4)加入50mL盐酸时,写出反应的离子反应方程式
(5)在这个样品中,含碳酸钠的质量分数为
(6)A点时,溶液溶质是
您最近半年使用:0次



